酸、堿、鹽是幾類重要的化合物,它們之間能發(fā)生復分解反應。
(1)復分解反應發(fā)生的條件是有沉淀析出,或有氣體放出,或有水水生成。
(2)某化學小組進行“酸和堿的中和反應”實驗:將鹽酸滴入一定量的澄清石灰水中,實驗無明顯現(xiàn)象。取反應后的部分溶液加熱、蒸干,得到白色固體。
以下是探究白色固體成分的實驗,已知氯化鈣溶液呈中性。請?zhí)顚懭绫恚?br />
| 實驗操作 | 測定結果 | 白色固體成分 |
| 用pH試紙測定反應后溶液的酸堿度,操作方法是 用潔凈玻璃棒蘸取溶液滴到pH試紙上,把試紙顯示的顏色與標準比色卡比較 用潔凈玻璃棒蘸取溶液滴到pH試紙上,把試紙顯示的顏色與標準比色卡比較 |
pH>7 |
CaCl2、Ca(OH)2 CaCl2、Ca(OH)2
|
|
pH≤7 pH≤7
|
CaCl2 |
(3)“粗鹽提純”指除去NaCl中的泥沙和MgCl2、CaCl2、Na2SO4等雜質(zhì)。某同學設計了除去三種可溶性雜質(zhì)的實驗方案:先將固體溶解,然后向其中依次加入過量的BaCl2、NaOH、Na2CO3溶液,充分反應后過濾,蒸發(fā)結晶。請回答:
①溶解、過濾和蒸發(fā)操作中都用到一種玻璃儀器,該儀器在蒸發(fā)操作中的作用是什么?
攪拌,使受熱均勻,防止液滴飛濺
攪拌,使受熱均勻,防止液滴飛濺
,②加入Na2CO3溶液的目的是什么?
除去溶液中的鈣、鋇離子
除去溶液中的鈣、鋇離子
,③以上方案還需完善,請說明原因并加以補充
經(jīng)上述處理后的溶液中還含有氫氧化鈉和碳酸鈉等雜質(zhì),呈堿性,因此,還需加入適量稀鹽酸和氫氧化鈉、碳酸鈉反應,從而把過量的氫氧化鈉、碳酸鈉除去,調(diào)節(jié)溶液的pH=7
經(jīng)上述處理后的溶液中還含有氫氧化鈉和碳酸鈉等雜質(zhì),呈堿性,因此,還需加入適量稀鹽酸和氫氧化鈉、碳酸鈉反應,從而把過量的氫氧化鈉、碳酸鈉除去,調(diào)節(jié)溶液的pH=7
。(4)LiOH和NaOH的化學性質(zhì)相似。“神舟”飛船內(nèi),可用盛有LiOH的過濾網(wǎng)吸收航天員呼出的氣體,以降低CO2含量。請計算:用LiOH完全吸收176g CO2,生成Li2CO3和H2O,理論上至少需要LiOH的質(zhì)量是多少?
【答案】水;用潔凈玻璃棒蘸取溶液滴到pH試紙上,把試紙顯示的顏色與標準比色卡比較;CaCl2、Ca(OH)2;pH≤7;攪拌,使受熱均勻,防止液滴飛濺;除去溶液中的鈣、鋇離子;經(jīng)上述處理后的溶液中還含有氫氧化鈉和碳酸鈉等雜質(zhì),呈堿性,因此,還需加入適量稀鹽酸和氫氧化鈉、碳酸鈉反應,從而把過量的氫氧化鈉、碳酸鈉除去,調(diào)節(jié)溶液的pH=7
【解答】
【點評】
聲明:本試題解析著作權屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/5/23 20:38:36組卷:14引用:3難度:0.4
相似題
-
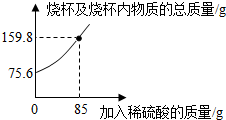 1.為測定某碳素鋼樣品中鐵的質(zhì)量分數(shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為52.2g的燒杯中,然后緩慢加入一定質(zhì)量的稀硫酸,當加稀硫酸質(zhì)量為85g時,反應恰好完全(雜質(zhì)不反應且產(chǎn)生的氣體全部逸出),反應過程中的質(zhì)量關系如圖.完成下列問題:
1.為測定某碳素鋼樣品中鐵的質(zhì)量分數(shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為52.2g的燒杯中,然后緩慢加入一定質(zhì)量的稀硫酸,當加稀硫酸質(zhì)量為85g時,反應恰好完全(雜質(zhì)不反應且產(chǎn)生的氣體全部逸出),反應過程中的質(zhì)量關系如圖.完成下列問題:
(1)該實驗取用的樣品質(zhì)量為g.
(2)計算樣品中鐵的質(zhì)量分數(shù)(寫出解題過程).發(fā)布:2025/1/9 8:0:2組卷:139引用:39難度:0.1 -
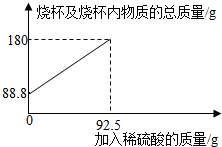 2.為測定某碳素鋼樣品中鐵的質(zhì)量分數(shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為51.8克的燒杯中,然后逐步加入一定質(zhì)量分數(shù)的稀硫酸,當加入92.5g稀硫酸時恰好完全反應,加入稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關系如圖。
2.為測定某碳素鋼樣品中鐵的質(zhì)量分數(shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為51.8克的燒杯中,然后逐步加入一定質(zhì)量分數(shù)的稀硫酸,當加入92.5g稀硫酸時恰好完全反應,加入稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關系如圖。
(1)該實驗取用的樣品質(zhì)量為g。
(2)反應后所得溶液中的溶質(zhì)的質(zhì)量分數(shù)。(寫出計算過程,結果保留一位小數(shù))
(3)反應結束后,小明不慎向燒杯中多加了10g稀硫酸,若在圖中補繪此過程中稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關系圖,所得線段的終點位于線段AB延長線的(填:上方、下方或線上)。發(fā)布:2025/1/9 8:0:2組卷:4引用:1難度:0.3 -
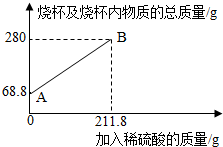 3.為測定某碳素鋼樣品中鐵的質(zhì)量分數(shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為51.8克的燒杯中,然后逐步加入一定質(zhì)量分數(shù)的稀硫酸,當加入211.8g稀硫酸時恰好完全反應,加入稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關系如圖。
3.為測定某碳素鋼樣品中鐵的質(zhì)量分數(shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為51.8克的燒杯中,然后逐步加入一定質(zhì)量分數(shù)的稀硫酸,當加入211.8g稀硫酸時恰好完全反應,加入稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關系如圖。
(1)該實驗取用的樣品質(zhì)量為g。
(2)求樣品中鐵的質(zhì)量分數(shù);反應后所得溶液中的溶質(zhì)的質(zhì)量分數(shù)。(寫出計算過程,結果保留一位小數(shù))
(3)反應結束后,小明不慎向燒杯中多加了20g稀硫酸,若在圖中補繪此過程中稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關系圖,所得線段的終點位于線段AB延長線的(填:上方、下方或線上)。發(fā)布:2025/1/9 8:0:2組卷:8引用:1難度:0.3


