 現有2.8g Fe全部溶于一定濃度200mL的HNO3溶液中,得到標準狀況下的氣體1.12L,測得反應后溶液的pH為1(反應前后溶液體積變化忽略不計)。請回答下列問題:
現有2.8g Fe全部溶于一定濃度200mL的HNO3溶液中,得到標準狀況下的氣體1.12L,測得反應后溶液的pH為1(反應前后溶液體積變化忽略不計)。請回答下列問題:
(1)反應后溶液中鐵元素的存在形式是Fe3+Fe3+;
(2)反應后溶液中c(NO3-)=0.850.85mol/L;
(3)反應后的溶液最多還能溶解Fe的質量是1.821.82g;
(4)1.12L氣體的成分是NONO;
(5)向含4mol HNO3的稀溶液中,逐漸加入Fe粉至過量,假設生成的氣體只有NO,請在坐標系中畫出n(Fe2+)隨n(Fe)變化的示意圖,并標出n(Fe2+)的最大值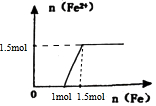
 。
。


【考點】化學方程式的有關計算.
【答案】Fe3+;0.85;1.82;NO;

【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:39引用:2難度:0.5
相似題
-
1.鋼鐵是最重要、用量最大的金屬材料之一.完成下列計算:
(1)生產1噸含鐵96%的生鐵,至少需要氧化鐵含量70%的赤鐵礦(雜質不含鐵)噸.(計算結果保留2位小數)
(2)工業煉鐵用一氧化碳還原氧化鐵時會發生如下一系列反應:
3Fe2O3+CO→2Fe3O4+CO2 Fe3O4+CO→3FeO+CO2 FeO+CO→Fe+CO2
某次實驗中,用CO還原4.80g氧化鐵,當固體質量變成4.56g時,測得此固體中只存在2種氧化物.通過計算確定此固體可能的成分和它們的物質的量之比.
(3)為了測定某碳素鋼(假設只含鐵和碳)的含碳量,將10.000g鋼樣完全溶解于過量的熱濃硝酸中,產生了0.300mol氣體(假設氣體全部逸出,N2O4已折算為NO2).氣體用50.00mL 12.00mol/L的NaOH溶液完全吸收后,只生成兩種鹽,溶液蒸干后得到不含結晶水的固體32.664g.計算:
(1)鋼樣的含碳量.
(2)參加反應的硝酸的物質的量.發布:2025/1/9 8:0:2組卷:75引用:1難度:0.1 -
2.乙醇、乙二醇(HOCH2CH2OH)、甘油(丙三醇HOCH2CHOHCH2OH)分別與足量金屬鈉作用,產生等量的氫氣,則三種醇的物質的量之比為( )
A.6:3:2 B.1:2:3 C.3:2:1 D.4:3:2 發布:2024/12/30 19:0:1組卷:85引用:2難度:0.7 -
3.清潔能源,即綠色能源,它包括核能和“可再生能源”。其中可再生能源包括:水力發電、風力發電、太陽能、生物能(沼氣)、地熱能、海潮能等這些能源。生物能(沼氣)的主要成分是甲烷(CH4),現有甲烷的質量為3.2g,請計算(寫出簡要計算過程):
(1)該甲烷在標準狀況下的體積為多少L?
(2)使該甲烷充分燃燒,需要O2的物質的量是多少?發布:2025/1/25 8:0:2組卷:7引用:1難度:0.7


