 金屬及其合金在生產(chǎn)生活中有廣泛的用途。請運(yùn)用所學(xué)知識回答下列問題:
金屬及其合金在生產(chǎn)生活中有廣泛的用途。請運(yùn)用所學(xué)知識回答下列問題:
(1)下列金屬的用途利用了金屬導(dǎo)電性的是 AA。
A.銅制電線B.鐵制鐵鍋C.金制項鏈D.鋁制飲料罐
(2)請寫出一個能驗證鐵比銅活潑的化學(xué)方程式 Fe+CuSO4=Cu+FeSO4Fe+CuSO4=Cu+FeSO4。
(3)鋁的化學(xué)性質(zhì)活潑,為什么鋁制品卻有很好的抗腐蝕性能 鋁在空氣中與氧氣反應(yīng),其表面生成一層致密的氧化鋁薄膜,從而阻止鋁進(jìn)一步被氧化鋁在空氣中與氧氣反應(yīng),其表面生成一層致密的氧化鋁薄膜,從而阻止鋁進(jìn)一步被氧化?
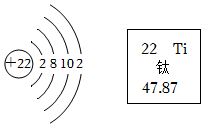
(4)“奮斗者”號在馬里亞納海溝成功坐底,其載人艙球殼采用了中國科學(xué)院自主發(fā)明的Ti-62A鈦合金新材料。下列說法不正確的是 CC。
A.鈦原子核內(nèi)質(zhì)子數(shù)為22 B.鈦元素位于第四周期
C.鈦原子的質(zhì)量是47.87g D.鈦原子核外有22個電子
(5)將鋅粉加入到一定質(zhì)量Cu(NO3)2和AgNO3的混合溶液中,充分反應(yīng)后過濾,可以得到溶液和固體。
①寫出會導(dǎo)致溶液質(zhì)量變小的有關(guān)反應(yīng)的化學(xué)方程式 Zn+2AgNO3=Zn(NO3)2+2AgZn+2AgNO3=Zn(NO3)2+2Ag。
②溶液中發(fā)生反應(yīng)的基本類型為 置換反應(yīng)置換反應(yīng)。
③若所得溶液中只含有一種溶質(zhì),請分析所得固體的成分 一定有銅和銀,可能含有鋅一定有銅和銀,可能含有鋅。
(6)某工廠利用廢鐵屑與廢硫酸起反應(yīng)來制取硫酸亞鐵。現(xiàn)有廢硫酸10t(H2SO4的質(zhì)量分?jǐn)?shù)為9.8%),與足量廢鐵屑起反應(yīng),可生產(chǎn)硫酸亞鐵的質(zhì)量是多少?
【考點】根據(jù)化學(xué)反應(yīng)方程式的計算;金屬的物理性質(zhì)及用途;金屬與氧氣的反應(yīng);原子結(jié)構(gòu)示意圖;元素周期表的特點及其應(yīng)用.
【答案】A;Fe+CuSO4=Cu+FeSO4;鋁在空氣中與氧氣反應(yīng),其表面生成一層致密的氧化鋁薄膜,從而阻止鋁進(jìn)一步被氧化;C;Zn+2AgNO3=Zn(NO3)2+2Ag;置換反應(yīng);一定有銅和銀,可能含有鋅
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:18引用:3難度:0.6
相似題
-
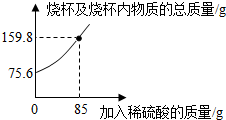 1.為測定某碳素鋼樣品中鐵的質(zhì)量分?jǐn)?shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為52.2g的燒杯中,然后緩慢加入一定質(zhì)量的稀硫酸,當(dāng)加稀硫酸質(zhì)量為85g時,反應(yīng)恰好完全(雜質(zhì)不反應(yīng)且產(chǎn)生的氣體全部逸出),反應(yīng)過程中的質(zhì)量關(guān)系如圖.完成下列問題:
1.為測定某碳素鋼樣品中鐵的質(zhì)量分?jǐn)?shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為52.2g的燒杯中,然后緩慢加入一定質(zhì)量的稀硫酸,當(dāng)加稀硫酸質(zhì)量為85g時,反應(yīng)恰好完全(雜質(zhì)不反應(yīng)且產(chǎn)生的氣體全部逸出),反應(yīng)過程中的質(zhì)量關(guān)系如圖.完成下列問題:
(1)該實驗取用的樣品質(zhì)量為g.
(2)計算樣品中鐵的質(zhì)量分?jǐn)?shù)(寫出解題過程).發(fā)布:2025/1/9 8:0:2組卷:139引用:39難度:0.1 -
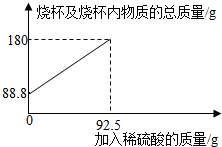 2.為測定某碳素鋼樣品中鐵的質(zhì)量分?jǐn)?shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為51.8克的燒杯中,然后逐步加入一定質(zhì)量分?jǐn)?shù)的稀硫酸,當(dāng)加入92.5g稀硫酸時恰好完全反應(yīng),加入稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關(guān)系如圖。
2.為測定某碳素鋼樣品中鐵的質(zhì)量分?jǐn)?shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為51.8克的燒杯中,然后逐步加入一定質(zhì)量分?jǐn)?shù)的稀硫酸,當(dāng)加入92.5g稀硫酸時恰好完全反應(yīng),加入稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關(guān)系如圖。
(1)該實驗取用的樣品質(zhì)量為g。
(2)反應(yīng)后所得溶液中的溶質(zhì)的質(zhì)量分?jǐn)?shù)。(寫出計算過程,結(jié)果保留一位小數(shù))
(3)反應(yīng)結(jié)束后,小明不慎向燒杯中多加了10g稀硫酸,若在圖中補(bǔ)繪此過程中稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關(guān)系圖,所得線段的終點位于線段AB延長線的(填:上方、下方或線上)。發(fā)布:2025/1/9 8:0:2組卷:4引用:1難度:0.3 -
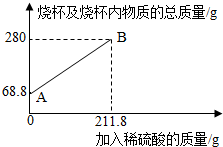 3.為測定某碳素鋼樣品中鐵的質(zhì)量分?jǐn)?shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為51.8克的燒杯中,然后逐步加入一定質(zhì)量分?jǐn)?shù)的稀硫酸,當(dāng)加入211.8g稀硫酸時恰好完全反應(yīng),加入稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關(guān)系如圖。
3.為測定某碳素鋼樣品中鐵的質(zhì)量分?jǐn)?shù),現(xiàn)取一定質(zhì)量的樣品粉末于質(zhì)量為51.8克的燒杯中,然后逐步加入一定質(zhì)量分?jǐn)?shù)的稀硫酸,當(dāng)加入211.8g稀硫酸時恰好完全反應(yīng),加入稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關(guān)系如圖。
(1)該實驗取用的樣品質(zhì)量為g。
(2)求樣品中鐵的質(zhì)量分?jǐn)?shù);反應(yīng)后所得溶液中的溶質(zhì)的質(zhì)量分?jǐn)?shù)。(寫出計算過程,結(jié)果保留一位小數(shù))
(3)反應(yīng)結(jié)束后,小明不慎向燒杯中多加了20g稀硫酸,若在圖中補(bǔ)繪此過程中稀硫酸的質(zhì)量與燒杯及燒杯內(nèi)物質(zhì)的總質(zhì)量的關(guān)系圖,所得線段的終點位于線段AB延長線的(填:上方、下方或線上)。發(fā)布:2025/1/9 8:0:2組卷:8引用:1難度:0.3


