銅是人類廣泛使用的第一種金屬,含銅物質(zhì)在生產(chǎn)生活中有著廣泛應(yīng)用。
回答下列問(wèn)題:
(1)銅錳氧化物(CuMn2O4能在常溫下催化氧化一氧化碳和甲醛(HCHO)。
①基態(tài)Cu原子的M層電子排布式為 3s23p63d103s23p63d10。
②CO和N2互為等電子體。標(biāo)準(zhǔn)狀況下VL CO分子中π鍵數(shù)目為 VNA11.2VNA11.2。
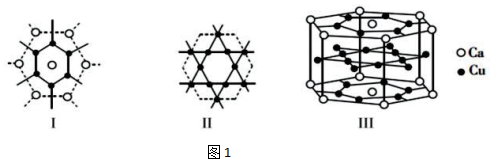
(2)鈣銅合金可用作電解法制備金屬鈣的陰極電極材料。鈣在元素周期表中位于 ss(填“s”、“p”、“d”或“ds“)區(qū)。一種鈣銅合金的結(jié)構(gòu)如圖1所示(Ⅲ可看作是由Ⅰ、Ⅱ兩種原子層交替堆積排列而形成的)。該鈣銅合金中銅原子與鈣原子的個(gè)數(shù)比為 5:15:1。
(3)已知硫酸銅稀溶液呈藍(lán)色,判斷硫酸銅稀溶液中不存在的作用力有 BCBC(填英文字母)。
A.配位鍵
B.金屬鍵
C.離子鍵
D.氫鍵
E.范德華力
(4)已知Cu2O的熔點(diǎn)為1235°C,Cu2S 的熔點(diǎn)為1130°C,Cu2O熔點(diǎn)較高的原因是 兩者都是離子晶體,且陰陽(yáng)離子電荷數(shù)都相同,但離子半徑:r(O2-)<r(S2-),所以Cu2O的晶格能大,熔點(diǎn)較高兩者都是離子晶體,且陰陽(yáng)離子電荷數(shù)都相同,但離子半徑:r(O2-)<r(S2-),所以Cu2O的晶格能大,熔點(diǎn)較高。
(5)Cu2+可形成[Cu(X)2]2+,其中X代表CH3-HN-CH2-CH2-NH2。則1mol[Cu(X)2]2+微粒中VSEPR模型為四面體的非金屬原子共有 1010mol。
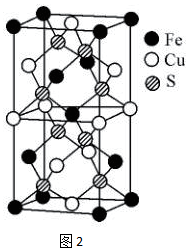
(6)一種含有Fe、Cu、S三種元素的礦物的晶胞(如圖2所示),屬于四方晶系( 晶胞底面為正方形),則該化合物的化學(xué)式為 FeCuS2FeCuS2;若晶胞的底面邊長(zhǎng)為a nm,晶體的密度為pg?cm-3,阿伏加德羅常數(shù)為NA,則該晶胞的高為 736a2ρNA×10-21736a2ρNA×10-21nm。
V
N
A
11
.
2
V
N
A
11
.
2
736
a
2
ρ
N
A
×
1
0
-
21
736
a
2
ρ
N
A
×
1
0
-
21
【答案】3s23p63d10;;s;5:1;BC;兩者都是離子晶體,且陰陽(yáng)離子電荷數(shù)都相同,但離子半徑:r(O2-)<r(S2-),所以Cu2O的晶格能大,熔點(diǎn)較高;10;FeCuS2;
V
N
A
11
.
2
736
a
2
ρ
N
A
×
1
0
-
21
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書(shū)面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:13引用:1難度:0.5
相似題
-
 1.A、B、C、D、E、F是元素周期表中前四周期元素,且原子序數(shù)依次增大,其相關(guān)信息如下:
1.A、B、C、D、E、F是元素周期表中前四周期元素,且原子序數(shù)依次增大,其相關(guān)信息如下:
①A的周期序數(shù)等于其主族序數(shù);
②B、D原子的L層中都有兩個(gè)未成對(duì)電子;
③E元素原子最外層電子排布式為(n+1)Sn(n+1)Pn-1;
④F原子有四個(gè)能層,K、L、M全充滿,最外層只有一個(gè)電子.
試回答下列問(wèn)題:
(1)基態(tài)E原子中,電子占據(jù)的最高能層符號(hào)為,F(xiàn)的價(jià)層電子排布式為.
(2)B、C、D的電負(fù)性由大到小的順序?yàn)?!--BA-->(用元素符號(hào)填寫(xiě)),C與A形成的分子CA3的VSEPR模型為.
(3)B和D分別與A形成的化合物的穩(wěn)定性:BA4小于A2D,原因是.
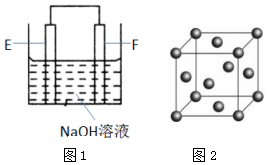
(4)以E、F的單質(zhì)為電極,組成如圖1所示的裝置,E極的電極反應(yīng)式為.
(5)向盛有F的硫酸鹽FSO4的試管里逐滴加入氨水,首先出現(xiàn)藍(lán)色沉淀,繼續(xù)滴加氨水,藍(lán)色沉淀溶解,得到深藍(lán)色溶液,再向深藍(lán)色透明溶液中加入乙醇,析出深藍(lán)色晶體.藍(lán)色沉淀溶解的離子方程式為.
(6)F的晶胞結(jié)構(gòu)(面心立方)如圖2所示:已知兩個(gè)最近的F的距離為acm,F的密度為g/cm3(阿伏加德羅常數(shù)用NA表示,F(xiàn)的相對(duì)原子質(zhì)量用M表示)發(fā)布:2025/1/18 8:0:1組卷:14引用:2難度:0.5 -
 2.鐵及其化合物在生產(chǎn)生活及科學(xué)研究方面應(yīng)用非常廣泛。
2.鐵及其化合物在生產(chǎn)生活及科學(xué)研究方面應(yīng)用非常廣泛。
(1)基態(tài)Fe原子的價(jià)層電子的電子排布圖為;其最外層電子的電子云形狀為。
(2)(NH4)2Fe(SO4)2?6H2O俗稱摩爾鹽
①NH4+電子式為。
②N、O兩元素的第一電離能由大到小的順序?yàn)?!--BA-->(用元素符號(hào)表示)
③SO42-中S原子的雜化方式為,VSEPR模型名稱為。
(3)K3[Fe(CN)6]晶體中中心原子的配位數(shù)為;晶體的配位體為(用化學(xué)符號(hào)表示)
(4)FeS2晶體的晶胞如圖(c)所示。晶胞邊長(zhǎng)為a nm、FeS2相對(duì)式量為M,阿伏加德羅常數(shù)的值為NA,其晶體密度的計(jì)算表達(dá)式為g?cm-3發(fā)布:2025/1/5 8:0:1組卷:7引用:1難度:0.7 -
 3.碳及其化合物有著重要用途。回答下列問(wèn)題:
3.碳及其化合物有著重要用途。回答下列問(wèn)題:
(1)基態(tài)碳原子的價(jià)層電子排布圖為。
(2)在CH2=CHCN中,碳原子的雜化方式有、,所含σ鍵數(shù)目和π鍵數(shù)目之比為。
(3)甲烷、水、氨氣中C、O、N原子均采用sp3雜化方式,VSEPR模型均為正四面體構(gòu)型,比較三者鍵角的大小(由大到小,用H一R-H表示),其原因是。
(4)C60室溫下為紫紅色固體,不溶于水,能溶于四氯化碳等非極性溶劑。據(jù)此判斷C60的晶體類型是。
(5)C60晶胞結(jié)構(gòu)如圖,C60分子處于頂點(diǎn)和面心。已知:C60晶胞棱長(zhǎng)為14.20? (1?=10-8cm),則C60的晶體密度為g/cm3。
C60體中存在正四面體空隙(例如1、3、6、7四點(diǎn)構(gòu)成)和正八面體空隙(例如3、6、7、8、9、12六點(diǎn)構(gòu)成),則平均每一個(gè)C60晶胞中有個(gè)正四面體空隙和4個(gè)正八面體空隙。當(dāng)堿金屬元素全部占滿所有空隙后,這類C60摻雜物才具有超導(dǎo)性。若用金屬銫(Cs)填滿所有空隙,距離最近的兩個(gè)Cs原子間的距離為?。發(fā)布:2025/1/5 8:0:1組卷:53引用:2難度:0.4
相關(guān)試卷


