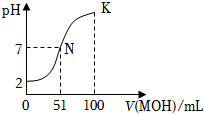
 常溫下,向100mL0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,圖中所示曲線表示混合溶液的pH變化情況(體積變化忽略不計(jì))。回答下列問題:
常溫下,向100mL0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,圖中所示曲線表示混合溶液的pH變化情況(體積變化忽略不計(jì))。回答下列問題:
(1)由圖中信息可知HA為 強(qiáng)強(qiáng)(填“強(qiáng)”或“弱”)酸,MOH為 弱弱(填“強(qiáng)”或“弱”)堿。
(2)①常溫下一定濃度的鹽MA稀溶液的pH=a,則a <<(填“>”“<”或“=”)7,用離子方程式表示其原因:M++H2O?MOH+H+M++H2O?MOH+H+。
②此時(shí),溶液中由水電離出的c(OH-) >>(填“>”“<”或“=”)1×10-7mol?L-1,用含a的式子表示由水電離出的c(OH-)=10-a10-amol?L-1。
(3)滴加51mLMOH溶液時(shí),N點(diǎn)所對應(yīng)的溶液c(M+) ==(填“>”“<”或“=”)c(A-),此時(shí),c(M+)=11511151mol?L-1(用分?jǐn)?shù)表示)。
(4)關(guān)于K點(diǎn)所對應(yīng)的溶液中的關(guān)系可能正確的是 ACAC(填選項(xiàng)字母)。
A.c(M+)>c(A-)>c(OH-)>c(H+)
B.c(M+)<c(MOH)
C.c(M+)+c(MOH)=2c(A-)
D.2c(M+)+c(H+)=2c(A-)+c(OH-)
1
151
1
151
【考點(diǎn)】酸堿混合時(shí)的定性判斷及有關(guān)pH的計(jì)算.
【答案】強(qiáng);弱;<;M++H2O?MOH+H+;>;10-a;=;;AC
1
151
【解答】
【點(diǎn)評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:75引用:3難度:0.5
相似題
-
1.常溫下,在體積均為20mL、濃度均為0.1mol/L的HX溶液、HY溶液中分別滴加0.1mol/L的NaOH溶液,反應(yīng)后溶液中水電離的c(H+)的負(fù)對數(shù)[-lgc(H+)水]與滴加氫氧化鈉溶液體積的關(guān)系如圖所示。下列推斷正確的是( )
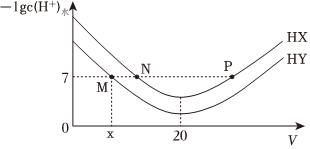
A.HX、HY均為弱酸且HX>HY B.P點(diǎn)溶液中c(Na+ )=c(X-)>c(H+)=c(OH-) C.常溫下用蒸餾水分別稀釋N、P點(diǎn)溶液,溶液pH都變小 D.常溫下,HY的電離常數(shù)Ka= x(20-x)×10-7發(fā)布:2024/12/15 2:30:7組卷:71引用:4難度:0.6 -
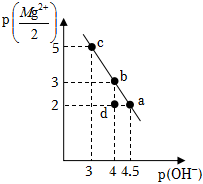 2.25℃時(shí),向10mL0.05mol?L-1的MgCl2溶液中通入氨氣,測得溶液中的p(OH-)與p()之間的變化曲線如圖所示[已知:Kb(NH3?H2O)=1.0×10-5,p(X)=-lgc(X),忽略反應(yīng)過程中溶液體積的變化]。下列說法正確的是( )Mg2+2
2.25℃時(shí),向10mL0.05mol?L-1的MgCl2溶液中通入氨氣,測得溶液中的p(OH-)與p()之間的變化曲線如圖所示[已知:Kb(NH3?H2O)=1.0×10-5,p(X)=-lgc(X),忽略反應(yīng)過程中溶液體積的變化]。下列說法正確的是( )Mg2+2A.a(chǎn)點(diǎn)溶液滿足:2c(Mg2+)+c( )<c(Cl-)NH+4B.b點(diǎn)溶液滿足:c( )>c(Cl-)>c(Mg2+)>c(OH-)NH+4C.c點(diǎn)溶液中通入NH3的量在標(biāo)準(zhǔn)狀況下的體積為22.4mL D.d點(diǎn)溶液中無Mg(OH)2沉淀產(chǎn)生 發(fā)布:2024/12/30 4:0:1組卷:23引用:2難度:0.5 -
3.下列說法正確的是( )
A.食鹽溶液中除去SO42- 最合適的試劑是Ba(NO3)2 B.NaCl溶液和CH3COONH4溶液均顯中性,兩溶液中水的電離程度相同 C.25℃時(shí),用醋酸溶液中和等濃度NaOH溶液至pH=7,VCH3COOH<VNaOH D.AgCl易轉(zhuǎn)化為AgI沉淀且Ksp(AgX)=[Ag+]?[X-],故Ksp(AgI)<Ksp(AgCl) 發(fā)布:2025/1/1 8:0:2組卷:0引用:1難度:0.7
相關(guān)試卷


