(一)氨氣(NH3)的合成是人類科學技術上的重大突破。合成氨工藝的主要流程如圖1:
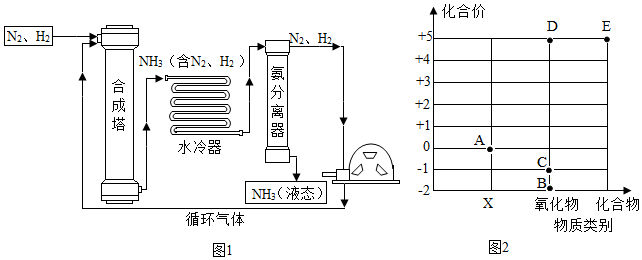
(1)合成塔中的反應必須在高溫、高壓并使用催化劑的條件下進行。該反應的化學方程式為 N2+3H2 催化劑 高溫高壓2NH3N2+3H2 催化劑 高溫高壓2NH3,該反應所屬的基本反應類型是 化合反應化合反應。
(2)從合成塔排出的氣體屬于 混合物混合物(填“純凈物”或“混合物”)。
(3)在生產NH3的過程中,化合價發生改變的元素有 N、HN、H。
(二)從化合價和物質類別兩個維度認識元素及其化合物性質是重要的化學學習方式。A-E物質是氧氣、五氧化二磷、氯酸鉀、水、過氧化氫5種物質中的一種。部分元素的化合價與物質類別二維圖如圖2所示。
①X表示的物質類別為 單質單質(填“單質”或“化合物”);
②C點表示的物質化學式為 H2O2H2O2;
③寫出E點物質的陰離子符號 ClO3-ClO3-;
④E在實驗室中轉化為A的化學方程式為 2KClO3MnO2△2KCl+3O2↑2KClO3MnO2△2KCl+3O2↑。
催化劑
高溫高壓
催化劑
高溫高壓
M
n
O
2
△
M
n
O
2
△
【答案】N2+3H2 2NH3;化合反應;混合物;N、H;單質;H2O2;ClO3-;2KClO32KCl+3O2↑
催化劑
高溫高壓
M
n
O
2
△
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:16引用:1難度:0.4
相似題
-
1.新冠肺炎疫情防控期間,西安市各學校開展全域噴灑低濃度、有效成分是次氯酸鈉的“84”消毒液進行消毒。如圖所示是模擬制備“84”消毒液的流程(Cl2是一種黃綠色的有毒氣體)。請回答下列問題:
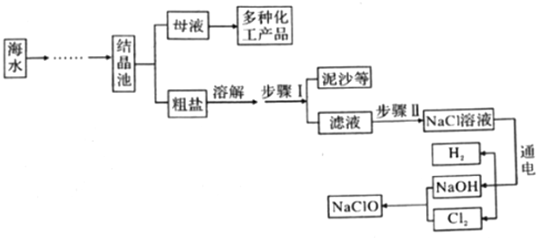
(1)NaOH的俗稱為(寫一種)。
(2)步驟Ⅱ中,通常用碳酸鈉溶液除去濾液中的氯化鈣雜質,請寫出有關反應的化學方程式。
(3)電解水時,一般在水中加入少量NaOH以增強水的導電性,不能加入NaCl的原因是。發布:2025/1/3 8:0:1組卷:6引用:1難度:0.5 -
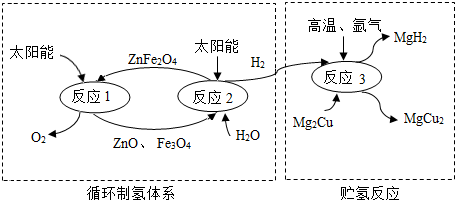 2.如圖是制取與貯存氫氣的一種方法,Mg2Cu是一種貯氫合金,吸氫后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列說法不正確的是( )
2.如圖是制取與貯存氫氣的一種方法,Mg2Cu是一種貯氫合金,吸氫后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列說法不正確的是( )A.ZnFe2O4中Fe的化合價為+3價 B.循環制氫反應中無需加入ZnFe2O4 C.反應1和反應2的總方程式為:2H2O 2H2↑+O2↑通電D.M與足量稀鹽酸反應生成的H2質量大于反應2產生的H2質量 發布:2024/12/31 8:0:1組卷:48引用:2難度:0.5 -
3.某種家用的消毒液的主要成分是次氯酸鈉(NaClO),制取NaClO的化學方程式為:Cl2+2NaOH=NaClO+NaCl+H2O,下列說法錯誤的是( )
A.NaClO中氯元素的化合價為-1 B.反應中用到的NaOH俗稱燒堿 C.該化學方程式中涉及到兩種鹽 D.反應前后氯元素化合價既升高又降低 發布:2025/1/3 8:0:1組卷:71引用:1難度:0.7


