為驗證Cl2、Fe3+、I2三者氧化性的相對強弱,某小組用下圖所示裝置進行實驗(夾持儀器已略去,氣密性已檢驗)。

實驗過程:
Ⅰ.打開彈簧夾,打開活塞a,滴加濃鹽酸。
Ⅱ.當B和C 中的溶液都變為黃色時,夾緊彈簧夾。
Ⅲ.向B中加入一定量KSCN溶液,混合液顯紅色,一段時間后,B 中溶液紅色加深,關閉活塞a。
Ⅳ……
(1)A中產生黃綠色氣體,寫出A中發生反應的離子方程式2H++Cl-+ClO-=Cl2↑+H2O2H++Cl-+ClO-=Cl2↑+H2O。
(2)驗證氯氣的氧化性強于碘單質的實驗現象是濕潤的淀粉KI試紙變藍濕潤的淀粉KI試紙變藍。
(3)B中溶液發生的離子方程式Cl2+2Fe2+-=2Fe3++2Cl-Cl2+2Fe2+-=2Fe3++2Cl-。
(4)為驗證Fe3+的氧化性強于碘單質,過程Ⅳ的操作和現象是打開活塞b,將C中溶液滴入D中,關閉活塞b,取下D振蕩。靜置后CCl4層溶液變為紫色打開活塞b,將C中溶液滴入D中,關閉活塞b,取下D振蕩。靜置后CCl4層溶液變為紫色,對應反應的離子方程式是2I-+2Fe3+-=2Fe3++I2 2I-+2Fe3+-=2Fe3++I2 。
(5)浸有氫氧化鈉溶液的棉花作用是吸收尾氣,防止氯氣污染空氣吸收尾氣,防止氯氣污染空氣。
(6)過程Ⅲ實驗的目的是確認C的黃色溶液中無Cl2,排除Cl2對Fe3+氧化碘離子實驗的干擾確認C的黃色溶液中無Cl2,排除Cl2對Fe3+氧化碘離子實驗的干擾。
【考點】氧化性、還原性強弱的比較.
【答案】2H++Cl-+ClO-=Cl2↑+H2O;濕潤的淀粉KI試紙變藍;Cl2+2Fe2+-=2Fe3++2Cl-;打開活塞b,將C中溶液滴入D中,關閉活塞b,取下D振蕩。靜置后CCl4層溶液變為紫色;2I-+2Fe3+-=2Fe3++I2 ;吸收尾氣,防止氯氣污染空氣;確認C的黃色溶液中無Cl2,排除Cl2對Fe3+氧化碘離子實驗的干擾
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:211引用:4難度:0.5
相似題
-
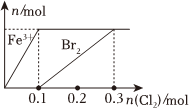 1.向200mLFeBr2溶液中逐漸通入Cl2,其中n(Fe3+)、n(Br2 )隨通入n(Cl2)的變化如圖所示,下列說法錯誤的是( )
1.向200mLFeBr2溶液中逐漸通入Cl2,其中n(Fe3+)、n(Br2 )隨通入n(Cl2)的變化如圖所示,下列說法錯誤的是( )A.還原性強弱:Fe2+>Br- B.由圖可知,該FeBr2溶液的濃度為1mol?L-1 C.n(Cl2)=0.12mol時,溶液中的離子濃度有 ═c(Fe3+)c(Br-)59D.氯氣過量時,反應的離子方程式為:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- 發布:2024/12/7 9:30:1組卷:50引用:3難度:0.5 -
2.根據反應式:①2Fe3++2I-═2Fe2++I2,②Br2+2Fe2+═2Br-+2Fe3+,可判斷離子的還原性從強到弱的順序是( )
A.Br-、Fe2+、I- B.I-、Fe2+、Br- C.Br-、I-、Fe2+ D.Fe2+、I-、Br- 發布:2024/11/28 12:30:2組卷:346引用:8難度:0.8 -
3.已知:
①2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O;
②Cl2+2FeCl2═2FeCl3;
③2KI+2FeCl3═2KCl+I2+2FeCl2。
則下列判斷正確的是( )A.氧化性:MnO4->Fe3+>Cl2>I2 B.還原性:Cl->I->Fe2+ C.Fe3+只有氧化性,Fe2+只有還原性 D.由信息推測:Cl2+2I-═2Cl-+I2反應可以進行 發布:2024/12/11 14:0:2組卷:421引用:7難度:0.4


