已知濃硫酸和木炭粉在加熱條件下可發生化學反應.
(1)上述反應的化學方程式為2H2SO4(濃)+C △ 2H2O↑+CO2↑+2SO2↑2H2SO4(濃)+C △ 2H2O↑+CO2↑+2SO2↑.
(2)試用如圖所列各裝置設計一個實驗,來驗證上述反應所產生的各種產物.
△
△
| 編號 | ||||
| 裝置 | 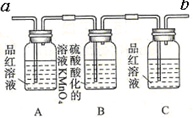 | 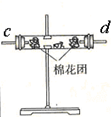 | 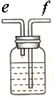 | 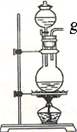 |
g
g
接c(或d)
c(或d)
,d(或c)
d(或c)
接a
a
,b
b
接f
f
.(3)實驗時可觀察到裝置①中A瓶中的溶液褪色,C瓶中的溶液不褪色.A瓶中的溶液的作用是
檢驗SO2氣體;
檢驗SO2氣體;
;B瓶中的溶液的作用是吸收SO2氣體
吸收SO2氣體
;C瓶中的溶液的作用是檢驗SO2氣體是否除干凈
檢驗SO2氣體是否除干凈
.(4)裝置②中所加固體藥品是無水硫酸銅.可驗證的產物是
H2O
H2O
.(5)裝置③中所盛溶液是澄清石灰水,可驗證的產物
CO2
CO2
.【考點】濃硫酸的性質實驗.
【答案】2H2SO4(濃)+C 2H2O↑+CO2↑+2SO2↑;g;c(或d);d(或c);a;b;f;檢驗SO2氣體;;吸收SO2氣體;檢驗SO2氣體是否除干凈;H2O;CO2
△
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:345引用:5難度:0.5
相似題
-
1.下列依據實驗方案和現象對濃硫酸性質做出的判斷合理的是( )
實驗方案 實驗I: 
實驗Ⅱ: 
實驗現象 試紙中心區域變黑,邊緣變紅 黑色固體溶解,溶液接近無色(溶液中錳元素僅以Mn2+存在),產生能使帶火星的木條復燃的無色氣體 A.由Ⅰ可知,濃硫酸具有脫水性 B.由Ⅰ可知,濃硫酸具有弱酸性 C.由Ⅱ可知,濃硫酸具有強氧化性 D.由Ⅱ可知,濃硫酸具有吸水性 發布:2024/12/30 11:30:1組卷:167引用:6難度:0.5 -
 2.實驗室為探究鐵與足量濃硫酸的反應,并驗證SO2的性質,設計如圖所示裝置進行實驗,下列說法錯誤的是( )
2.實驗室為探究鐵與足量濃硫酸的反應,并驗證SO2的性質,設計如圖所示裝置進行實驗,下列說法錯誤的是( )A.實驗結束后,可取A中試管內的溶液稀釋后滴加KSCN溶液檢驗是否有Fe3+ B.B中溶液紫色褪去,C中生成淡黃色沉淀,均體現了SO2的還原性 C.D中品紅溶液褪色,體現了SO2的漂白性 D.E中溶液紅色變淺,體現了SO2酸性氧化物的性質 發布:2024/12/30 14:0:1組卷:115引用:3難度:0.7 -
3.某小組同學探究濃硫酸的性質,向試管①、②中加入等量的98%的濃硫酸,實驗如下。下列對實驗的分析不合理的是( )
實驗1 實驗2 實驗3 裝置 


現象 溶液顏色無明顯變化;把蘸濃氨水的玻璃棒靠近試管口,產生白煙 溶液變黃;把濕潤的品紅試紙靠近試管口,試紙褪色 溶液變深紫色(經檢驗溶液含單質碘) A.實驗1中,白煙是NH4Cl B.根據實驗1和實驗2判斷還原性:Br->Cl- C.根據實驗3判斷還原性:I->Br- D.上述實驗體現了濃H2SO4的強氧化性、難揮發性等性質 發布:2024/12/30 7:30:1組卷:190引用:5難度:0.7


