如圖1也是一些可用來制取二氧化碳氣體的裝置,請你分析:
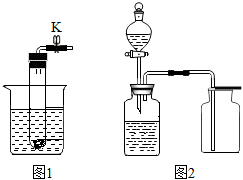
(1)所選用原料組合可以是 大理石或石灰石與稀鹽酸大理石或石灰石與稀鹽酸。
(2)這個裝置的特點是 可以控制反應的發生與停止可以控制反應的發生與停止。
關閉活塞K,出現的現象是 試管中的液面下降,固體逐漸分離,反應停止試管中的液面下降,固體逐漸分離,反應停止。
開啟活塞K,出現的現象是 試管中的液面上升,固體與液體接觸,反應開始試管中的液面上升,固體與液體接觸,反應開始。
(3)按圖2裝置來制取二氧化碳氣體,氣體通入盛有滴有紫色石蕊試液的試劑瓶內,溶液的顏色從 紫紫色變 紅紅色。二氧化碳溶于水生成了 碳酸碳酸,反應的化學方程式為 CO2+H2O=H2CO3CO2+H2O=H2CO3。
(4)取少量試劑瓶內的液體加到小試管內,加熱該溶液,溶液的顏色從 紅紅色,變成 紫紫色。說明碳酸 不穩定不穩定,受熱 易分解易分解。反應的化學方程式為 H2CO3 △ CO2↑+H2OH2CO3 △ CO2↑+H2O。
(5)實驗室用大理石或石灰石來制取二氧化碳氣體,可選用的酸液有:鹽酸、硫酸、醋酸等,其中不宜采用的酸是 硫酸硫酸,原因是 硫酸與碳酸鈣反應生成微溶于水的硫酸鈣,會附著在大理石或石灰石的表面,阻止反應的進一步發生硫酸與碳酸鈣反應生成微溶于水的硫酸鈣,會附著在大理石或石灰石的表面,阻止反應的進一步發生。
△
△
【答案】大理石或石灰石與稀鹽酸;可以控制反應的發生與停止;試管中的液面下降,固體逐漸分離,反應停止;試管中的液面上升,固體與液體接觸,反應開始;紫;紅;碳酸;CO2+H2O=H2CO3;紅;紫;不穩定;易分解;H2CO3 CO2↑+H2O;硫酸;硫酸與碳酸鈣反應生成微溶于水的硫酸鈣,會附著在大理石或石灰石的表面,阻止反應的進一步發生
△
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/7/26 8:0:9組卷:1引用:2難度:0.6
相似題
-
1.實驗室制取氣體所需的裝置如圖所示,請回答以下問題。
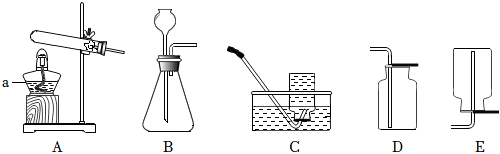
(1)a儀器名稱。收集氧氣可以選用C,原因是。用高錳酸鉀制氧氣,反應的化學方程式為。
(2)實驗室用石灰石和稀鹽酸制取CO2,發生裝置應選用,收集用,CO2的驗滿方法為。發布:2024/12/8 10:30:2組卷:50引用:4難度:0.5 -
2.用圖-1所示裝置制取干燥的CO2,并對CO2的部分性質進行探究。
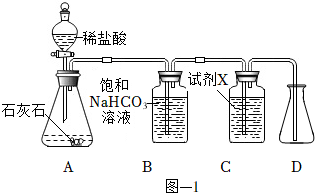
(1)裝置A中發生反應的化學方程式為。
(2)①裝置B中飽和NaHCO3溶液的作用是。
②裝置C中試劑X應該選用(填字母)。
a.稀H2SO4
b.濃H2SO4
c.KOH溶液
(3)收集CO2并驗滿。將集滿CO2的錐形瓶與盛有足量NaOH溶液的注射器和傳感器密封連接,緩慢的將NaOH溶液注入到錐形瓶中,采集信息形成圖像。見圖-2。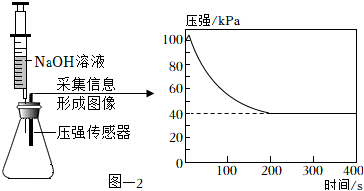
①檢驗裝置D中CO2已經集滿的方法是。
②隨著反應的進行,錐形瓶中壓強降低的原因是。
③反應結束后錐形瓶中的壓強保持在40kPa說明。
(4)取2mL飽和澄清石灰水于試管中,用4mL蒸餾水稀釋,向其中緩慢通入足量CO2。測定反應體系的電導率變化如圖-3所示。(忽略反應前后溶液體積的變化)
【查閱資料】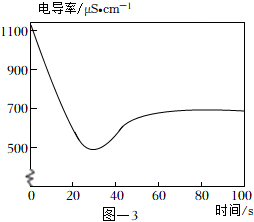
材料一:溶液的導電能力越強,溶液的電導率越大。
材料二:單位體積溶液中某離子的個數越多,則該離子的濃度越大,溶液的導電能力越強。相同濃度的不同離子導電能力不同。
材料三:Ca( OH)2溶于水能完全解離出Ca2+和OH-。
CaCO3遇到溶有CO2的水時,能反應生成易溶于水的Ca( HCO3)2,Ca( HCO3)2在水中能完全解離出Ca2+和。HCO-3
①石灰水中通入CO2氣體,溶液的電導率先逐漸降低的主要原因是。
②反應最終電導率的穩定值低于初始值的可能原因是、。發布:2024/12/25 13:0:1組卷:841引用:3難度:0.6 -
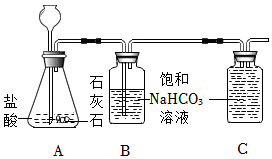 3.實驗室可用如圖裝置制取二氧化碳;已知常溫下CO2灘溶于飽和NaHCO3溶液。
3.實驗室可用如圖裝置制取二氧化碳;已知常溫下CO2灘溶于飽和NaHCO3溶液。
(1)寫出A裝置中發生反應的化學方程式。
(2)B中飽和碳酸氫鈉溶液的作用是什么?
(3)利用排飽和NaHCO3溶液法可以收集較純凈的二氧化碳氣體,請將C裝置中的導管補畫完整。發布:2024/12/25 15:0:2組卷:7引用:2難度:0.6


