取一定量Fe2O3粉末(紅棕色)加入適量某濃度的鹽酸中,得到呈棕黃色的飽和FeCl3溶液,利用此溶液進行以下實驗:
(1)寫出生成此溶液所發生反應的化學方程式為 Fe2O3+6HCl═2FeCl3+3H2OFe2O3+6HCl═2FeCl3+3H2O。
(2)取少量該FeCl3溶液置于試管甲中,滴入NaOH溶液,可以觀察到有紅褐色沉淀生成,反應的化學方程式為 FeCl3+3NaOH═3NaCl+Fe(OH)3↓FeCl3+3NaOH═3NaCl+Fe(OH)3↓,此反應屬于 復分解反應復分解反應(填基本反應類型)。
(3)在小燒杯甲中加入25mL蒸餾水,加熱至沸騰后,向 沸水沸水中加入2mL 飽和氯化鐵溶液飽和氯化鐵溶液,繼續煮沸至溶液呈 紅褐紅褐 色,即可制得Fe(OH)3膠體,反應方程式為 FeCl3+3H2O △ Fe(OH)3(膠體)+3HClFeCl3+3H2O △ Fe(OH)3(膠體)+3HCl。
(4)另取一小燒杯乙加入25mL蒸餾水,然后再加入2mL該FeCl3溶液,振蕩均勻,將乙燒杯與另一盛有Fe(OH)3膠體的丙燒杯一起放置在暗處,分別用紅色激光筆照射燒杯中的液體,可以看到 丙丙(填“乙”或“丙”)燒杯中產生丁達爾效應。用這個實驗可以區別 溶液和膠體溶液和膠體。
(5)取丙燒杯中的少量Fe(OH)3膠體置于試管乙中,向試管乙中滴加一定量的稀硫酸,邊滴加邊振蕩,在此過程中可看到試管乙中生成的紅褐色沉淀逐漸溶解,最終又得到棕黃色的溶液,發生此變化的化學方程式為 2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O。
(6)Fe(OH)3膠體區別于FeCl3溶液最本質的特征是 AA。
A.Fe(OH)3膠體粒子的直徑在1~100nm之間
B.Fe(OH)3膠體具有丁達爾效應
C.Fe(OH)3膠體是均一的分散系
D.Fe(OH)3膠體的分散質能透過濾紙
(7)制得的Fe(OH)3膠體中往往混有H+和Cl-,可以利用 滲析滲析(方法)來提純Fe(OH)3膠體。證明Fe(OH)3膠體和Cl-已分離完全的實驗操作是 取滲析2-3次以后的放置一定時間的滲析液2mL盛在試管中,向試管內加硝酸酸化的硝酸銀溶液,如果溶液里不產生白色沉淀,證明Fe(OH)3膠體與Cl-已完全分離取滲析2-3次以后的放置一定時間的滲析液2mL盛在試管中,向試管內加硝酸酸化的硝酸銀溶液,如果溶液里不產生白色沉淀,證明Fe(OH)3膠體與Cl-已完全分離。
△
△
【答案】Fe2O3+6HCl═2FeCl3+3H2O;FeCl3+3NaOH═3NaCl+Fe(OH)3↓;復分解反應;沸水;飽和氯化鐵溶液;紅褐;FeCl3+3H2O Fe(OH)3(膠體)+3HCl;丙;溶液和膠體;2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O;A;滲析;取滲析2-3次以后的放置一定時間的滲析液2mL盛在試管中,向試管內加硝酸酸化的硝酸銀溶液,如果溶液里不產生白色沉淀,證明Fe(OH)3膠體與Cl-已完全分離
△
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:25引用:1難度:0.7
相似題
-
1.鐵的氧化物有很多,在中學化學中經常提到的有FeO、Fe2O3和Fe3O4,而且在一定條件下它們之間是可以相互轉化的,例如:在1400℃以上的溫度下加熱Fe2O3時,Fe2O3會部分失去氧,生成Fe3O4.下列有關說法正確的是( )
A.FeO、Fe2O3和Fe3O4均為黑色固體 B.Fe3O4常寫成FeO?Fe2O3,其中既有+2價的Fe,又有+3價的Fe,所以Fe3O4是一種混合物 C.熱穩定性Fe2O3>Fe3O4 D.FeO、Fe2O3和Fe3O4均可與鹽酸反應,且反應類型均為復分解反應 發布:2024/12/30 3:30:1組卷:406引用:6難度:0.9 -
2.下列說法正確的是( )
A.NaOH俗稱燒堿 B.Fe2O3是黑色的固體 C.Na2O可用于呼吸面具中氧氣的來源 D.Al(OH)3只能與強酸溶液反應,不能與強堿溶液反應 發布:2025/1/3 8:0:1組卷:17引用:1難度:0.7 -
3.查閱資料:CaO、MgO在高溫下與C難反應,但能與SiO2反應.硫鐵礦燒渣是一種工業廢渣(含Fe2O3及少量SiO2、Al2O3、CaO、MgO等雜質),該燒渣可用于制取氧化鐵,具體化工生產工藝流程如下:
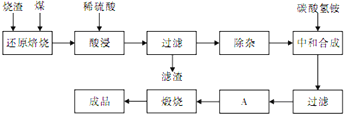
(1)焙燒時產生的主要有害氣體是.
(2)為測定過濾所得濾液中Fe2+的含量,實驗室中常用酸性高錳酸鉀溶液進行滴定,寫出該反應的離子方程式:;實驗中所用酸性高錳酸鉀溶液濃度為0.10mol/L,濾液用滴定管量取20.00ml,用酸性高錳酸鉀溶液滴定到終點時消耗了標準的酸性高錳酸鉀溶液12.04ml,濾液中c(Fe2+)=.
(3)若在空氣中“酸浸”時間過長,溶液中Fe2+含量將下降,其原因是:(用離子方程式表示).
(4)根據下表數據:
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 2.01 7.11 萬全沉淀的pH 4.77 3.68 9.61 ,檢驗Fe3+已經除盡的試劑是(除KSCN外).
(5)“中和合成”的目的是將溶液中Fe2+轉變為碳酸亞鐵沉淀,則A的操作是.發布:2025/1/19 8:0:1組卷:24引用:2難度:0.5


