NOx的排放主要來(lái)自于汽車尾氣,包含NO2和NO。若用活性炭對(duì)NO進(jìn)行吸附,可發(fā)生C(s)+2NO(g)?N2(g)+CO2(g),在T1℃時(shí),借助傳感器測(cè)得反應(yīng)在不同時(shí)間點(diǎn)上各物質(zhì)的濃度如表:
| 濃度(mol?L-1) | 時(shí)間(min) | |||||
| 0 | 10 | 20 | 30 | 40 | 50 | |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
c
c
.a.該反應(yīng)體現(xiàn)了NO的氧化性
b.降低NO濃度能夠減慢反應(yīng)速率
c.加入足量的炭粉可以使NO100%轉(zhuǎn)化
d.合適的催化劑可以加快反應(yīng)速率
(2)上表0~10min內(nèi),NO的平均反應(yīng)速率v(NO)=
0.042mol/(L?min)
0.042mol/(L?min)
;當(dāng)升高反應(yīng)溫度,該反應(yīng)的平衡常數(shù)K減小,說(shuō)明正反應(yīng)為 放熱
放熱
反應(yīng)(填“吸熱”或“放熱”).(3)30min后,只改變某一條件,反應(yīng)重新達(dá)到平衡;根據(jù)上表中的數(shù)據(jù)判斷改變的條件可能是
bc
bc
(填字母).a.加入一定量的活性炭
b.通入一定量的NO
c.適當(dāng)縮小容器的體積
d.加入合適的催化劑
某實(shí)驗(yàn)室模擬該反應(yīng),在恒壓密閉容器中加入足量的活性炭和一定量的NO氣體,測(cè)得NO的轉(zhuǎn)化單隨溫度的變化如圖所示:
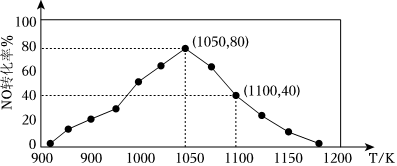
(4)由圖可知,1050K前反應(yīng)中NO的轉(zhuǎn)化率隨溫度升高而增大,原因是
1050K前反應(yīng)未達(dá)到平衡狀態(tài),增大壓強(qiáng),物質(zhì)的濃度增大,反應(yīng)速率加快,NO轉(zhuǎn)化率提高
1050K前反應(yīng)未達(dá)到平衡狀態(tài),增大壓強(qiáng),物質(zhì)的濃度增大,反應(yīng)速率加快,NO轉(zhuǎn)化率提高
;在1100K時(shí),CO2的體積分?jǐn)?shù)為 20%
20%
.(5)NO2排放到大氣中會(huì)引起
酸雨、光化學(xué)煙霧
酸雨、光化學(xué)煙霧
(填兩個(gè))等環(huán)境問(wèn)題.【考點(diǎn)】化學(xué)平衡的影響因素;化學(xué)平衡的計(jì)算.
【答案】c;0.042mol/(L?min);放熱;bc;1050K前反應(yīng)未達(dá)到平衡狀態(tài),增大壓強(qiáng),物質(zhì)的濃度增大,反應(yīng)速率加快,NO轉(zhuǎn)化率提高;20%;酸雨、光化學(xué)煙霧
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書(shū)面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:43引用:2難度:0.5
相似題
-
1.升高溫度,下列數(shù)據(jù)不一定增大的是( )
A.化學(xué)反應(yīng)速率v B.水的離子積常數(shù)Kw C.化學(xué)平衡常數(shù)K D.氨水的電離平衡常數(shù)Ka 發(fā)布:2025/1/6 6:0:5組卷:31引用:4難度:0.7 -
2.催化還原CO2是解決溫室效應(yīng)及能源問(wèn)題的重要手段之一。研究表明,在Cu/ZnO催化劑存在下,CO2和H2可發(fā)生以下兩個(gè)平衡反應(yīng)。下列有關(guān)說(shuō)法不正確的是( )
①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1=-53.7kJ?mol-1
②CO2(g)+H2(g)?CO(g)+H2O(g)△H2=+41.2kJ?mol-1A.反應(yīng)①為放熱反應(yīng),反應(yīng)②為吸熱反應(yīng) B.使用不同催化劑,會(huì)改變反應(yīng)①②的△H C.反應(yīng)CO(g)+2H2(g)?CH3OH(g)的△H3=-94.9kJ?mol-1 D.投料比不變,增加反應(yīng)物的濃度可提高CO2轉(zhuǎn)化為CH3OH平衡轉(zhuǎn)化率 發(fā)布:2025/1/6 6:0:5組卷:90引用:3難度:0.5 -
3.現(xiàn)代工業(yè)將煤汽化,既可以提高燃料的利用率、減少CO、SO2等的排放,又可以擴(kuò)大水煤氣的用途.甲醇是一種可再生能源,具有開(kāi)發(fā)和應(yīng)用的廣闊前景,工業(yè)上一般可采用水煤氣來(lái)合成甲醇CO(g)+2H2(g)?CH3OH(g).
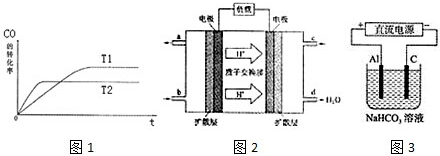
(1)如圖1是該反應(yīng)在不同溫度下CO的轉(zhuǎn)化率隨時(shí)間變化的曲線.
①T1和T2溫度下的平衡常數(shù)大小關(guān)系是K1K2(填“>”、“<”或“=”).
②以下有關(guān)說(shuō)法正確的是
a.恒溫、恒容條件下,容器內(nèi)的壓強(qiáng)不發(fā)生變化則可逆反應(yīng)達(dá)到平衡
b.一定條件下,H2的消耗速率是CO的消耗速率的2倍時(shí)可逆反應(yīng)達(dá)到平衡
c.使用合適的催化劑能縮短達(dá)到平衡的時(shí)間并提高CH3OH的產(chǎn)率
d.某溫度下,將2molCO和6molH2充入2L的密閉容器中,充分反應(yīng),達(dá)到平衡后,測(cè)得c(CO)=0.2mol/L,則CO的轉(zhuǎn)化率為80%
(2)已知在常溫常壓下①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)△H=-akJ?mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-bkJ?mol-1③H2O(g)=H2O(1)△H=-ckJ?mol-1
則:CH3OH(1)+O2(g)=CO(g)+2H2O(1)△H=kJ?mol-1
(3)2009年10月,中國(guó)科學(xué)院長(zhǎng)春應(yīng)用化學(xué)研究所在甲醇燃料電池技術(shù)方面獲得新突破,組裝出了自呼吸電池及主動(dòng)式電堆.甲醇燃料電池的工作原理如圖2所示.
①該電池正極的電極反應(yīng)式為.
②工作一段時(shí)間后,當(dāng)6.4g甲醇完全反應(yīng)生成CO2時(shí),有個(gè)電子發(fā)生轉(zhuǎn)移.
(4)以上述電池做電源,用圖3所示裝置,在實(shí)驗(yàn)室中模擬鋁制品面“鈍化”處理的過(guò)程中,發(fā)現(xiàn)溶液逐漸變渾濁,原因是、(用相關(guān)的電極反應(yīng)式和離子方程式表示)發(fā)布:2024/12/30 14:0:1組卷:26引用:3難度:0.5
相關(guān)試卷


