 過氧化氫(H2O2)俗稱雙氧水。是一種重要的化工產品,具有漂白、氧化、消毒、殺菌等多種功效,廣泛應用于紡織、造紙、化工、電子、輕工、污水處理等工業。回答下列問題:
過氧化氫(H2O2)俗稱雙氧水。是一種重要的化工產品,具有漂白、氧化、消毒、殺菌等多種功效,廣泛應用于紡織、造紙、化工、電子、輕工、污水處理等工業。回答下列問題:
(1)H2O2的電子式為
 。
。
(2)用H2O2與稀硫酸的混合溶液可溶出印刷電路板金屬粉末中的銅。
已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64kJ/mol
2H2O2(1)═2H2O(l)+O2(g)△H=-196kJmol
H2(g)+12O2(g)═H2O(l)△H=-286kJ/mol
則在稀硫酸溶液中Cu與H2O2反應生成Cu2+和H2O的熱化學方程式為:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-320kJ/molCu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-320kJ/mol。
(3)工業上常用電解硫酸氫銨水溶液的方法制備過氧化氫,其原理為:首先2NH4HSO4 通電 (NH4)2S2O8+H2↑,然后由(NH4)2S2O8水解得到H2O2和另一產物。則:
①電解時陽極的電極反應式為2SO42--2e-=S2O82-2SO42--2e-=S2O82-;
②(NH4)2S2O8水解時發生反應的化學方程式為(NH4)2S2O8+2H2O=2NH4HSO4+H2O2(NH4)2S2O8+2H2O=2NH4HSO4+H2O2。
(4)現甲、乙兩個化學小組利用兩套相同裝置,通過測定產生相同體積氣體所用時間長短來探究影響H2O2分解速率的因素(僅一個條件改變)。甲小組有如下實驗設計方案。


1
2
通電
| 實驗編號 | 溫度 | 催化劑 | 濃度 |
| 甲組實驗Ⅰ | 25℃ | 三氧化二鐵 | 10mL 5%H2O2 |
| 甲組實驗Ⅱ | 25℃ | 二氧化錳 | 10mL 5%H2O2 |
①甲小組實驗得出的結論是
H2O2分解時,MnO2比Fe2O3催化效率更高
H2O2分解時,MnO2比Fe2O3催化效率更高
。②由乙組研究的酸、堿對H2O2分解影響因素的數據分析,相同條件下H2O2在
堿
堿
(填“酸”或“堿”)性環境下放出氣體速率較快;由此,乙組提出可以用BaO2固體與硫酸溶液反應制H2O2,其反應的離子方程式為BaO2+2H++SO42-═BaSO4↓+H2O2
BaO2+2H++SO42-═BaSO4↓+H2O2
;支持這一方案的理由是(BaSO4的生成有利于平衡右移即有利于H2O2的生成)酸性環境有利于H2O2的存在(等其他合理原因)
(BaSO4的生成有利于平衡右移即有利于H2O2的生成)酸性環境有利于H2O2的存在(等其他合理原因)
。③已知過氧化氫還是一種極弱的二元酸:H2O2?H++HO2-(K
a
1
1.33×104
1.33×104
(保留3位有效數字)。【答案】 ;Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-320kJ/mol;2SO42--2e-=S2O82-;(NH4)2S2O8+2H2O=2NH4HSO4+H2O2;H2O2分解時,MnO2比Fe2O3催化效率更高;堿;BaO2+2H++SO42-═BaSO4↓+H2O2;(BaSO4的生成有利于平衡右移即有利于H2O2的生成)酸性環境有利于H2O2的存在(等其他合理原因);1.33×104
;Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-320kJ/mol;2SO42--2e-=S2O82-;(NH4)2S2O8+2H2O=2NH4HSO4+H2O2;H2O2分解時,MnO2比Fe2O3催化效率更高;堿;BaO2+2H++SO42-═BaSO4↓+H2O2;(BaSO4的生成有利于平衡右移即有利于H2O2的生成)酸性環境有利于H2O2的存在(等其他合理原因);1.33×104
 ;Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-320kJ/mol;2SO42--2e-=S2O82-;(NH4)2S2O8+2H2O=2NH4HSO4+H2O2;H2O2分解時,MnO2比Fe2O3催化效率更高;堿;BaO2+2H++SO42-═BaSO4↓+H2O2;(BaSO4的生成有利于平衡右移即有利于H2O2的生成)酸性環境有利于H2O2的存在(等其他合理原因);1.33×104
;Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-320kJ/mol;2SO42--2e-=S2O82-;(NH4)2S2O8+2H2O=2NH4HSO4+H2O2;H2O2分解時,MnO2比Fe2O3催化效率更高;堿;BaO2+2H++SO42-═BaSO4↓+H2O2;(BaSO4的生成有利于平衡右移即有利于H2O2的生成)酸性環境有利于H2O2的存在(等其他合理原因);1.33×104【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:57引用:2難度:0.1
相似題
-
1.高錳酸鉀(KMnO4)和雙氧水(H2O2)都是常見的消毒試劑,在日常生活和工業生產中都有廣泛的應用。回答下面問題:
(1)酸性高錳酸鉀與雙氧水混合有氣體產生,經檢驗產生的氣體為氧氣。寫出反應的離子方程式。
(2)H2O2是一種二元弱酸,與NaOH反應的化學方程式為NaOH+H2O═NaHO2+H2O,寫出H2O2電離的方程式(只寫第一步)。在酸性條件下H2O2的分解速度變大,利用平衡移動的原理進行解釋:。
(3)現有H2O2-Al燃料電池電解尿素[CO(NH2)2]制備氫氣的裝置,b、c、d為石墨電極,電解池中的隔膜只阻止氣體通過,如圖:
①a電極是Al,寫出電極反應,反應后b電極區溶液的pH(填“增大”“減小”或“不變”)。
②c電極是(填“正極”“負極”“陰極”或“陽極”),d電極的電極反應為。
(4)某化學興趣小組為了探究KMnO4與H2O2氧化性強弱,設計了如圖實驗裝置:
①當閉合電鍵K時,電流表指針向左偏轉,甲燒杯中溶液顏色逐漸變淺,則石墨電極a上發生反應(填“氧化”或“還原”),石墨電極b上發生的電極反應為。
②反應一段時間后,向甲燒杯中滴加KOH溶液,同時向乙燒杯中滴加硫酸溶液,發現電流表指針逐漸翻轉,最后向右偏轉,說明KMnO4與H2O2氧化性與有關。發布:2024/8/9 8:0:9組卷:13引用:3難度:0.6 -
2.下列說法正確的是( )
A.H2O2具有強氧化性可用于殺菌消毒 B.熱的碳酸鈉溶液去污能力強,所以蒸干碳酸鈉溶液得到NaOH固體 C.在銅的電解精煉過程中,若轉移1 mol電子,則陽極溶解32 g Cu D.油脂在酸性條件下易水解,可用于制作肥皂 發布:2024/12/30 4:30:1組卷:69引用:2難度:0.9 -
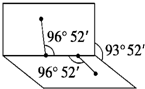 3.已知H2O2的結構如圖:H2O2分子不是直線形的,兩個H原子猶如在半展開的書的兩面紙上,書頁角為93°52′,而兩個O-H鍵與O-O鍵的夾角均為96°52′,試回答:
3.已知H2O2的結構如圖:H2O2分子不是直線形的,兩個H原子猶如在半展開的書的兩面紙上,書頁角為93°52′,而兩個O-H鍵與O-O鍵的夾角均為96°52′,試回答:
(1)寫出H2O2分子的電子式和結構式.
(2)寫出分子內的鍵型.
(3)估計它難溶于CS2,簡要說明原因.
(4)指出氧元素的化合價,簡要說明原因.發布:2024/12/30 8:30:1組卷:43引用:2難度:0.5


