燃煤煙氣中的NOx、SO2可通入堿液或利用電解池裝置進行吸收處理。
Ⅰ.常溫下,O3是一種有特殊臭味、穩定性較差的淡藍色氣體。O3氧化性強于O2,能更有效地氧化NO。
(1)2NO(g)+O2(g)═2NO2(g)△H1=-114kJ×mol-1
NO(g)+O3(g)═NO2(g)+O2(g)△H2=-199.1kJ×mol-1(活化能Ea=3.2kJ?mol-1)
則2O3(g)=3O2(g)△H3=-284.2-284.2kJ?mol-1(活化能Ea=119.2kJ?mol-1)
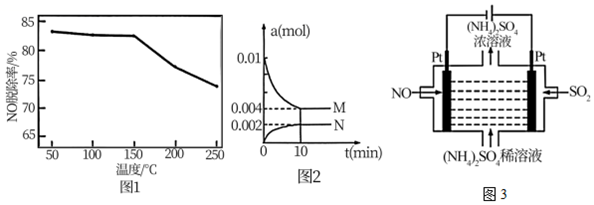
(2)為分析氧化時溫度對NO脫除率的影響,將NO與O3混合反應一段時間,再用堿液吸收氧化后的氣體。其他條件相同時,NO脫除率隨NO與O3混合反應時溫度變化如圖1所示。溫度在50~150℃時,隨著溫度升高,NO脫除率無明顯變化;溫度超過150℃時,隨著溫度升高,NO脫除率下降。其可能原因是50~150℃時,NO和O3反應的活化能低,反應速率快,O3分解的活化能高,反應速率慢,所以O3分解對O3氧化NO反應的影響不大,但溫度高于150℃時,O3分解速率迅速增加50~150℃時,NO和O3反應的活化能低,反應速率快,O3分解的活化能高,反應速率慢,所以O3分解對O3氧化NO反應的影響不大,但溫度高于150℃時,O3分解速率迅速增加。
Ⅱ.一定條件下20mLSO2水溶液中可發生如下反應:3SO2+2H2O?2H2SO4+S↓,部分物質的物質的量的變化如圖2所示。
(3)曲線N表示硫硫的變化(填名稱)。10min時反應達到平衡狀態,用H2SO4表示反應的平均速率為0.02mol/(L?min)0.02mol/(L?min)。
(4)下列不能說明3SO2(aq)+2H2O(l)?2H2SO4(aq)+S(s)反應已達到平衡狀態的是AA。
A.2v(SO2)=3v(H2SO4)
B.絕熱恒容時,反應的化學平衡常數不再變化
C.恒溫恒容時,混合溶液中硫酸的密度不再變化
D.反應過程中,溶液中分子總數不再改變
Ⅲ.若煙氣主要成分為NO、SO2,可通過電解法除去,其原理如圖3所示。陽極的電極反應式為SO2-2e-+2H2O=SO42-+4H+SO2-2e-+2H2O=SO42-+4H+。電解過程中得到的產物為H2SO4、(NH4)2SO4H2SO4、(NH4)2SO4。
【答案】-284.2;50~150℃時,NO和O3反應的活化能低,反應速率快,O3分解的活化能高,反應速率慢,所以O3分解對O3氧化NO反應的影響不大,但溫度高于150℃時,O3分解速率迅速增加;硫;0.02mol/(L?min);A;SO2-2e-+2H2O=SO42-+4H+;H2SO4、(NH4)2SO4
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:33引用:2難度:0.5
相似題
-
 1.第五主族的磷單質及其化合物在工業上有廣泛應用.
1.第五主族的磷單質及其化合物在工業上有廣泛應用.
(1)同磷灰石在高溫下制備黃磷的熱化學方程式為:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)△H已知相同條件下:4Ca5(PO4)3F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g)△H12Ca3(PO4)2(s)+10C(s)=P4(g)+6CaO(s)+10CO(g)△H2SiO2(s)+CaO(s)=CaSiO3(s)△H3用△H1、△H2和△H3表示△H,則△H=;
(2)白磷與氧氣反應生成P4O10固體.已知斷裂下列化學鍵需要吸收的能量分別為:P-P a kJ?mol-1、P-O b kJ?mol-1、P═O c kJ?mol-1、O═O d kJ?mol-1.根據圖1的分子結構和有關數據通過計算寫出該反應的熱化學方程式為.
(3)三聚磷酸可視為三個磷酸分子(磷酸結構式如圖2)之間脫去兩個水分子產物,其結構式為,三聚磷酸鈉(俗稱“五鈉”)是常用的水處理劑,其化學式為.
(4)次磷酸(H3PO2)為一元酸,分子中含一個羥基,其鈉鹽的正鹽的化學式為,該鹽可用于工業上的化學鍍鎳.①化學鍍鎳的溶液中含有Ni2+和H2PO2-,在酸性等條件下發生下述反應:
(a)□Ni2++□H2PO2-+□=□Ni++□H2PO3-+□
(b)6H2PO-2+2H+=2P+4H2PO3-+3H2↑請在答題卡上寫出并配平反應式(a);
②利用①中反應可在塑料鍍件表面沉積鎳-磷合金,從而達到化學鍍鎳的目的,這是一種常見的化學鍍.請從以下方面比較化學鍍與電鍍.原理上的不同點:;化學鍍的優點:.發布:2024/11/19 8:0:1組卷:77引用:2難度:0.1 -
2.氨和聯氨(N2H4)是氮的兩種常見化合物,在科學技術和生產中有重要的應用.聯氨(又稱肼,N2H4或H2N-NH2,無色液體)是一種應用廣泛的化工原料,可用作火箭燃料.回答下列問題:
(1)聯氨分子的電子式為,其中氮的化合價為;
(2)實驗室中可用次氯酸鈉溶液與氨反應制備聯氨,該反應中還原劑與氧化劑的物質的量之比為2:1,反應的化學方程式為.
(3)①2O2(g)+N2(g)═N2O4(g)△H1
②ON2(g)+2H2(g)═N2H4(l)△H2
③O2(g)+2H2(g)═2H2O(g)△H3
④N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H4=-1038.6kJ?mol-1
上述反應熱效應之間的關系式為△H4=,聯氨和N2O4可作為火箭推進劑的主要原因為.
(4)聯氨可用作火箭燃料,燃燒時發生的反應是N2O4(l)+2N2O4(l)═3N2(g)+4H2O(g)△H=-1038.6kJ?mol-1,若該反應中有4molN-H鍵斷裂,則反應放出的熱量為kJ.發布:2024/11/18 8:0:1組卷:12引用:0難度:0.9 -
3.已知在1200℃時,天然氣脫硫工藝中會發生下列反應:
①H2S(g)+O2(g)═SO2(g)+H2O(g) ΔH132
②2H2S(g)+SO2(g)═S2(g)+2H2O(g) ΔH232
③H2S(g)+O2(g)═S(g)+H2O(g) ΔH312
④2S(g)═S2(g) ΔH4
則ΔH4的正確表達式為( )A.ΔH4= (ΔH1+ΔH2-3ΔH3)23B.ΔH4= (3ΔH3-ΔH1-ΔH2)23C.ΔH4= (ΔH1+ΔH2-3ΔH3)32D.ΔH4= (ΔH1-ΔH2-3ΔH3)32發布:2024/12/6 13:30:1組卷:389引用:6難度:0.5
相關試卷


