(化學-化學與技術)
金屬鋁的生產是以Al2O3為原料,在熔融狀態下進行電解:2Al2O3750-970oC通電,Na3AIF64Al+3O2
請回答下列問題:
(1)冰晶石(Na3AIF6)的作用是降低Al2O3的熔化溫度降低Al2O3的熔化溫度.
(2)電解生成的金屬鋁是在熔融液的下層下層(填“上層”或“下層”).
(3)陰極和陽極均由碳棒(或石墨)碳棒(或石墨)材料做成;電解時所消耗的電極是陽極陽極(填“陽極”或“陰極”).
(4)鋁是高耗能產品,廢舊鋁材的回收利用十分重要.在工業上,最能體現節能減排思想的是將回收鋁做成cc(填代號).
a.冰晶石 b.氧化鋁 c.鋁錠 d.硫酸鋁.
750
-
970
o
C
通電
,
N
a
3
AI
F
6
【考點】工業制金屬鋁.
【答案】降低Al2O3的熔化溫度;下層;碳棒(或石墨);陽極;c
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:233引用:3難度:0.3
相似題
-
1.鋁是應用廣泛的金屬。以鋁土礦(主要成分為Al2O3,含SiO2和Fe2O3等雜質)為原料制備鋁的一種工藝流程如下:
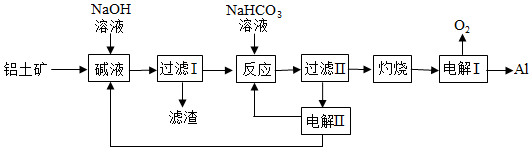
注:SiO2在“堿溶”時轉化為鋁硅酸鈉沉淀。
(1)“堿溶”時生成偏鋁酸鈉的離子方程式為。
(2)向“過濾Ⅰ”所得濾液中加入NaHCO3溶液,溶液的pH(填“增大”、“不變”或“減小”)。
(3)“電解Ⅰ”是電解熔融 Al2O3,電解過程中作陽極的石墨易消耗,原因是。
(4)“電解Ⅱ”是電解Na2CO3溶液,原理如圖所示。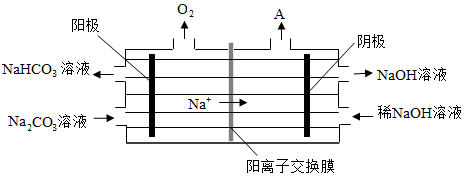
陽極的電極反應式為,陰極產生的物質A的化學式為。
(5)鋁粉在1000℃時可與N2反應制備AlN.在鋁粉中添加少量NH4Cl固體并充分混合,有利于AlN的制備,其主要原因是。發布:2024/6/27 10:35:59組卷:1521引用:21難度:0.5 -
2.以鋁土礦(主要成分為Al2O3,含少量SiO2和Fe2O3等雜質)為原料生產鋁和氮化鋁的一種工藝流程如下[已知:SiO2在“堿溶”時轉化為鋁硅酸鈉(NaAlSiO4?nH2O)沉淀]。

(1)用氧化物的形式表示鋁硅酸鈉的化學式。
(2)溶液a中加入NaHCO3后,生成沉淀的離子方程式為。
(3)有人考慮用熔融態AlCl3電解制備鋁,你覺得是否可行?請說明理由:。
(4)取一定量的氮化鋁樣品,用以下裝置測定樣品中AlN的純度(夾持裝置已略去)。打開K2,加入NaOH濃溶液,至不再產生NH3.打開K1,通入N2一段時間。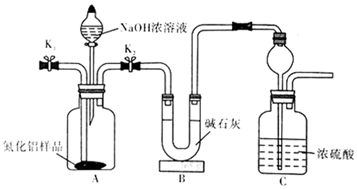
①寫出AlN與NaOH溶液反應的化學方程式。
②實驗中需要測定的數據是。發布:2024/4/20 14:35:0組卷:145引用:3難度:0.7 -
3.工業上用鋁土礦(主要成分為Al2O3,含有少量SiO2、FeO?xFe2O3等雜質)制取鋁的一種工藝流程示意圖如圖:
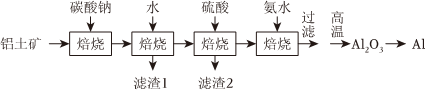
已知:Al2O3+Na2CO32NaAlO2+CO2↑△
(1)“焙燒”步驟中,不能使用陶瓷坩堝的原因是;
(2)“濾渣1”中的主要金屬元素為;“濾渣2”成分的化學式為;不能用二氧化碳代替硫酸溶液的原因是;
(3)寫出向“濾液2”滴加氨水至過量的主要的離子反應方程式;
(4)寫出工業冶煉鋁的化學反應方程式;
(5)若現在有a t鋁土礦,其中鋁元素的質量分數為10.8%,最終制得鋁錠b kg,則該流程的產率為%(用含a、b的代數式表示,結果需化簡)。發布:2024/6/27 10:35:59組卷:400引用:2難度:0.6


