某化學興趣小組以“生命之源——水”為主題開展項目式學習。
【任務一】認識水的蒸發
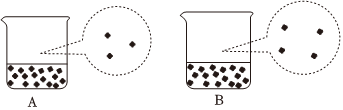
(1)如圖是兩杯等體積的水在不同溫度下放置時發生變化的微觀示意圖,已知兩杯水的水溫分別是20℃和50℃,則溫度為20℃的水為 AA(填序號)。
【任務二】探究水的電解
如圖是興趣小組利用注射器改裝的電解水實驗裝置。燒杯中盛有用煮沸后冷卻的蒸餾水配制成的2%的氫氧化鈉溶液,注射器排盡空氣后,吸取氫氧化鈉溶液20mL,接通電源。
(2)實驗中可觀察到 兩支注射器內均有氣泡產生,左側液面下降比右側更快(或左側產生氣體比右側多)兩支注射器內均有氣泡產生,左側液面下降比右側更快(或左側產生氣體比右側多),經檢驗氣體成分后,可推知水是由 氫元素和氧元素氫元素和氧元素組成的。
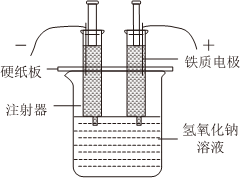
(3)該裝置的優點有 材料簡便易得或儀器加工簡單(合理即可)材料簡便易得或儀器加工簡單(合理即可)(寫一條即可)。
【任務三】再探究影響電解水速率的因素
以收集到20mL氫氣為標準,記錄時間和收集氧氣的體積,實驗數據如下表。
| 實驗序號 | ① | ② | ③ | ④ | ⑤ |
| 氫氧化鈉溶液的溫度/℃ | 15 | 15 | 15 | 30 | 45 |
| 外加電壓/V | 6 | 9 | 12 | 6 | 6 |
| 氧氣/mL | 9.9 | 10. | 9.0 | 9.6 | 9.7 |
| 時間/s | 54.6 | 23.4 | 15.0 | 46.2 | 35.4 |
外加電壓
外加電壓
因素對電解水快慢的影響;欲探究氫氧化鈉溶液的溫度對電解水快慢的影響,應選擇的實驗是 ①④⑤
①④⑤
(填實驗序號)。(5)根據表中實驗現象得出的結論是
其他條件相同時,外加電壓越大,電解速率越快;反應溫度越高,電解速率越快
其他條件相同時,外加電壓越大,電解速率越快;反應溫度越高,電解速率越快
。(6)影響電解水快慢除上述因素外,可能還有
氫氧化鈉溶液的濃度(或電極的材質)
氫氧化鈉溶液的濃度(或電極的材質)
(寫出1點即可),請設計實驗方案 在溫度和外加電壓都相同的條件下(或“在其他條件相同的條件下”),分別配制不同濃度的氫氧化鈉溶液進行實驗,測收集到等體積氫氣所需時間(合理即可)
在溫度和外加電壓都相同的條件下(或“在其他條件相同的條件下”),分別配制不同濃度的氫氧化鈉溶液進行實驗,測收集到等體積氫氣所需時間(合理即可)
。【考點】電解水實驗;分子的定義與分子的特性.
【答案】A;兩支注射器內均有氣泡產生,左側液面下降比右側更快(或左側產生氣體比右側多);氫元素和氧元素;材料簡便易得或儀器加工簡單(合理即可);外加電壓;①④⑤;其他條件相同時,外加電壓越大,電解速率越快;反應溫度越高,電解速率越快;氫氧化鈉溶液的濃度(或電極的材質);在溫度和外加電壓都相同的條件下(或“在其他條件相同的條件下”),分別配制不同濃度的氫氧化鈉溶液進行實驗,測收集到等體積氫氣所需時間(合理即可)
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/8/1 8:0:9組卷:141引用:1難度:0.5
相似題
-
1.習近平總書記在推進南水北調工程座談會上強調:水是生存之本、文明之源。
(1)水(填“屬于”、“不屬于”)六大營養素。
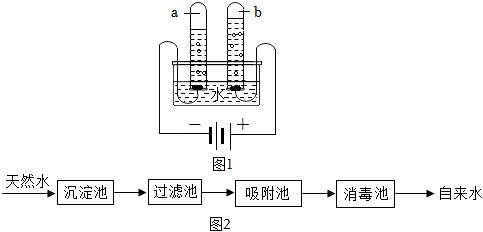
(2)圖1是電解水的實驗示意圖,試管(填“a”或“b”)中的氣體可以做氣體燃料,電解水的化學方程式為。
(3)天然水凈化為自來水的主要流程如圖2所示:
①“沉淀池”中可用明礬作絮凝劑,化學式為KAl(SO4)n?12H2O,n的值為。
②“吸附池”中常用(填物質名稱)吸附色素和異味。
③“消毒池”中常用液氯作消毒劑,發生了反應:Cl2+H2O=HCl+HClO。若用自來水直接配制硝酸銀溶液,會產生沉淀(填化學式)。
④次氯酸(HClO)可除去廢水中的NH3,產物有鹽酸和單質氣體生成,該氣體常用作食品保鮮填充氣,該氣體為(填化學式)。發布:2024/12/25 12:0:1組卷:73引用:2難度:0.6 -
2.研究“水”可從多角度展開。
(1)水的電解
①宏觀現象:按圖1所示裝置,通電一段時間后,試管A、B中產生氣體的體積比約為,檢驗B中氣體的現象是。
②微觀分析:該反應中發生分解的微粒名稱是。
③結論:水由組成。
(2)水的性質
將黃豆大小的金屬鉀放入盛有水的燒杯中,生成H2;在反應后的溶液中滴入酚酞試液,溶液變紅。寫出該反應的化學方程式。
(3)水的用途
①碘與鋅在常溫下反應速度很慢,若滴入幾滴水則反應劇烈,水在此的作用是。
②圖2實驗中,對水的主要作用分析不全面的是(填字母)。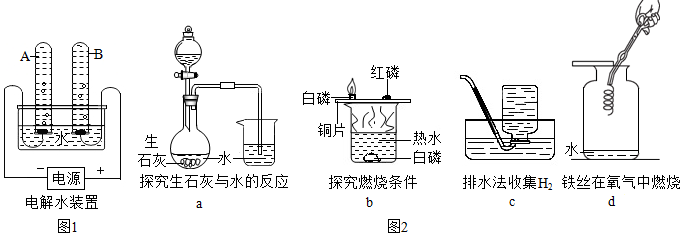
A.a圖中的水便于觀察燒瓶內氣壓變化
B.b圖中的水提供熱量
C.c圖集氣瓶中的水排盡空氣且便于觀察H2何時集滿
D.d圖中的水防止熔融物炸裂集氣瓶發布:2024/12/25 13:0:1組卷:384引用:18難度:0.5 -
3.夏季多暴雨,對居民生活用水會造成一定影響。下列關于水的說法不正確的是( )
A.暴雨會造成水庫水體渾濁,過濾后可得到純水 B.加入活性炭可吸附水中的異味、色素等 C.生活中可以通過煮沸的方法降低水的硬度 D.電解水時生成的氫氣和氧氣的體積比為2:1 發布:2025/1/1 14:30:4組卷:27引用:1難度:0.8


