鎘(Cd)可用于制作發光電子組件。以銅鎘廢渣(含Cu、Cd、Zn、Fe等單質)為原料制備鎘的工藝流程如下:
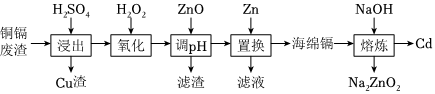
浸出后的溶液中含有Cd2+、Zn2+、Fe2+等金屬離子,相關金屬離子形成氫氧化物沉淀的pH (開始沉淀的pH按金屬離子濃度為1.0mol?L-1計算)如表:
| 氫氧化物 | Fe(OH)3 | Zn(OH)2 | Cd(OH)2 |
| 開始沉淀的pH | 1.5 | 5.9 | 7.2 |
| 沉淀完全的pH | 3.3 | 8.9 | 9.9 |
防止Cu在酸性條件下被O2氧化生成Cu2+,導致Cu被浸出
防止Cu在酸性條件下被O2氧化生成Cu2+,導致Cu被浸出
。(2)“氧化”時發生反應的離子方程式為
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe2++H2O2+2H+=2Fe3++2H2O
。HNO3也能氧化Fe2+,工業生產中不選用HNO3的原因是 會釋放出氮氧化物(或NO、NO2),造成環境污染
會釋放出氮氧化物(或NO、NO2),造成環境污染
。(3)“調pH”時控制溶液pH在3.3~5.9之間,“濾渣”的主要成分是
Fe(OH)3
Fe(OH)3
(填化學式)。(4)“置換”時發生的反應為Zn+Cd2+=Zn2++Cd。
鎘置換率[鎘置換率=
n
(
C
d
)
n
(
起始的
C
d
2
+
)
n
(
加入的
Z
n
)
n
(
起始的
C
d
2
+
)
n
(
加入的
Z
n
)
n
(
起始的
C
d
2
+
)
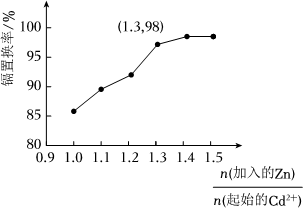
比值小于1.3時,鎘置換率低;比值大于1.3時,鋅粉用量增大,鎘置換率提升不大,且鋅粉過多會消耗更多的NaOH
比值小于1.3時,鎘置換率低;比值大于1.3時,鋅粉用量增大,鎘置換率提升不大,且鋅粉過多會消耗更多的NaOH
。
(5)Cd和Zn同族且相鄰,部分金屬水合離子的顏色如下表所示:
| 離子 | 26Fe2+ | 29Cu2+ | 21Sc3+ | 30Zn2+ | 48Cd2+ |
| 顏色 | 淺綠色 | 藍色 | 無色 | 無色 | 無色 |
如果金屬離子核外存在未成對電子則金屬水合離子有顏色,反之則無色
如果金屬離子核外存在未成對電子則金屬水合離子有顏色,反之則無色
。②硫酸酸化的硫酸鐵溶液中鐵元素以[Fe(H2O)6]3+形式存在而使溶液呈淺紫色,向其中滴入幾滴KSCN溶液,因生成[Fe(H2O)5(SCN)]2+、[Fe(H2O)4(SCN)2]+等離子而使溶液呈紅色,能發生上述反應的原因是
SCN-比H2O更容易與Fe3+形成配合物
SCN-比H2O更容易與Fe3+形成配合物
。【考點】物質分離和提純的方法和基本操作綜合應用.
【答案】防止Cu在酸性條件下被O2氧化生成Cu2+,導致Cu被浸出;2Fe2++H2O2+2H+=2Fe3++2H2O;會釋放出氮氧化物(或NO、NO2),造成環境污染;Fe(OH)3;比值小于1.3時,鎘置換率低;比值大于1.3時,鋅粉用量增大,鎘置換率提升不大,且鋅粉過多會消耗更多的NaOH;如果金屬離子核外存在未成對電子則金屬水合離子有顏色,反之則無色;SCN-比H2O更容易與Fe3+形成配合物
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:59引用:1難度:0.6
相似題
-
1.我國青藏高原的鹽湖中蘊藏著豐富的鋰資源,已探明的儲量約三千萬噸,碳酸鋰制備高純金屬鋰的一種工藝流程如圖。下列有關說法錯誤的是( )
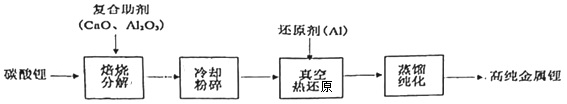
A.金屬鋰可保存在煤油中 B.使用復合助劑有利于碳酸鋰的分解 C.“粉碎”是為了增加接觸面積,加快反應速率 D.真空熱還原發生的主要化學反應為2Al+3Li2O 6Li+Al2O3高溫發布:2025/1/6 7:30:5組卷:28引用:2難度:0.9 -
2.硫鐵礦燒渣是硫鐵礦生產硫酸過程中產生的工業廢渣(主要含Fe2O3及少量SiO2、Al2O3等雜質)。用該燒渣制取藥用輔料-紅氧化鐵的工藝流程如圖:
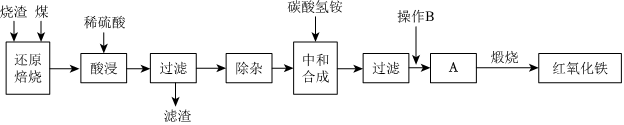
(1)在“還原焙燒”中產生的有毒氣體可能有。
(2)“酸浸”時間一般不超過20min,若在空氣中酸浸時間過長,溶液中Fe2+含量將下降,其原因是(用離子方程式表示)。
(3)“中和合成”的目的是將溶液中Fe2+轉變為碳酸亞鐵沉淀,則操作B是。
(4)煅燒A的反應方程式是。
(5)ag燒渣經過上述工藝可得紅氧化鐵bg。藥典標準規定,制得的紅氧化鐵中含氧化鐵不得少于98.0%,則所選用的燒渣中鐵的質量分數應不低于(用含a、b的表達式表示)。發布:2025/1/19 8:0:1組卷:30引用:1難度:0.5 -
3.查閱資料:CaO、MgO在高溫下與C難反應,但能與SiO2反應.硫鐵礦燒渣是一種工業廢渣(含Fe2O3及少量SiO2、Al2O3、CaO、MgO等雜質),該燒渣可用于制取氧化鐵,具體化工生產工藝流程如下:
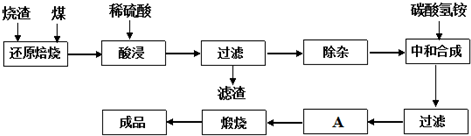
(1)焙燒時產生的主要有害氣體是.
(2)若在空氣中“酸浸”時間過長,溶液中Fe2+含量將下降,其原因是:(用離子方程式表示).
(3)根據下表數據:
在“除雜”步驟中,為除去Fe3+和Al3+,溶液的pH最大值應小于氫氧化物 Al(OH)3 Fe(OH)3 Fe(OH)2 開始沉淀的pH 3.10 2.01 7.11 完全沉淀的pH 4.77 3.68 9.61 ,檢驗Fe3+已經除盡的試劑是(除KSCN外).
(4)“中和合成”的目的是將溶液中Fe2+轉變為碳酸亞鐵沉淀,則A的操作是.發布:2025/1/19 8:0:1組卷:12引用:1難度:0.1


