 前四周期元素X、Y、Z、W、R的原子序數依次增大,已知:X原子的2p軌道為半充滿狀態;Y原子的L層有2個未成對電子;Z與Y位于同主族;W的+2價簡單離子核外電子層排布與氬原子相同;R原子的d軌道上有3個空軌道.請回答下列問題:
前四周期元素X、Y、Z、W、R的原子序數依次增大,已知:X原子的2p軌道為半充滿狀態;Y原子的L層有2個未成對電子;Z與Y位于同主族;W的+2價簡單離子核外電子層排布與氬原子相同;R原子的d軌道上有3個空軌道.請回答下列問題:
(1)X原子的電子排布圖為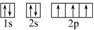
 ,R基態原子的價層電子排布式為3d24s23d24s2.
,R基態原子的價層電子排布式為3d24s23d24s2.
(2)X、Y原子的第一電離能大小順序為N>ON>O(用元素符號表示).
(3)1mol X的常見單質分子結構中σ鍵數目為6.02×10236.02×1023.
(4)Z的最高價氧化物對應水化物的酸根離子空間構型為正四面體正四面體,中心原子的雜化軌道類型為sp3sp3.
(5)WY的晶體類型是離子晶體離子晶體,Y的氫化物的沸點高于Z的氫化物的沸點,原因是水分子間存在氫鍵水分子間存在氫鍵.
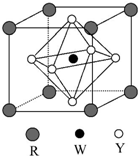
(6)某礦物晶體由Y、W、R三種元素組成,其晶胞結構如圖所示.
則該礦物的化學式為CaTiO3CaTiO3,若已知該晶胞的邊長為acm,則該晶胞的密度為136a3NA136a3NAg?cm-3.(用含a、NA的代數式表示).


136
a
3
N
A
136
a
3
N
A
【考點】晶胞的計算;位置結構性質的相互關系應用.
【答案】 ;3d24s2;N>O;6.02×1023;正四面體;sp3;離子晶體;水分子間存在氫鍵;CaTiO3;
;3d24s2;N>O;6.02×1023;正四面體;sp3;離子晶體;水分子間存在氫鍵;CaTiO3;
 ;3d24s2;N>O;6.02×1023;正四面體;sp3;離子晶體;水分子間存在氫鍵;CaTiO3;
;3d24s2;N>O;6.02×1023;正四面體;sp3;離子晶體;水分子間存在氫鍵;CaTiO3;136
a
3
N
A
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:17引用:3難度:0.5
相似題
-
 1.碳及其化合物有著重要用途。回答下列問題:
1.碳及其化合物有著重要用途。回答下列問題:
(1)基態碳原子的價層電子排布圖為。
(2)在CH2=CHCN中,碳原子的雜化方式有、,所含σ鍵數目和π鍵數目之比為。
(3)甲烷、水、氨氣中C、O、N原子均采用sp3雜化方式,VSEPR模型均為正四面體構型,比較三者鍵角的大小(由大到小,用H一R-H表示),其原因是。
(4)C60室溫下為紫紅色固體,不溶于水,能溶于四氯化碳等非極性溶劑。據此判斷C60的晶體類型是。
(5)C60晶胞結構如圖,C60分子處于頂點和面心。已知:C60晶胞棱長為14.20? (1?=10-8cm),則C60的晶體密度為g/cm3。
C60體中存在正四面體空隙(例如1、3、6、7四點構成)和正八面體空隙(例如3、6、7、8、9、12六點構成),則平均每一個C60晶胞中有個正四面體空隙和4個正八面體空隙。當堿金屬元素全部占滿所有空隙后,這類C60摻雜物才具有超導性。若用金屬銫(Cs)填滿所有空隙,距離最近的兩個Cs原子間的距離為?。發布:2025/1/5 8:0:1組卷:53引用:2難度:0.4 -
 2.A、B、C、D、E、F是元素周期表中前四周期元素,且原子序數依次增大,其相關信息如下:
2.A、B、C、D、E、F是元素周期表中前四周期元素,且原子序數依次增大,其相關信息如下:
①A的周期序數等于其主族序數;
②B、D原子的L層中都有兩個未成對電子;
③E元素原子最外層電子排布式為(n+1)Sn(n+1)Pn-1;
④F原子有四個能層,K、L、M全充滿,最外層只有一個電子.
試回答下列問題:
(1)基態E原子中,電子占據的最高能層符號為,F的價層電子排布式為.
(2)B、C、D的電負性由大到小的順序為(用元素符號填寫),C與A形成的分子CA3的VSEPR模型為.
(3)B和D分別與A形成的化合物的穩定性:BA4小于A2D,原因是.
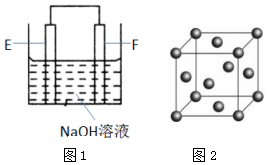
(4)以E、F的單質為電極,組成如圖1所示的裝置,E極的電極反應式為.
(5)向盛有F的硫酸鹽FSO4的試管里逐滴加入氨水,首先出現藍色沉淀,繼續滴加氨水,藍色沉淀溶解,得到深藍色溶液,再向深藍色透明溶液中加入乙醇,析出深藍色晶體.藍色沉淀溶解的離子方程式為.
(6)F的晶胞結構(面心立方)如圖2所示:已知兩個最近的F的距離為acm,F的密度為g/cm3(阿伏加德羅常數用NA表示,F的相對原子質量用M表示)發布:2025/1/18 8:0:1組卷:14引用:2難度:0.5 -
 3.鐵及其化合物在生產生活及科學研究方面應用非常廣泛。
3.鐵及其化合物在生產生活及科學研究方面應用非常廣泛。
(1)基態Fe原子的價層電子的電子排布圖為;其最外層電子的電子云形狀為。
(2)(NH4)2Fe(SO4)2?6H2O俗稱摩爾鹽
①NH4+電子式為。
②N、O兩元素的第一電離能由大到小的順序為(用元素符號表示)
③SO42-中S原子的雜化方式為,VSEPR模型名稱為。
(3)K3[Fe(CN)6]晶體中中心原子的配位數為;晶體的配位體為(用化學符號表示)
(4)FeS2晶體的晶胞如圖(c)所示。晶胞邊長為a nm、FeS2相對式量為M,阿伏加德羅常數的值為NA,其晶體密度的計算表達式為g?cm-3發布:2025/1/5 8:0:1組卷:7引用:1難度:0.7


