當前位置:
試題詳情
人們的日常生活離不開金屬,高科技新材料的開發和應用也需要金屬。
(1)地殼中含量居第一位的金屬元素是AlAl(填元素符號)。
(2)日常使用的金屬材料多數屬于合金,與組成合金的純金屬相比,合金的優點一般有②③④②③④(填序號)
①強度更低;②硬度更高;③熔點低;④抗腐蝕性更好
(3)某化學興趣小組的學生發現金屬R不在初中學到的金屬活動性順序表中,該小組為了了解R與常見金屬鋁、銅的金屬活動性順序,進行如下探究活動;
【作出猜想】他們考慮到鋁的活動性比銅強,對三種金屬的活動性順序作出如下猜想:
猜想一:Al>Cu>R;
猜想二Al>R>CuAl>R>Cu
猜想三:R>Al>Cu
【查閱資料】R是一種銀白色的金屬,在R的鹽溶液中只有+2價,R的鹽溶液呈藍色,常溫下鋁的表面會形成一層致密的氧化膜:硫酸鋁、氧化鋁、硝酸鋁的溶液均為無色。
【實驗探究】為了探究哪一種猜想成立,甲、乙、丙三名同學分別針對猜想一、猜想二、猜想三設計實驗方案并展開實驗探究。
| 猜想 | 主要操作 | 主要現象 | 實驗結論 |
| 猜想一 | 打磨R絲,并將其插入到硫酸銅溶液中 | R絲表面覆蓋了一層紅色的物質 | 猜想一 不成立 不成立 (填“成立”或“不成立”) |
| 猜想二 | 打磨粗細相同的R絲、鋁絲、銅絲,分別將它們插入到體積相同、溶質質量分數也相同的稀硫酸中 | ①R絲表面產生氣泡緩慢,溶液由無色逐漸變成藍色 ②鋁絲表面產生氣泡較快 ③銅絲表面沒有氣泡產生 |
猜想二成立。 R與稀硫酸反應的化學方程式為 R+H2SO4=RSO4+H2↑ R+H2SO4=RSO4+H2↑ |
| 猜想三 | 將鋁絲插入到RSO4溶液中 將鋁絲插入到RSO4溶液中
|
無明顯現象 | 猜想三成立 |
究竟哪種猜想成立?三名同學經討論交流發現丙同學在實驗前沒有打磨鋁絲,這可能會導致實驗結論錯誤。于是他們先打磨鋁絲,再將其插入到丙同學做實驗用過的溶液中,一段時間后溶液的顏色
消失
消失
;進而確認猜想三不成立,猜想二成立。(4)為了測定銅鋅合金樣品中鋅的質量稱取樣品20g于燒杯中,向其中加入50g稀硫酸至恰好完全反應反應后燒杯中物質的總質量為69.8g。請計算:樣品中鋅的質量。
【答案】Al;②③④;Al>R>Cu;不成立;R+H2SO4=RSO4+H2↑;將鋁絲插入到RSO4溶液中;消失
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/11/5 8:0:2組卷:41引用:1難度:0.3
相似題
-
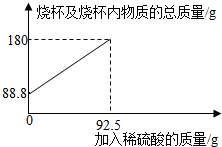 1.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為51.8克的燒杯中,然后逐步加入一定質量分數的稀硫酸,當加入92.5g稀硫酸時恰好完全反應,加入稀硫酸的質量與燒杯及燒杯內物質的總質量的關系如圖。
1.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為51.8克的燒杯中,然后逐步加入一定質量分數的稀硫酸,當加入92.5g稀硫酸時恰好完全反應,加入稀硫酸的質量與燒杯及燒杯內物質的總質量的關系如圖。
(1)該實驗取用的樣品質量為g。
(2)反應后所得溶液中的溶質的質量分數。(寫出計算過程,結果保留一位小數)
(3)反應結束后,小明不慎向燒杯中多加了10g稀硫酸,若在圖中補繪此過程中稀硫酸的質量與燒杯及燒杯內物質的總質量的關系圖,所得線段的終點位于線段AB延長線的(填:上方、下方或線上)。發布:2025/1/9 8:0:2組卷:4引用:1難度:0.3 -
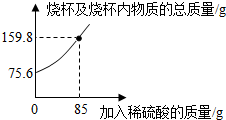 2.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為52.2g的燒杯中,然后緩慢加入一定質量的稀硫酸,當加稀硫酸質量為85g時,反應恰好完全(雜質不反應且產生的氣體全部逸出),反應過程中的質量關系如圖.完成下列問題:
2.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為52.2g的燒杯中,然后緩慢加入一定質量的稀硫酸,當加稀硫酸質量為85g時,反應恰好完全(雜質不反應且產生的氣體全部逸出),反應過程中的質量關系如圖.完成下列問題:
(1)該實驗取用的樣品質量為g.
(2)計算樣品中鐵的質量分數(寫出解題過程).發布:2025/1/9 8:0:2組卷:139引用:39難度:0.1 -
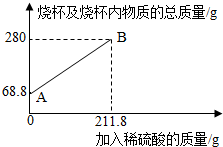 3.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為51.8克的燒杯中,然后逐步加入一定質量分數的稀硫酸,當加入211.8g稀硫酸時恰好完全反應,加入稀硫酸的質量與燒杯及燒杯內物質的總質量的關系如圖。
3.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為51.8克的燒杯中,然后逐步加入一定質量分數的稀硫酸,當加入211.8g稀硫酸時恰好完全反應,加入稀硫酸的質量與燒杯及燒杯內物質的總質量的關系如圖。
(1)該實驗取用的樣品質量為g。
(2)求樣品中鐵的質量分數;反應后所得溶液中的溶質的質量分數。(寫出計算過程,結果保留一位小數)
(3)反應結束后,小明不慎向燒杯中多加了20g稀硫酸,若在圖中補繪此過程中稀硫酸的質量與燒杯及燒杯內物質的總質量的關系圖,所得線段的終點位于線段AB延長線的(填:上方、下方或線上)。發布:2025/1/9 8:0:2組卷:8引用:1難度:0.3


