從能量轉化角度看,原電池是將化學能轉化為電能的裝置;從化學反應角度看,原電池的原理是氧化還原反應中的還原劑失去的電子經外接導線傳遞給氧化劑,使氧化還原反應分別在兩個電極上進行。
(1)下列反應通過原電池裝置,不能實現化學能直接轉化為電能的是(填序號) BB。
A.2H2+O2 點燃 2H2O
B.CaO+H2O=Ca(OH)2
C.Fe+Cu2+=Cu+Fe2+
(2)FeCl3常用于腐蝕印刷電路銅板,反應過程的離子方程式為 2Fe3++Cu=2Fe2++Cu2+2Fe3++Cu=2Fe2++Cu2+,若將此反應設計成原電池,請寫出該原電池正極的電極反應:Fe3++e-=Fe2+Fe3++e-=Fe2+。
(3)如圖是某化學興趣小組探究不同條件下化學能轉變為電能的裝置。請回答下列問題:
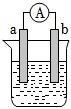
①當電極a為Zn片,電極b為Cu片,且兩極板質量相等。電解質溶液為CuSO4溶液,當電路中有0.1mole-通過時,兩極板的質量差為 6.456.45g。
②當電極a為Mg片,電極b為Al片,電解質溶液為NaOH溶液時,則負極的電極反應式為 Al-3e-+4OH-=AlO-2+2H2OAl-3e-+4OH-=AlO-2+2H2O。
(4)某種燃料電池的工作原理示意圖如圖所示,a、b均為惰性電極。
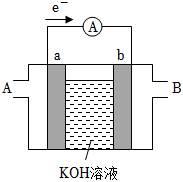
①空氣從 BB(填“A”或“B”)口通入,溶液中OH-移向 aa極(填“a”或“b”)。
②當電路中通過2mol電子時,理論上消耗標準狀況下的O211.211.2L。
點燃
A
l
O
-
2
A
l
O
-
2
【考點】原電池與電解池的綜合.
【答案】B;2Fe3++Cu=2Fe2++Cu2+;Fe3++e-=Fe2+;6.45;Al-3e-+4OH-=+2H2O;B;a;11.2
A
l
O
-
2
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:16引用:2難度:0.5
相似題
-
1.關于如圖所示的原電池,下列說法正確的是( )
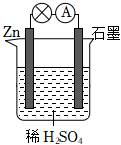
A.石墨電極上發生氧化反應 B.電子由鋅片通過導線流向石墨棒 C.該裝置將電能轉化為化學能 D.將稀硫酸換成乙醇,燈泡亮度不變 發布:2025/1/6 6:0:5組卷:83引用:5難度:0.8 -
2.某原電池結構如圖所示,下列有關該原電池的說法正確的是( )
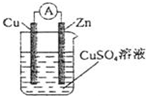
A.銅棒為負極 B.鋅棒發生還原反應 C.電子從銅棒經外電路流向鋅棒 D.鋅棒質量減輕 發布:2025/1/6 6:0:5組卷:417引用:11難度:0.9 -
3.一種新型短路膜電化學電池消除CO2裝置如圖所示。下列說法錯誤的是( )
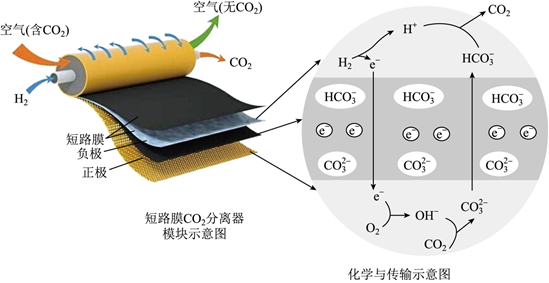
A.負極反應為:H2+2OH--2e-=2H2O B.正極反應消耗標準狀況下22.4LO2,理論上需要轉移4mol電子 C.短路膜和常見的離子交換膜不同,它既能傳遞離子,還可以傳遞電子 D.該裝置可用于空氣中CO2的捕獲,緩解溫室效應 發布:2024/12/30 19:30:2組卷:51引用:5難度:0.5


