回答問題:
(1)高鐵酸鉀(K2FeO4)不僅是一種理想的水處理劑,而且高鐵電池的研制也在進行中。如圖1所示是高鐵電池的模擬實驗裝置。

①該電池放電時正極反應式為 FeO42-+4H2O+3e-═Fe(OH)3↓+5OH-FeO42-+4H2O+3e-═Fe(OH)3↓+5OH-。
②鹽橋中盛有飽和KCl溶液,此鹽橋中氯離子向 右右(填“左”或“右”)移動;
③圖2為高鐵電池和常用的高能堿性電池的放電曲線,由此可得出高鐵電池的優點 使用時間長、工作電壓穩定使用時間長、工作電壓穩定。
(2)一定溫度下,反應H2+Cl2═2HCl中的某一基元反應為H2+Cl═HCl+H,其能量變化如圖所示。H…H…Cl表示反應物分子舊化學鍵沒有完全斷裂、新化學鍵沒有完全形成的過渡態。

該基元反應的活化能為 21.521.5 kJ?mol-1,ΔH為 +7.5+7.5kJ?mol-1。
(3)已知:Ⅰ.C(石墨,s)+O2(g)═CO2(g) ΔH1=-393.5 kJ?mol-1
Ⅱ.2H2(g)+O2(g)═2H2O(l) ΔH2=-571.6 kJ?mol-1
Ⅲ.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l) ΔH3=-2 599.2 kJ?mol-1
則由C(石墨,s)和H2(g)反應生成1mol C2H2(g)的焓變為 +226.7kJ?mol?1+226.7kJ?mol?1。
【答案】FeO42-+4H2O+3e-═Fe(OH)3↓+5OH-;右;使用時間長、工作電壓穩定;21.5;+7.5;+226.7kJ?mol?1
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:18引用:1難度:0.6
相似題
-
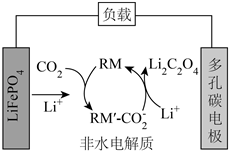 1.我國某科研團隊借助氧化還原介質RM,將Li-CO2電池的放電電壓提高至3V以上,該電池的工作原理如圖。下列說法正確的是( )
1.我國某科研團隊借助氧化還原介質RM,將Li-CO2電池的放電電壓提高至3V以上,該電池的工作原理如圖。下列說法正確的是( )A.LiFePO4電極的電勢比多孔碳電極的高 B.負極反應:LiFePO4-xe-═Li(1-x)FePO4+xLi+ C.RM和RM′- 均為該電池反應的催化劑CO-2D.LiFePO4電極每減重7g,就有22gCO2被固定 發布:2024/12/20 4:30:1組卷:156引用:2難度:0.5 -
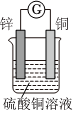 2.如圖所示將鋅、銅通過導線相連,置于硫酸銅溶液中。
2.如圖所示將鋅、銅通過導線相連,置于硫酸銅溶液中。
(1)該裝置將轉化為能。
(2)Zn電極為極,發生反應,電極方程式為。
(3)外電路電子由電極經導線流向電極。
(4)若反應過程中鋅溶解了6.5g,則銅電極增重g,該回路中轉移的電子數為。發布:2024/12/30 3:0:4組卷:309引用:2難度:0.7 -
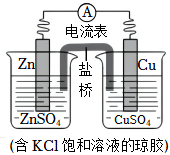 3.銅鋅原電池的裝置如圖,其中鹽橋為內含KCl的瓊脂凝膠,下列說法不正確的是( )
3.銅鋅原電池的裝置如圖,其中鹽橋為內含KCl的瓊脂凝膠,下列說法不正確的是( )A.Zn是負極反應物,發生氧化反應 B.電子從鋅片流向銅片 C.銅電極上發生反應Cu2++2e-═Cu D.鹽橋中Cl-進入CuSO4溶液 發布:2024/12/15 19:30:1組卷:194引用:1難度:0.5


