當前位置:
試題詳情
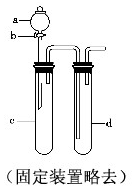 銅與稀硝酸反應產生NO,NO又被氧化成NO2,對實驗觀察無色NO有干擾,過多的NO、NO2又會污染環境,改進實驗的涉及符合綠色化學的思想.有興趣小組設計出如圖所示裝置來改進教材中“銅與硝酸反應”的實驗,以探究化學實驗的綠色化.
銅與稀硝酸反應產生NO,NO又被氧化成NO2,對實驗觀察無色NO有干擾,過多的NO、NO2又會污染環境,改進實驗的涉及符合綠色化學的思想.有興趣小組設計出如圖所示裝置來改進教材中“銅與硝酸反應”的實驗,以探究化學實驗的綠色化.
(1)實驗前,關閉活塞b,試管d中加水至浸沒長導管口,塞緊試管c和d的膠塞,加熱c,其目的在于檢驗裝置氣密性檢驗裝置氣密性;
(2)在d中加適量NaOH溶液,c中放一小塊銅片,由分液漏斗a向c中加入2mL濃硝酸,c中反應的化學方程式Cu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2OCu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2O;再由a向c中加2mL蒸餾水,c中實驗現象為反應變緩,氣體顏色變淺反應變緩,氣體顏色變淺;
(3)表中是制取硝酸銅的三種方案,能體現綠色化學理念的最佳方案是丙丙,理由是制取等量的硝酸銅時,丙方案耗酸量最少,無污染制取等量的硝酸銅時,丙方案耗酸量最少,無污染.
| 方案 | 反應物 |
| 甲 | Cu、濃硝酸 |
| 乙 | Cu、稀硝酸 |
| 丙 | Cu、O2、稀硝酸 |
向d中加入KBr溶液,c中加入固體KMnO4,由a向c中加入濃鹽酸
向d中加入KBr溶液,c中加入固體KMnO4,由a向c中加入濃鹽酸
,實驗現象為c中有黃綠色氣體產生,d中溶液變為橙色
c中有黃綠色氣體產生,d中溶液變為橙色
,但此實驗的不足之處是未處理尾氣
未處理尾氣
.【答案】檢驗裝置氣密性;Cu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2O;反應變緩,氣體顏色變淺;丙;制取等量的硝酸銅時,丙方案耗酸量最少,無污染;向d中加入KBr溶液,c中加入固體KMnO4,由a向c中加入濃鹽酸;c中有黃綠色氣體產生,d中溶液變為橙色;未處理尾氣
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/12/21 8:0:2組卷:31引用:2難度:0.3
相似題
-
1.有關硝酸化學性質的敘述中,正確的是( )
A.硝酸能與Na2CO3、Na2S、Na2SO3等鹽反應,產生CO2、H2S和SO2 B.硝酸與FeO反應生成Fe(NO3)2和水,與Fe反應生成Fe(NO3)2和H2 C.濃硝酸、稀硝酸都只能使藍色石蕊試紙變紅 D.濃硝酸因分解放出的NO2又溶解于濃硝酸而使之呈黃色 發布:2024/12/30 5:0:1組卷:53引用:5難度:0.7 -
2.下列有關化學反應的敘述正確的是( )
A.常溫下Cu和濃硫酸反應生成CuSO4 B.過量的Fe與稀硝酸反應生成Fe(NO3)2 C.光照條件下,甲苯和Cl2反應生成鄰氯甲苯 D.加熱條件下,溴乙烷與NaOH水溶液反應生成乙烯 發布:2025/1/3 17:30:5組卷:28引用:1難度:0.7 -
3.稀HNO3還原產物可以是:①NO、②N2O、③N2、④NH4NO3.在稀HNO3和Zn的反應中,若有1mol HNO3參加反應,則有0.8mol電子轉移,由此推斷稀HNO3的還原產物為( )
A.僅④ B.②和④ C.③和④ D.僅② 發布:2024/12/30 4:30:1組卷:97引用:5難度:0.9


