海洋化學資源的綜合利用對人類的發展意義重大。
Ⅰ.食鹽是日常生活的必需品,也是重要的化工原料。粗鹽中常含有少量泥沙及Ca2+、Mg2+、SO2-4等雜質離子。為除去粗鹽中的Ca2+、Mg2+、SO2-4以及泥沙等雜質,某同學設計了一種制備精鹽的實驗方案,步驟如圖:
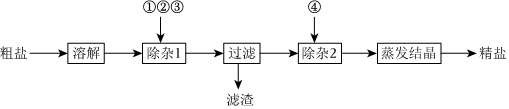
(1)為除去Ca2+、Mg2+、SO2-4,按照順序加入試劑①~③,可以是下列組合中的 BDBD(填字母)。
A.①Na2CO3②BaCl2③NaOH
B.①BaCl2②NaOH③Na2CO3
C.①NaOH②Na2CO3③BaCl2
D.①BaCl2②Na2CO3③NaOH
(2)步驟“除雜2”中涉及反應的離子方程式有:H++OH-=H2O、CO2-3+2H+=H2O+CO2↑H++OH-=H2O、CO2-3+2H+=H2O+CO2↑。
(3)粗鹽提純的整個操作過程中多處需要使用到玻璃棒,“過濾”過程中使用玻璃棒的作用是 引流引流。
Ⅱ.從海帶中提取碘的工業生產過程如圖:
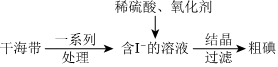
(4)氧化劑將I-→I2。下列氧化劑中,最好選用 DD(填字母)。
A.酸性KMnO4
B.新制氯水
C.濃硫酸
D.H2O2
(5)實驗室中常用CCl4從氧化后的溶液中萃取I2,其原理是 I2在CCl4中的溶解度遠大于I2在水中的溶解度I2在CCl4中的溶解度遠大于I2在水中的溶解度。
Ⅲ.某工廠采用如下步驟從海水中提取鎂:①把貝殼制成石灰乳;②在引入的海水中加入石灰乳,沉降,過濾,洗滌;③將沉淀物與鹽酸反應,蒸發結晶,過濾,得到含結晶水的晶體;④將所得晶體在一定條件下加熱得到無水氯化鎂;⑤電解熔融氯化鎂,得到金屬鎂。
(6)在以上提取鎂的過程中,沒有涉及的化學反應類型是 CC。
A.分解反應
B.化合反應
C.置換反應
D.復分解反應
(7)該過程中屬于氧化還原反應的化學方程式為 MgCl2 電解 Mg+Cl2↑MgCl2 電解 Mg+Cl2↑。
SO
2
-
4
SO
2
-
4
SO
2
-
4
CO
2
-
3
CO
2
-
3
電解
電解
【答案】BD;H++OH-=H2O、+2H+=H2O+CO2↑;引流;D;I2在CCl4中的溶解度遠大于I2在水中的溶解度;C;MgCl2 Mg+Cl2↑
CO
2
-
3
電解
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:20引用:2難度:0.7
相似題
-
1.為了除去KCl溶液中少量的MgCl2、MgSO4雜質,可選用Ba(OH)2溶液、稀鹽酸和K2CO3溶液三種試劑,按圖步驟操作:
溶液加過量A濾液加過量B操作Ⅰ加過量C較純凈的KCl溶液加熱煮沸
(1)寫出下列試劑的化學式:A,C
(2)根據題意,回答下列問題:
①加入過量A的目的是,
②加入過量B的目的是,
③加熱煮沸的目的是,
(3)操作Ⅰ的名稱是。發布:2024/12/14 8:0:2組卷:53引用:1難度:0.6 -
2.除去粗鹽中的雜質 CaCl2、MgCl2和 Na2SO4,過程如下:

下列有關說法中,不正確的是( )A.除去 Mg2+的主要反應:MgCl2+2NaOH-=Mg(OH)2↓+2NaCl B.試劑①一定不是Na2CO3溶液 C.檢驗 是否除凈:取少量濾液,加稀鹽酸酸化,再加 BaCl2溶液SO2-4D.濾液加稀鹽酸時只發生反應:HCl+NaOH=H2O+NaCl 發布:2024/12/30 4:0:1組卷:124引用:11難度:0.8 -
3.通過海水晾曬可得粗鹽,粗鹽除NaCl外,還含有MgCl2、CaCl2、Na2SO4以及泥沙等雜質,粗鹽精制的實驗流程如下。下列說法不正確的是( )

A.在第①步中使用玻璃棒攪拌可加速粗鹽溶解 B.第⑤步操作是過濾 C.在第②③④⑥步通過加入化學試劑除雜,加入試劑順序為:NaOH溶液→Na2CO3溶液→BaCl2溶液→稀鹽酸 D.除去MgCl2的離子方程式為:Mg2++2OH-=Mg(OH)2↓ 發布:2024/12/30 4:30:1組卷:91引用:5難度:0.8


