mg某雙原子分子的氣體在標準狀況下的體積為V1L,其摩爾質量為Mg/mol,將其溶于水(該氣體與水不反應)得到體積為V2L的溶液,NA表示阿伏加德羅常數的值,則下列錯誤的是( )
22 . 4 m V 1 |
N A V 1 22 . 4 |
m M V 2 |
V 1 22 . 4 V 2 |
【考點】物質的量與其濃度和氣體摩爾體積的綜合應用.
【答案】B
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/5/27 14:0:0組卷:608引用:4難度:0.7
相似題
-
1.(1)1.5NA個H3PO4的摩爾質量為
,含氧原子的物質的量為。
(2)amolH2SO4中含有b個氧原子,則阿伏加德羅常數可以表示為
(3)25.2gNa2RO3含Na+0.4mol,則Na2RO3的摩爾質量為,R的相對原子質量為。含R的質量為1.6g的Na2RO3,其物質的量為。
(4)相同條件下,比較下列物質中氫原子數目多少(填“>”“<”或“=”):
①4.9gH2SO43.6gH2O②1.6LCH42.4LH2發布:2024/4/20 14:35:0組卷:311引用:2難度:0.5 -
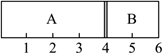 2.室溫下,某容積固定的密閉容器被可移動的活塞隔成A、B兩室(假設活塞質量和與容器的摩擦忽略不計),A中充入了一定量H2、O2的混合氣體,混合氣體的質量為34g;B中充入了1molN2,此時活塞的位置如圖所示。下列說法不正確的是( )
2.室溫下,某容積固定的密閉容器被可移動的活塞隔成A、B兩室(假設活塞質量和與容器的摩擦忽略不計),A中充入了一定量H2、O2的混合氣體,混合氣體的質量為34g;B中充入了1molN2,此時活塞的位置如圖所示。下列說法不正確的是( )A.A室混合氣體的物質的量為2mol B.A室中氧氣的質量為30g C.若將A室中H2、O2的混合氣體點燃引爆,恢復到反應前溫度,活塞最終停留在刻度3處 D.A室中氣體充分反應后恢復至室溫整個容器內氣體壓強與反應前氣體壓強之比為1:2 發布:2024/5/28 8:0:9組卷:52引用:2難度:0.6 -
3.(1)0.3 mol NH3 分子中所含質子數與
個H2O 分子中所含質子數相等。
(2)含 0.4 mol Al3+的Al2(SO4)3 中所含的 SO42-的物質的量是。
(3)已知 16 g A 和 20 g B 恰好完全反應生成 0.04 mol C 和 31.76 g D,則 C 的摩爾質量為。
(4)在反應 X+2Y=R+2M 中,已知 R 和 M 的相對分子質量之比為 22:9,當 1.6gX 與 Y 完全反應后,生成 4.4gR,則在此反應中Y 和 M 的質量比是發布:2024/6/27 10:35:59組卷:252引用:2難度:0.6


