酸、堿、鹽種類繁多,與人類日常生活和工農(nóng)業(yè)生產(chǎn)關(guān)系十分密切。
(1)稀鹽酸、稀硫酸、白醋都能使紫色石蕊溶液變紅,原因是它們的溶液中均含有 H+H+。(填離子符號)
(2)如圖是氫氧化鈉溶液與硫酸反應時溶液pH變化的示意圖。

①根據(jù)圖示判斷;該實驗是將 硫酸硫酸(填“氫氧化鈉溶液”或“硫酸”)滴加到另一種溶液中。
②滴入溶液體積為V2mL時,溶液中的溶質(zhì)為 Na2SO4、H2SO4Na2SO4、H2SO4。
(3)食鹽(主要成分是NaCl)除可用作調(diào)味品外,還是一種重要化工原料。晾曬海水所得到的粗鹽中含有不溶性雜質(zhì)(泥沙)和可溶性雜質(zhì)(CaCl2、MgCl2、Na2SO4);如圖是某化學小組在實驗室對粗鹽樣品進行除雜提純的過程。
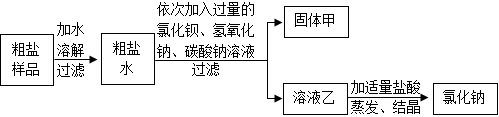
①溶解、過濾、蒸發(fā)操作中都要用到的一種玻璃儀器是 玻璃棒玻璃棒。
②加入Na2CO3溶液的作用是什么 除去溶液中的氯化鈣和過量的氯化鋇除去溶液中的氯化鈣和過量的氯化鋇。
③固體甲的成分有哪些 BaCO3、CaCO3、Mg(OH)2、BaSO4BaCO3、CaCO3、Mg(OH)2、BaSO4。(寫出化學式)
(4)為探究某瓶長期敞口放置的NaOH溶液中溶質(zhì)成分,某同學設計了如下方案:取少量溶液,加入足量Ca(OH)2溶液,反應后靜置,取上層清液滴加酚酞溶液。若溶液變紅,溶質(zhì)為Na2CO3和NaOH,請指出該方案中的錯誤并加以改正。
(5)LiOH和NaOH的化學性質(zhì)相似。“神舟”飛船內(nèi),可用盛有LiOH的過濾網(wǎng)吸收航天員呼出的氣體,以降低CO2含量。請計算;用LiOH完全吸收132gCO2,生成Li2CO3和H2O,理論上至少需要LiOH的質(zhì)量是多少?
【答案】H+;硫酸;Na2SO4、H2SO4;玻璃棒;除去溶液中的氯化鈣和過量的氯化鋇;BaCO3、CaCO3、Mg(OH)2、BaSO4
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:58引用:2難度:0.5
相似題
-
1.在“粗鹽的初步提純”實驗中,下列操作正確的是( )
A. 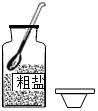
取用B. 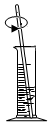
溶解C. 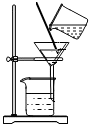
過濾D. 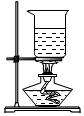
蒸發(fā)發(fā)布:2024/12/25 16:0:1組卷:136引用:3難度:0.7 -
2.多角度認識溶液,有助于我們更好地了解其在生產(chǎn)生活中的重要作用.
(1)物質(zhì)在水中的分散
①食鹽是重要的調(diào)味品,其主要成分氯化鈉是由構(gòu)成的(選填“分子”、“原子”或“離子”),將適量食鹽加入水中,充分攪拌后能形成溶液.
②食用油加入水中,充分攪拌能形成乳濁液.洗潔精洗滌油膩的碗筷是利用原理.
③面粉加入水中,充分攪拌后能形成懸濁液.除去懸濁液中難溶性的面粉可用的操作方法是.
(2)溶液的性質(zhì)
①關(guān)于溶液的說法正確的有(填標號).
A.鹽酸是純凈物 B.溶液是均一、穩(wěn)定的
C.溶液的酸堿度可用石蕊溶液測定 D.飽和溶液不一定是濃溶液
②有些固體物質(zhì)溶解形成溶液后會呈現(xiàn)不同的顏色,如品紅溶液是紅色的,放入活性炭可使紅色褪去,這利用活性炭的作用.
③a,b兩種物質(zhì)的溶解度曲線如圖1所示.下列說法正確的是
A.a(chǎn)物質(zhì)的溶解度一定大于b物質(zhì)的溶解度
B.將a溶液從t2℃時降溫到t1℃時,一定有晶體析出
C.t1℃時,a、b兩種物質(zhì)飽和溶液的溶質(zhì)質(zhì)量分數(shù)相等
D.將t2℃時b的飽和溶液變?yōu)椴伙柡腿芤海刹扇〗禍氐姆椒?br />(3)溶液的變化
將一定質(zhì)量的飽和氯化鈉溶液通電一段時間后,下列敘述正確的是
通電
(反應原理為:2NaCl+2H2O═2NaOH+H2↑+Cl2↑)
A.溶液的pH逐漸減小 B.溶液中鈉元素的質(zhì)量增大
C.溶液中氧元素的質(zhì)量分數(shù)不變 D.氯化鈉溶液的溶質(zhì)質(zhì)量分數(shù)減小
(4)如圖2是“粗鹽中難溶性雜質(zhì)的去除”的實驗操作示意圖:
①儀器a的名稱.
②操作A中托盤兩邊各放一張大小相同的紙片,其作用是.
③操作B中還需要用到的儀器是.
④操作 C過濾時倒入液體的液面要低于濾紙邊緣主要是為了防止(填字母).
A.過濾速度慢 B.濾紙破損 C.雜質(zhì)未經(jīng)過濾就進入濾液
⑤圖中部分操作有錯誤,其中有的錯誤會導致精鹽產(chǎn)率明顯偏低,其原因是.發(fā)布:2025/1/1 8:0:2組卷:55引用:1難度:0.5 -
 3.去除難溶性雜質(zhì)后的食鹽樣品中還含有可溶性雜質(zhì):CaCl2、MgCl2和Na2SO4.為除去可溶性雜質(zhì),將食鹽樣品溶于水,依次加入稍過量的三種溶液:BaCl2溶液、NaOH溶液、Na2CO3溶液。充分反應后過濾,得濾渣X,向濾液中加入過量的稀鹽酸,攪拌、煮沸,得氯化鈉溶液。下列說法正確的是( )
3.去除難溶性雜質(zhì)后的食鹽樣品中還含有可溶性雜質(zhì):CaCl2、MgCl2和Na2SO4.為除去可溶性雜質(zhì),將食鹽樣品溶于水,依次加入稍過量的三種溶液:BaCl2溶液、NaOH溶液、Na2CO3溶液。充分反應后過濾,得濾渣X,向濾液中加入過量的稀鹽酸,攪拌、煮沸,得氯化鈉溶液。下列說法正確的是( )A.濾渣X中有三種成分 B.“向濾液中加入過量的稀鹽酸”目的只是為了除去過量的NaOH C.除雜過程中有Na2CO3參加的化學反應為復分解反應 D.將氯化鈉溶液用題圖裝置加熱蒸發(fā),至水分完全蒸干時停止加熱 發(fā)布:2024/12/25 15:30:1組卷:741引用:8難度:0.5


