工業(yè)上可利用如下反應:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),既可以生產(chǎn)甲醇,又可以降低二氧化碳排放量。回答下列問題。
(1)若該反應在一定條件能自發(fā)進行,判斷該反應的ΔH <<0(填“<”或“>”)。
(2)寫出CH3OH中官能團的電子式 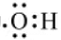
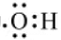 ,CO2的空間構型 直線形直線形。
,CO2的空間構型 直線形直線形。
(3)下列有關敘述正確的是 abab(填字母序號)。
a.容器內(nèi)氣體壓強不再發(fā)生改變時,該反應達到化學平衡狀態(tài)
b.從體系中不斷分離出甲醇可以能提高CO2的平衡轉(zhuǎn)化率
c.向容器內(nèi)通入少量氦氣,則平衡向正反應方向移動
d.升溫時,該反應的平衡常數(shù)增大
(4)當起始物n(H2)n(CO2)=3時,在不同條件下達到平衡,設體系中甲醇的物質(zhì)的量分數(shù)為x(CH3OH),如圖表示的是250℃下x(CH3OH)與壓強關系曲線和壓強為5×105Pa下x(CH3OH)與溫度關系曲線。
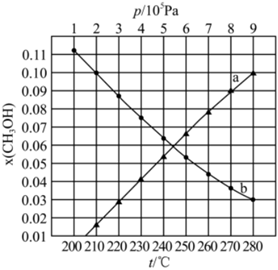
①表示250℃下x(CH3OH)與壓強關系曲線的是 曲線a曲線a(填“曲線a”或“曲線b”)。
②當CO2的平衡轉(zhuǎn)化率為13時,反應條件可能是 9×105Pa、250℃或5×105Pa,210℃9×105Pa、250℃或5×105Pa,210℃。
(5)某科研機構利用CO2的弱氧化性開發(fā)了丙烷氧化脫氫制丙烯的新工藝,該工藝采用鉻的氧化物作催化劑,其反應機理如圖。
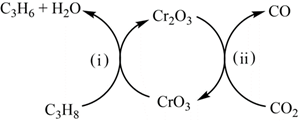
寫出第Ⅱ步的化學方程式 Cr2O3+3CO2=2CrO3+3COCr2O3+3CO2=2CrO3+3CO,該工藝采用的催化劑為 CrO3CrO3。
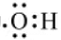
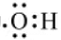
n
(
H
2
)
n
(
CO
2
)
1
3
【答案】<;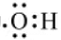 ;直線形;ab;曲線a;9×105Pa、250℃或5×105Pa,210℃;Cr2O3+3CO2=2CrO3+3CO;CrO3
;直線形;ab;曲線a;9×105Pa、250℃或5×105Pa,210℃;Cr2O3+3CO2=2CrO3+3CO;CrO3
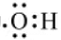 ;直線形;ab;曲線a;9×105Pa、250℃或5×105Pa,210℃;Cr2O3+3CO2=2CrO3+3CO;CrO3
;直線形;ab;曲線a;9×105Pa、250℃或5×105Pa,210℃;Cr2O3+3CO2=2CrO3+3CO;CrO3【解答】
【點評】
聲明:本試題解析著作權屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:26引用:1難度:0.5
相似題
-
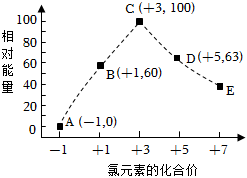 1.一定條件下,在水溶液中物質(zhì)的量均為1mol的Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相對大小如圖所示。圖中最穩(wěn)定的點為( )
1.一定條件下,在水溶液中物質(zhì)的量均為1mol的Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相對大小如圖所示。圖中最穩(wěn)定的點為( )A.A B.B C.C D.D 發(fā)布:2025/1/6 6:0:5組卷:0引用:1難度:0.9 -
2.下列與化學反應的能量變化有關的敘述正確的是( )
A.由石墨比金剛石穩(wěn)定可知,C(金剛石)═C(石墨)△H<0 B.一個反應的反應物的總能量可能等于其生成物的總能量 C.有熱量變化的反應一定是化學反應 D.強酸與強堿的中和反應的熱化學方程式均可表示為H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ?mol-1 發(fā)布:2025/1/6 6:0:5組卷:1引用:3難度:0.6 -
3.下列說法不正確的是( )
A.CH3COOH 溶液加水稀釋后,溶液中 的值減小c(CH3COOH)c(CH3COO-)B.已知一定溫度下,醋酸溶液的物質(zhì)的量濃度為c,電離度為α,Ka= .若加入少量醋酸鈉固體,則CH3COOH?CH3COO-+H+向左移動,α減小,Ka變小(cα)2c(1-α)C.實驗測得環(huán)己烷(l)、環(huán)己烯(l)和苯(l)的標準燃燒熱分別為-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以證明在苯分子中不存在獨立的碳碳雙鍵 D.已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g),△H=+489.0 kJ/mol.
CO(g)+O2(g)═CO2(g),△H=-283.0 kJ/mol.12
C(石墨)+O2(g)═CO2(g),△H=-393.5 kJ/mol.
則4Fe(s)+3O2(g)═2Fe2O3(s),△H=-1641.0 kJ/mol發(fā)布:2025/1/1 8:0:2組卷:11引用:1難度:0.7


