下表是碳酸鈉、氯化鈉的部分溶解度數據。
| 溫度/℃ | 20 | 30 | 40 | 50 | 60 | 80 | 100 | |
| 溶解度(g/100g水) | 碳酸鈉 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 | 45.1 | 44.7 |
| 氯化鈉 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 38.4 | 39.8 | |
48.8g
48.8g
。(2)碳酸鈉與氯化鈉的溶解度相等的溫度范圍是
20℃<t℃<30℃
20℃<t℃<30℃
。(3)20℃時,在100g水中進行如下實驗。
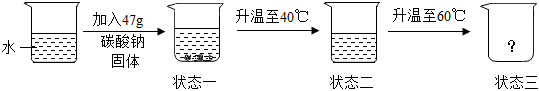
為了使狀態二中的溶液達到飽和,至少需再加入
1.8
1.8
g碳酸鈉;再升溫至60℃時,狀態三的燒杯中會出現的現象是 有固體析出
有固體析出
。(4)20℃時,向含有100g水的Na2CO3溶液中加入一定量的CaCl2固體,反應的化學方程式是
CaCl2+Na2CO3=CaCO3↓+2NaCl
CaCl2+Na2CO3=CaCO3↓+2NaCl
。如圖表示兩種生成物的質量與加入CaCl2的質量的變化關系,其中曲線b表示的生成物是 碳酸鈣
碳酸鈣
(填名稱)。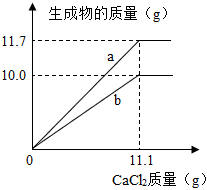
請結合相關數據分析說明:20℃時,Na2CO3溶液是否為飽和溶液
與11.1gCaCl2恰好完全反應的Na2CO3質量只有10.6g,而20℃時,100g水中最多能溶解21.8gNa2CO3,所以該溶液為不飽和溶液
與11.1gCaCl2恰好完全反應的Na2CO3質量只有10.6g,而20℃時,100g水中最多能溶解21.8gNa2CO3,所以該溶液為不飽和溶液
。【答案】48.8g;20℃<t℃<30℃;1.8;有固體析出;CaCl2+Na2CO3=CaCO3↓+2NaCl;碳酸鈣;與11.1gCaCl2恰好完全反應的Na2CO3質量只有10.6g,而20℃時,100g水中最多能溶解21.8gNa2CO3,所以該溶液為不飽和溶液
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/7/2 8:0:9組卷:55引用:2難度:0.5
相似題
-
1.Na2CO3俗稱純堿,NaOH俗稱燒堿,它們都是白色粉末。請回答下列問題。
(1)能區別Na2CO3和NaOH兩種溶液的方法是(填序號)。
①加入澄清石灰水
②加入食鹽水
③滴入無色酚酞溶液
④加入稀鹽酸
(2)敞口放置的燒堿會吸收空氣中的而變質,反應的化學方程式為。要檢驗NaOH是否變質,可選用的方法是。 (填序號)
①加入澄清石灰水
②加入氯化鈣溶液
③滴入無色酚酞溶液
④加入稀鹽酸
(3)純堿可與CO2和H2O反應生成NaHCO3,該反應的化學方程式為,Na2CO3與稀鹽酸反應放出CO2,但實驗室卻不用這個反應制取CO2,其主要原因可能是;已知在某溫度下,Na2CO3的溶解度比NaHCO3大,則該溫度時,向飽和Na2CO3溶液中連續通入CO2,可觀察到的現象是。發布:2025/1/3 8:0:1組卷:4引用:2難度:0.5 -
2.蛋白質是組成細胞的基礎物質,沒有蛋白質就沒有生命.人體內的血紅蛋白、各種酶都是蛋白質.一些可溶性的重金屬鹽(如Cu2+、Ba2+、Ag+等的可溶性鹽)與蛋白質作用會使蛋白質凝固變性,從而喪失其生理功能危及生命.因此,可溶性重金屬鹽為有毒物質,根據上述所給知識,用化學式回答下列問題:
(1)CuSO4、AgNO3、Ba(NO3)2、AgCl四種物質中,無毒的是;
(2)在醫療上用X射線檢查胃腸疾病時,讓病人服用硫酸鋇的懸濁液(俗稱鋇餐),而不能服用碳酸鋇,其原因是人體胃液中含有一定量的,與碳酸鋇反應后,產生了一定量的使人中毒的氯化鋇,其反應的化學方程式是.
(3)若因氯化鋇中毒,下列方案中可作為最佳解毒措施的是(填序號).
A、多飲糖水;B、飲用純堿溶液;C、飲用食鹽水;D、飲用硫酸鈉溶液.發布:2024/12/25 17:30:2組卷:48引用:17難度:0.7 -
3.下列物質不能與氯化鋇溶液發生反應的是( )
A.硫酸銅 B.硝酸銀 C.氯化鈣 D.碳酸鈉 發布:2024/12/25 17:0:2組卷:68引用:3難度:0.5


