大氣中的CO2含量不斷上升,導致溫室效應增強,全球氣候變暖。黨的二十大報告再次強調了“雙碳目標”。
Ⅰ.下列燃料的過度使用不會造成溫室效應增強的是 dd。(填字母)
a.煤
b.石油
c.天然氣
d.氫氣
Ⅱ.將CO2作為資源是實現碳中和的有效方法。CO2與H2在催化條件下反應生成甲醇。反應的化學方程式為CO2+3H2 催化劑 CH3OH+X,X的化學式為 H2OH2O。
Ⅲ.“碳捕捉和封存”技術是實現碳中和的重要途徑之一。
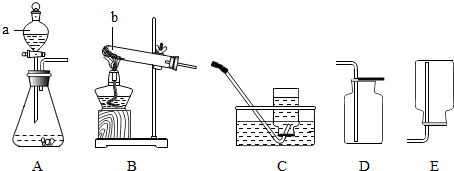
(1)某實驗小組的同學在實驗室利用如圖A~E裝置制取純凈、干燥的CO2。

①實驗室用A裝置制取CO2的化學方程式為 CaCO3+2HCl═CaCl2+H2O+CO2↑CaCO3+2HCl═CaCl2+H2O+CO2↑。
②為達到實驗目的,所選用裝置的導管接口從左到右正確的連接順序為a接 cc(填字母,下同)、bb接 ee、dd接 ff。
③同學們用F裝置“捕捉”CO2,先關閉彈簧夾,將濃NaOH溶液滴入試管中,充分反應后,再打開彈簧夾,可觀察到的現象是 氯化鈣溶液進入左側試管中,并產生白色沉淀氯化鈣溶液進入左側試管中,并產生白色沉淀;寫出“捕捉”CO2反應的化學方程式:2NaOH+CO2=Na2CO3+H2O2NaOH+CO2=Na2CO3+H2O。
(2)從分子的角度解釋CO2可以通過壓縮封存的原因:分子間存在著間隔,壓強增大時分子間的間隔減小分子間存在著間隔,壓強增大時分子間的間隔減小。
(3)石灰石循環法可用來捕捉煙氣中的CO2,該方法是用高溫煅燒石灰石生成的CaO來捕捉CO2。某化工廠使用含雜質的石灰石樣品12t,充分高溫煅燒后制備出了5.6tCaO,則該石灰石中碳酸鈣的質量分數是多少?(計算結果精確到0.1%)
催化劑
【答案】d;H2O;CaCO3+2HCl═CaCl2+H2O+CO2↑;c;b;e;d;f;氯化鈣溶液進入左側試管中,并產生白色沉淀;2NaOH+CO2=Na2CO3+H2O;分子間存在著間隔,壓強增大時分子間的間隔減小
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/23 12:26:7組卷:32引用:1難度:0.6
相似題
-
1.通過半年的化學學習,你已經掌握了實驗室制取氣體的有關規律,以下是老師提供的一些實驗裝置。請結合圖回答問題
(1)寫出圖中標號的儀器名稱:b。
(2)寫出實驗室用A裝置制取CO2的化學方程式。
(3)通過查閱資料得知:①氨氣(NH3)是一種密度比空氣小且極易溶于水的氣體,其水溶液稱為氨水,氨水能使無色酚酞變紅;②氨氣在加熱條件下能與氧化銅反應生成銅、水和空氣中含量最多的氣體。小芳同學加熱氯化銨和氫氧化鈣的固體混合物制取氨氣,她應選擇的反應的發生裝置是,收集裝置是(填字母編號)。
(4)小芳將收集滿氨氣的集氣瓶倒扣在滴有無色酚酞的水中,觀察到的現象是,。
(5)請寫出氨氣和氧化銅反應的化學方程式。發布:2024/11/5 8:0:2組卷:138引用:1難度:0.4


