2023年天津市耀華中學高考化學一模試卷
發布:2024/5/17 8:0:8
選擇題
-
1.實現中國夢,離不開化學與科技的發展,下列有關說法錯誤的是( )
A.我國“天眼”的球面射電板上使用的鋁合金板屬于金屬材料 B.華為公司自主研發的“麒麟9000”芯片的主要成分是單質硅 C.新能源汽車電池使用的石墨烯電極材料屬于有機高分子化合物 D.“神舟十四號”宇宙飛船返回艙表層材料中的玻璃纖維屬于無機非金屬材料 組卷:160引用:5難度:0.7 -
2.我國發布了《醫用同位素中長期發展規劃(2021-2035年)》,對提升醫用同位素相關產業能力水平、保障健康中國戰略實施具有重要意義。醫用同位素有14C、18F、131I、60Co等,有關說法不正確的是( )
A.60Co位于元素周期表的第四周期第Ⅷ族 B.18F和131I的最外層電子數相同 C.14C與12C的化學性質幾乎相同 D.化合物23Na18F的中子總數為41 組卷:103引用:2難度:0.7 -
3.下列化學用語表示正確的是( )
A.鎂原子的結構示意圖: 
B.2-丁烯的鍵線式: 
C.鄰羥基苯甲醛分子內氫鍵: 
D.乙烯的空間填充模型:  組卷:108引用:1難度:0.5
組卷:108引用:1難度:0.5 -
4.下列實驗操作設計正確且能達到實驗目的的是( )

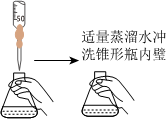
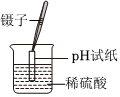
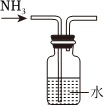
A.演示噴泉實驗 B.滴定實驗中用標準堿液滴定鹽酸接近滴定終點的操作 C.測稀硫酸的pH D.制備氨水 A.A B.B C.C D.D 組卷:222引用:5難度:0.8 -
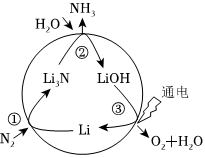 5.固氮是將游離態的氮轉變為氮的化合物,一種新型人工固氮的原理如圖所示。下列敘述正確的是( )
5.固氮是將游離態的氮轉變為氮的化合物,一種新型人工固氮的原理如圖所示。下列敘述正確的是( )A.轉化過程中所涉及的元素均呈現了兩種價態 B.反應①②③均為氧化還原反應 C.Li是催化劑,只有Li3N是中間產物 D.整個過程的總反應可表示為2N2+6H2O 4NH3+3O2催化劑組卷:182引用:3難度:0.7
-
15.已知甲酸銅是一種重要的化工原料,常溫常壓下穩定,可溶于水,難溶于乙醇,具有還原性,某實驗小組在實驗室用廢銅屑制備甲酸銅晶體Cu(HCOO)2?4H2O,實驗流程如圖:

回答下列問題:
(1)若甲同學設計方案:銅屑、稀硫酸加熱通入氧氣制得硫酸銅溶液,再與甲酸反應生成甲酸銅溶液,再結晶。請判斷:甲同學(填“能”或“不能”)制得甲酸銅晶體。
(2)步驟Ⅱ制備Cu(OH)2?CuCO3時,寫出CuSO4和NaHCO3物質的量之比為1:2時的離子方程式:。
(3)操作步驟Ⅲ:向盛Cu(OH)2?CuCO3燒杯中加入一定量熱蒸餾水,逐滴加入甲酸至固體恰好全部溶解,然后除去少量不溶性雜質,過程中為了防止甲酸銅結晶損失,可采取操作;接著冷卻結晶,過濾,再洗滌晶體2~3次,為使固體快速干燥,可選(填寫序號)來洗滌。得到產品。
A.冷水
B.乙醇
C.四氯化碳
D.飽和甲酸銅溶液
(4)晶體中甲酸根含量的測定: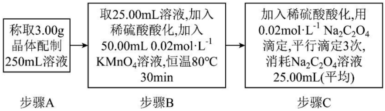
①下列儀器可供步驟A選用的是(寫名稱,下同);可供步驟C中滴定選用的是。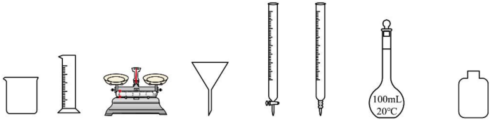
②溶液恒溫80℃30min時應采取的操作方法是,步驟C滴定時當觀察到即達到滴定終點。
③計算晶體中甲酸根的質量分數為。組卷:77引用:1難度:0.3 -
16.溴代烷的制備,分“氧化”和“溴化”兩個過程,回答下列問題。
(1)氧化過程:HBr(g)與O2(g)在合適溫度下制備Br2(g)。
已知:T℃時,相關物質的相對能量如下表所示:
此溫度下,在恒容密閉容器中充入4molHBr(g)和1molO2(g),測得反應物的平衡轉化率為60%。若保持其他條件不變,改為絕熱狀態,平衡時,測得放出熱量為QkJ,則下列關系正確的是物質 HBr(g) O2(g) H2O(g) Br2(g) 相對能量/kJ?mol-1 x y z w (填標號)。
A.Q=0.6(2z+2w-4x-y)
B.Q<0.6(2z+2w-4x-y)
C.Q<0.6(4x+y-2z-2w)
D.0.6(4x+y-2z-2w)<Q<4x+y-2z-2w
(2)溴化過程:在T℃下,向10V0L容器中投入初始濃度均為0.1mol?L-1的Br2(g)和CH4(g),發生反應:Br2(g)+CH4(g)?CH3Br(g)+HBr(g)。保持溫度不變,壓縮容器體積,分別測得不同容積下CH3Br(g)的平衡濃度如下表:
當容器體積從10V0L縮小到3V0L時,測得此時容器內仍有四種氣態組分,則m=容器體積V/L 10V0 3V0 V0 c(CH3Br)/mol?L-1 m 0.09 0.25 ;容器體積縮小到V0L時,平衡移動(填“正向”、“逆向”或“不”)。T℃時,此反應在容積為10V0L和V0L時化學平衡常數分別為K1、K2,則K1K2(填“大于”、“小于”或“等于”)。
(3)新工藝可將甲烴、HBr和O2混合,直接催化“氧化溴化”:2CH4(g)+2HBr(g)+O2(g)?2CH3Br(g)+2H2O(g)ΔH<0。反應起始物料n(CH4)、n(HBr)、n(O2)分別為2mol、2mol、1mol時,在不同條件下達到平衡,設體系中CH3Br的物質的量分數為x(CH3Br),在T為500℃下的x(CH3Br)~p、在p為3×105Pa下的x(CH3Br)~T如圖所示: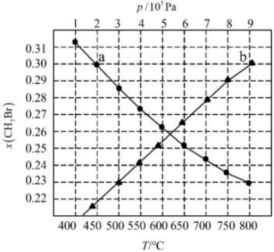
①圖中a點對應的反應條件為,此時用各物質平衡分壓表示的平衡常數Kp=Pa-1(列計算式,某氣體分壓=總壓×該氣體的物質的量百分數)。
②b點對應的甲烷轉化率α(CH4)=(保留三位有效數字)。組卷:72引用:1難度:0.6


