2023年遼寧省沈陽市中考化學一模試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題(共15分)
-
1.下列自然資源的利用過程中,發(fā)生了化學變化的是( )
A.礦石粉碎 B.風力發(fā)電 C.糧食釀酒 D.撒網捕魚 組卷:29引用:1難度:0.8 -
2.沈陽的清水大米外形晶瑩剔透,香味持久。大米富含的主要營養(yǎng)成分是( )
A.糖類 B.蛋白質 C.油脂 D.維生素 組卷:26引用:1難度:0.8 -
3.富硒大米中的“硒”是指( )
A.原子 B.分子 C.單質 D.元素 組卷:66引用:7難度:0.9 -
4.下列物質能為學校種植的花草提供氮肥的是( )
A.K2CO3 B.NH4Cl C.Na2SO4 D.Ca3(PO4)2 組卷:38引用:1難度:0.8 -
5.下列實驗操作正確的是( )
A. 
滴加液體B. 
量取液體C. 
聞氣體氣味D. 
干燥氫氣組卷:22引用:1難度:0.7 -
6.下列試劑可以用來除鐵銹的是( )
A.純堿溶液 B.濃食鹽水 C.植物油 D.稀鹽酸 組卷:59引用:2難度:0.5
二、非選擇題(共50分)
-
18.金屬和材料的利用和發(fā)展推動人類進步,與化學密不可分。
(1)人類制得并利用金屬有著悠久的歷史: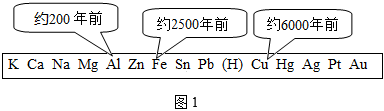 根據如圖,人類開始利用銅、鐵、鋁三種金屬的年代先后順序與 有關。
根據如圖,人類開始利用銅、鐵、鋁三種金屬的年代先后順序與 有關。
(2)工業(yè)上電解氧化鋁制取金屬鋁的化學方程式是:2Al2O34Al+3O2↑,該反應屬于通電反應。現電解10t氧化鋁最多可生產鋁的質量是t(精確到0.1t)。
(3)實驗室模擬煉鐵原理的裝置如圖2所示,請回答下列問題: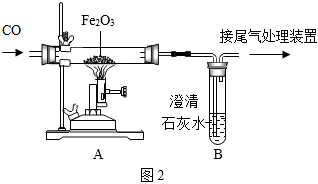
①寫出A裝置中發(fā)生反應的化學方程式。
②實驗結束后,B裝置中的液體倒吸入A裝置的玻璃管中,造成這一問題的原因是。
③實驗中擬采用如下方法處理尾氣:
A.酒精燈點燃
B.排水法收集
C.氣球收集
請任選以上三種方法中的一種,分別從優(yōu)、缺點兩方面進行評價。
(4)某化學小組利用濕法煉銅的原理展開如下探究:
【提出問題】市場上有還原鐵粉和納米鐵粉兩種鐵粉,如何選擇?
【實驗探究】還原鐵粉:價格30元/500g 納米鐵粉:價格300元/500g
①取兩只規(guī)格相同的燒杯,分別加入1.5gCuSO4粉末,室溫下配制成CuSO4飽和溶液。
②向CuSO4飽和溶液中分別加入恰好完全反應所需質量的還原鐵粉和納米鐵粉,靜置一段時間,使其充分反應。
③經檢驗,鐵粉已完全反應,然后過濾、洗滌,并將所得固體置于陰涼處干燥。
④分別稱量獲得固體的質量。
【獲得數據】
【問題分析】初始物質 理論生成銅的質量/g 實際生成銅的質量/g 產率 CuSO4溶液+還原鐵粉 0.60 0.58 96.67% CuSO4溶液+納米鐵粉 0.60 0.56 93.33%
①濕法煉銅的原理是(用化學方程式表示)。
②上述步驟③中檢驗鐵粉完全反應的操作方法是。
【得出結論】
③由上述探究活動可知:在濕法煉銅中應選用還原鐵粉,理由是。組卷:102引用:1難度:0.5 -
19.項目式學習是一類重要的學習活動,深受同學們喜愛。某學習小組的同學們開展了通過從粗鹽中提純氯化鈉、并按需求制成不同功能的食用鹽這一項目式學習活動。
【設計實施】經過研討,同學們設計了三個具體任務,并加以實施:
任務一:除去粗鹽中的泥沙
(1)小組同學稱取了5g粗鹽(主要成分是氯化鈉,還含有氯化鎂、泥沙),按照如下步驟進行實驗: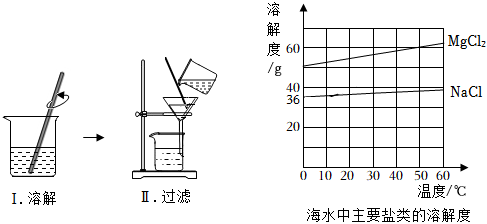
①步驟Ⅰ:為加速固體溶解,可采用的方法是(寫一種即可)。
②步驟Ⅱ:過濾后濾紙上留下的是。
③從節(jié)約能源和提高產率的角度分析,將5g粗鹽充分溶解所需水的體積比較適合的是。(實驗環(huán)境溫度為20℃,水的密度為1g/mL)
A.10mL
B.14mL
C.100mL
任務二:除去濾液中的氯化鎂
(2)根據粗鹽中氯化鈉質量分數約為80%~90%,以及溶解度曲線的比較,小組同學決定采用方法除去濾液中的氯化鎂。但在結晶的過程中一定要趁熱過濾,你認為這樣做的目的是。
【分析交流】
(3)檢驗分離效果:怎樣證明氯化鎂是否除盡?
查閱相關資料:部分酸、堿、鹽的溶解性表(室溫)
(溶:該物質可溶于水;不:該物質不溶于水)陰離子
陽離子OH- NO-3Cl- SO2-4Na+ 溶 溶 溶 溶 Mg2+ 不 溶 溶 溶
請用溶解性表中提供的物質完成以下實驗:
任務三:自制食用鹽實驗步驟 實驗現象 實驗結論 取上述過濾后的少量固體置于試管,加水至完全溶解,然后加入 溶液,觀察現象氯化鎂已除盡
(4)小組同學將超市里售賣的兩種食用鹽的標簽做了對比,如表:
表:沈陽超市中常見的加碘精制鹽和低鈉湖鹽成分配料表
①小組同學想比較一下兩種食用鹽的咸度,下列哪一種方法更科學種類 NaCl(g/100g) KCl(g/100g) KIO3(以I計)(mg/100g) 適宜人群 加碘精制鹽 ≥99.1 0 18~33 大多數 低鈉湖鹽 60~80 20-40 21-39 特別適合高血壓患者 (填字母序號)。
A.用舌尖蘸少量鹽品嘗
B.取等體積水,加入等質量的鹽,完全溶解后再品嘗
C.不用嘗,鹽都有咸味
②根據配料表的成分,小組同學發(fā)現低鈉鹽主要就是在氯化鈉中加入來降低鈉元素含量。從其功能看,低鈉鹽主要是面向群體。
【反思評價】
小組同學通過其他途徑獲得了高純度KCl和KIO3,按照配料表中的物質配比稱量、混合、研磨,較順利制得了精制鹽和低鈉鹽。但在市場調查時,也看到其他功能和配料方法的食鹽,有待繼續(xù)探究……組卷:144引用:1難度:0.4


