2021-2022學年四川省眉山市仁壽二中高一(上)第四次質(zhì)檢化學試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題(本題共21小題,每小題0分,共42分)
-
1.化學研究最重要的方法是( )
A.觀察法 B.實驗法 C.推理法 D.計算法 組卷:35引用:2難度:0.8 -
2.化學與生產(chǎn)、生活及社會發(fā)展密切相關(guān)。下列有關(guān)說法錯誤的是( )
A.司母戊鼎、飛機外殼和石灰石均屬于合金 B.高純度的硅單質(zhì)廣泛用于制作半導體材料和太陽能電池 C.鐵鹽和鋁鹽均可用于凈水 D.利用焰色反應可制成節(jié)日煙花 組卷:7引用:2難度:0.7 -
3.國家衛(wèi)健委公布的新型冠狀病毒肺炎診療方案指出,乙醚、75%乙醇、含氯消毒劑、過氧乙酸(CH3COOOH)、氯仿(CHCl3)等均可有效滅活病毒。對于上述有關(guān)藥品,下列說法錯誤的是( )
A.乙醇能與水以任意比例互溶 B.NaClO通過氧化滅活病毒 C.過氧乙酸摩爾質(zhì)量為76 D.乙醚和氯仿均有毒,使用時應注意防護 組卷:169引用:2難度:0.8 -
4.下列有關(guān)實驗操作的說法正確的是( )
A.用容量瓶配制溶液時,搖勻后發(fā)現(xiàn)液面低于刻度線,立即加水至刻度線 B.進行分液操作時,先從分液漏斗上口倒出上層液體,后通過下端活塞放出下層液體 C.往沸水中滴加飽和氯化鐵溶液制備氫氧化鐵膠體時,要邊滴溶液邊攪拌防止溶液飛濺 D.蒸餾時溫度計水銀球應位于蒸餾燒瓶支管口處 組卷:6引用:3難度:0.5 -
5.下列敘述正確的是( )
A.溶液和膠體的本質(zhì)區(qū)別是能否產(chǎn)生丁達爾效應 B.鹵水點豆腐和靜電除塵都應用了膠體聚沉的性質(zhì) C.合金的熔點一般比組成成分的金屬熔點低 D.樹狀分類法是唯一能表示物質(zhì)分類的方法 組卷:5引用:2難度:0.8 -
6.下列組合正確的是( )
純凈物 混合物 電解質(zhì) 非電解質(zhì) A 氯水 水煤氣 NaCl 酒精 B 氫氧化鋇 冰水混合物 冰醋酸 硫酸鋇 C 膽礬 石灰水 KOH 二氧化碳 D 硫酸 碳素鋼 鹽酸 氮氣 A.A B.B C.C D.D 組卷:50引用:4難度:0.6 -
7.下列實驗裝置或操作與粒子的大小無直接關(guān)系的是( )
A. 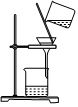
過濾B. 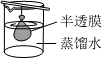 滲析
滲析C. 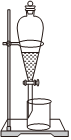
萃取D. 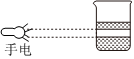
丁達爾效應組卷:79引用:16難度:0.9 -
8.某國外化學教材中有一張關(guān)于氧化還原反應的插圖(如圖所示),由圖可知
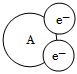 在該反應中( )
在該反應中( )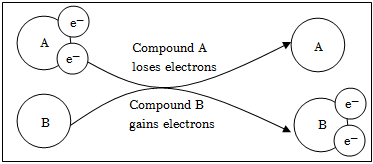
A.作氧化劑 B.被氧化 C.發(fā)生還原反應 D.是還原產(chǎn)物 組卷:20引用:2難度:0.8
二、非選擇題(本大題共包括4個小題,共58分)
-
24.鐵及其化合物在生產(chǎn)、生活中有著廣泛的應用。
(1)鋼(一種鐵碳合金)是用量最大、用途最廣的合金。鋼的硬度比純鐵。(填“大”或“小”)
(2)高鐵酸鉀(K2FeO4)是一種新型高效、無毒的多功能水處理劑,K2FeO4中Fe的化合價為。
(3)若一定量的普通鐵粉和水蒸氣在高溫下反應生成44.8LH2(標準狀況),則轉(zhuǎn)移電子的物質(zhì)的量為mol。
(4)FeSO4可作補血劑,用于治療缺鐵性貧血癥。用FeSO4溶液制備Fe(OH)2的操作是用長滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再擠出NaOH溶液。這樣操作的目的是。
(5)印刷電路板是由高分子材料和銅箔復合而成,刻制印刷電路時,要用FeCl3溶液作為“腐蝕液”,該反應的離子方程式為,檢驗反應后的溶液中是否還有三價鐵離子的試劑是。
(6)聚硅酸鐵是目前無機高分子絮凝劑研究的熱點,一種用鋼管廠的廢鐵渣(主要成分Fe3O4,含少量碳及二氧化硅)為原料制備的流程如圖。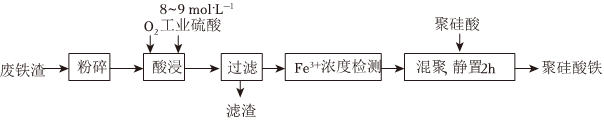
①加熱條件下酸浸時,F(xiàn)e3O4與硫酸反應的化學方程式為。
②酸浸時,通入O2的目的是。
③“Fe3+濃度檢測”是先用SnCl2將Fe3+還原為Fe2+,再用酸性K2Cr2O7,標準溶液測定Fe2+的量(Cr2O72-被還原為Cr3+),則SnCl2、Fe2+和Cr3+三者中還原性最強的是。組卷:65引用:2難度:0.3 -
25.氮氧化合物和二氧化硫是引起霧霾重要物質(zhì),工業(yè)用多種方法來治理。某種綜合處理含
廢水和工業(yè)廢氣(主要含NO、CO、CO2、SO2、N2)的流程如圖。NH+4
已知:NO+NO2+2NaOH═2NaNO2+H2O;2NO2+2NaOH═NaNO3+NaNO2+H2O
(1)NO是色的氣體,(填“易”或“難”)溶于水;NO在空氣中很容易被氧化成NO2,NO2能與水發(fā)生化學反應,寫出NO2與水反應的化學方程式為。
(2)SO2造成的一種常見的環(huán)境污染為。
(3)固體1的主要成分有Ca(OH)2、。(填化學式)
(4)用NaNO2溶液處理含廢水反應的離子方程式為NH+4。
(5)驗證廢水中已基本除凈的方法是NH+4。(寫出操作現(xiàn)象與結(jié)論)
(6)捕獲劑捕獲的氣體主要是。(填化學式)
(7)流程中生成的NaNO2因外觀和食鹽相似,又有咸味,容易使人誤食中毒。已知NaNO2能發(fā)生如下反應:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O,I2可以使淀粉溶液變藍。根據(jù)上述反應,選擇生活中常見的物質(zhì)和有關(guān)試劑進行實驗,以鑒別NaNO2和NaCl固體。需選用的物質(zhì)是。(填序號)
①水
②淀粉碘化鉀試紙
③淀粉
④白酒
⑤白醋組卷:53引用:3難度:0.5


