2023-2024學年遼寧省沈陽二中高三(上)開學化學試卷
發布:2024/8/28 0:0:8
一、選擇題(本題包括15小題,每小題3分,共45分,每小題只有1個選項符合題意)
-
1.下列“類比”、“推理”合理的是( )
A.Fe與Cl2反應生成FeCl3,則Fe與I2反應生成FeI3 B.CaO與CO2反應生成CaCO3,CuO與CO2反應生成CuCO3 C.在Na2O2與水反應后的溶液中加入MnO2粉末,會產生大量氣體,該氣體能使帶火星的木條復燃,則可推測Na2O2與水反應有中間產物H2O2生成 D.Na與水反應生成NaOH和H2,則Fe與水蒸氣反應生成Fe(OH)3和H2 組卷:23引用:2難度:0.6 -
2.84消毒液可用于新型冠狀病毒的消殺,其有效成分為NaClO。NaClO在空氣中可發生反應NaClO+CO2+H2O═NaHCO3+HClO。用化學用語表示的相關微粒,正確的是( )
A.中子數為10的氧原子: O108B.Na+的結構示意圖: 
C.CO2的結構式:O=C=O D.NaClO的電子式:  組卷:31引用:2難度:0.8
組卷:31引用:2難度:0.8 -
3.用NA代表阿伏加德羅常數的值,下列說法正確的是( )
A.50mL12mol/L鹽酸與足量MnO2共熱,轉移的電子數為0.15NA B.足量鐵在1molCl2中充分燃燒,反應轉移的電子數為3NA C.Al3++4OH-= +2H2O,說明1molAl(OH)3電離出H+數為NAAlO-2D.常溫常壓下,78gNa2O2中含有的陰離子數為NA 組卷:31引用:1難度:0.8 -
4.下列物質性質和用途都正確且相關的是( )
選項 性質或組成 用途或物質類別 A FeCl3溶液顯酸性 用于刻蝕電路板 B SO2具有氧化性 SO2常用于漂白秸稈、織物 C HF溶液具有酸性 HF溶液能在玻璃上刻圖案 D 陶瓷中雖然一般含金屬元素 但陶瓷屬于無機非金屬材料 A.A B.B C.C D.D 組卷:11引用:1難度:0.7 -
5.下列有關圖象的說法正確的是( )
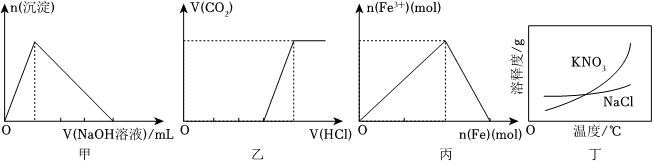
A.圖甲表示:向某明礬溶液中逐滴加入NaOH溶液至過量,生成沉淀的物質的量與滴加NaOH溶液體積的關系 B.圖乙表示:向含等物質的量的NaOH和Na2CO3的混合溶液中逐滴加入稀鹽酸至過量,生成氣體的體積與滴加HCl溶液體積的關系 C.圖丙表示:在稀硝酸溶液中逐漸加入鐵粉至過量,溶液中Fe3+物質的量與逐漸加入鐵粉物質的量的變化關系 D.根據圖丁,除去混在KNO3中少量的NaCl可用“蒸發濃縮,趁熱過濾”的方法 組卷:98引用:4難度:0.6 -
6.下列實驗裝置、操作正確,且能實現相應實驗目的的是( )
實驗裝置 實驗操作 實驗目的 A 
用標準KMNO4溶液滴定Na2S2O3溶液 測定Na2S2O3溶液濃度 B 
蒸發AlCl3溶液 得到AlCl3固體 C 
逐滴滴加AgNO3溶液 根據沉淀產生的先后順序確定Ksp(AgCl)和Ksp(AgI)的大小 D 
加熱NH4Cl固體 制備NH3 A.A B.B C.C D.D 組卷:46引用:2難度:0.5
二、填空題
-
18.納米級MoS2復合材料被認為是一種理想的鈉離子電池負極材料,以鉬精礦[主要成分MoS2,以及SiO2、CaO、Fe、Cu、Ca3Fe2(SiO4)3等雜質]為原料生產納米級MoS2的工業流程如圖:

已知:i.MoS2不溶于水和常見的酸堿,“燒熔”時可轉化為酸性氧化物MoO3;
ii.Ca3Fe2(SiO4)3經“燒熔”后可與沸鹽酸反應。
(1)“粉碎”的目的為
(2)濾液②中含有的金屬離子為;濾渣②的成分為。
(3)“堿浸”時發生反應的化學方程式為;用NaOH溶液代替氨水的不足之處為。
(4)已知“硫代”一步生成了,則“沉鉬”中加入鹽酸生成MoS3的離子方程式為MoS2-4。
(5)分析化學上,常利用“沉鉬”反應測定鉬的含量,若稱量54.0g鉬精礦,“沉鉬”時得到28.8gMoS3,則鉬精礦中鉬的百分含量為(轉化工藝中鉬的損失不計,保留三位有效數字)。組卷:14引用:1難度:0.5 -
19.KI可用于分析試劑、感光材料、制藥等,其制備原理如圖:
反應Ⅰ:3I2+6KOH=KIO3+5KI+3H2O
反應Ⅱ:3H2S+KIO3=3S↓+KI+3H2O
請回答有關問題。
(1)裝置中盛裝30%氫氧化鉀溶液的儀器名稱是。
(2)關閉啟普發生器活塞,先滴入30%的KOH溶液.待觀察到三頸燒瓶中溶液顏色由棕黃色變為(填現象),停止滴入KOH溶液;然后打開啟普發生器活塞,待三頸燒瓶和燒杯中產生氣泡的速率接近相等時停止通氣。
(3)滴入硫酸溶液,并對三頸燒瓶中的溶液進行水浴加熱,其目的是。
(4)把三頸燒瓶中的溶液倒入燒杯中,加入碳酸鋇,在過濾器中過濾,過濾得到的沉淀中除含有過量碳酸鋇外,還含有單質硫和(填名稱)。合并濾液和洗滌液,蒸發至析出結晶,干燥得成品。
(5)碘被稱為“智力元素”,科學合理地補充碘可防治碘缺乏病,KIO3用于加碘鹽中。實驗室模擬工業制備KIO3流程如圖:
幾種物質的溶解度見下表:
①由上表數據分析可知,“操作a”為KCl KH(IO3)2 KClO3 25℃時的溶解度 20.8 0.8 7.5 80℃時的溶解度 37.1 12.4 16.2 。
②反應Ⅰ中,兩種還原產物得電子數相等,請寫出發生的化學反應方程式。
(6)某同學測定上述流程生產的KIO3樣品的純度。
取1.00g樣品溶于蒸餾水中并用硫酸酸化,再加入過量的KI和少量的淀粉溶液,逐滴滴加2.0mol?L-1Na2S2O3溶液,恰好完全反應時共消耗12.60mLNa2S2O3溶液。該樣品中KIO3的質量分數為(已知反應:I2+2Na2S2O3=2NaI+Na2S4O6)。組卷:12引用:1難度:0.6


