2021-2022學(xué)年遼寧省沈陽(yáng)市郊聯(lián)體高三(上)月考化學(xué)試卷(10月份)
發(fā)布:2024/4/20 14:35:0
一、選擇題(本題共15個(gè)小題,每小題3分,共45分,每小題有1個(gè)選項(xiàng)符合題意)
-
1.古代的很多詩(shī)歌、諺語(yǔ)都蘊(yùn)含著科學(xué)知識(shí)。下列解釋正確的是( )
A.“忽聞海上有仙山,山在虛無(wú)縹緲間”的海市蜃樓是一種自然現(xiàn)象,與膠體知識(shí)有關(guān) B.“春蠶到死絲方盡,蠟炬成灰淚始干”,“淚”是指石蠟燃燒生成的水 C.“爆竹聲中除舊歲,春風(fēng)送暖入屠蘇”,爆竹爆炸發(fā)生的是分解反應(yīng) D.“紛紛燦爛如星隕,赫赫喧雁似火攻”中煙花是某些金屬元素發(fā)生化學(xué)變化呈現(xiàn)出的顏色 組卷:31引用:4難度:0.6 -
2.下列關(guān)于化學(xué)用語(yǔ)的表述正確的是( )
A.BF3的電子式: 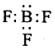
B.Fe2+的原子結(jié)構(gòu)示意圖: 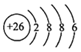
C.中子數(shù)為143的U原子: U23592D.乙醇的結(jié)構(gòu)簡(jiǎn)式:C2H6O 組卷:10引用:2難度:0.7 -
3.NA為阿伏加德羅常數(shù)的值。下列敘述正確的是( )
A.18g重水(D2O)中含有的質(zhì)子數(shù)為10NA B.3mol的NO2與H2O完全反應(yīng)時(shí)轉(zhuǎn)移的電子數(shù)為4NA C.31gP4(分子結(jié)構(gòu):  )中的共價(jià)鍵數(shù)目為1.5NA
)中的共價(jià)鍵數(shù)目為1.5NAD.1LpH=4的0.1mol?L-1K2Cr2O7溶液中Cr2O72-離子數(shù)為0.1NA 組卷:27引用:3難度:0.7 -
4.下列說(shuō)法正確的是( )
A.H2、D2、T2互為同素異形體 B.H2、D2、T2在相同條件下的密度之比為1:2:3 C.由H、D、T與16O、17O、18O能形成9種水分子 D.D、T發(fā)生核聚變成為其他元素,屬于化學(xué)變化 組卷:18引用:3難度:0.8 -
5.室溫下,下列各組離子在給定溶液中能大量共存的是( )
A.pH=10的溶液中,Na+、ClO-、AlO2-、Cl- B.0.1mol?L-1Fe2(SO4)3溶液中,Cu2+、CO32-、SO42-、NH4+ C.使藍(lán)色石蕊試紙變紅的溶液中,Mg2+、HCO3-、K+、Cl- D.0.2mol?L-1KI溶液中,MnO4-、H+、Al3+、Br- 組卷:79引用:10難度:0.8 -
6.在給定條件下,下列選項(xiàng)所示的物質(zhì)間轉(zhuǎn)化均能實(shí)現(xiàn)的是( )
A.NaCl(aq) Cl2(g)電解FeCl2(s)Fe(s)△B.N2(g) NH3(g)H2(g)高溫高壓、催化劑NaHCO3(s)CO2(g)NaCl(aq)C.MgCl2(aq) Mg(OH)2(s)石灰乳Mg(s)煅燒D.S(s) SO3(g)O2(g)點(diǎn)燃H2SO4(aq)H2O(l)組卷:30引用:4難度:0.7
二、非選擇題(共55分)
-
18.某種電鍍污泥主要含有碲化亞銅(Cu2Te)、三氧化二鉻(Cr2O3)以及少量的金(Au),可用于制取Na2Cr2O7溶液、金屬銅和粗碲等,以實(shí)現(xiàn)有害廢料的資源化利用,工藝流程如圖:
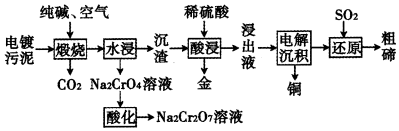
已知:煅燒時(shí),Cu2Te發(fā)生的反應(yīng)為Cu2Te+2O22CuO+TeO2。高溫
(1)Te元素在元素周期表中的位置為其基態(tài)原子的電子占據(jù)的最高能層符號(hào)為。
(2)煅燒時(shí),Cr2O3發(fā)生反應(yīng)的化學(xué)方程式為。
(3)浸出液中除了含有TeOSO4(在電解過(guò)程中不反應(yīng))外,還可能含有(填化學(xué)式)。電解沉積過(guò)程中析出單質(zhì)銅的電極為極。
(4)工業(yè)上用重鉻酸鈉(Na2Cr2O7)母液生產(chǎn)重鉻酸鉀(K2Cr2O7)的工藝流程如圖所示: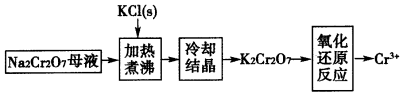
通過(guò)冷卻結(jié)晶能析出大量K2Cr2O7的原因是。
(5)測(cè)定產(chǎn)品中K2Cr2O7含量的方法如下:稱取試樣2.50g配成250mL溶液,取25.00mL于錐形瓶中,加入足量稀硫酸和幾滴指示劑,用0.1000mol?L-1(NH4)2Fe(SO4)2標(biāo)準(zhǔn)液進(jìn)行滴定。滴定過(guò)程中發(fā)生反應(yīng)的離子方程式為。
若三次實(shí)驗(yàn)消耗(NH4)2Fe(SO4)2標(biāo)準(zhǔn)液的體積平均為25.00mL,則所得產(chǎn)品中K2Cr2O7的純度為%(保留三位有效數(shù)字)。組卷:105引用:5難度:0.5 -
19.某科學(xué)研究小組設(shè)計(jì)以輝鉬礦(MoS2、CuFeS2、Cu2S及SiO2等)為原料制備少量鉬酸銨的工藝流程如圖。
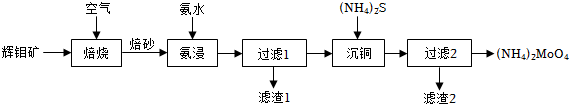
已知:①“焙砂”中有MoO3、CuSO4、CuMoO4、Fe2O3、Fe2(SO4)3、SiO2。
②“氨浸“時(shí),銅元素轉(zhuǎn)化為[Cu(NH3)4](OH)2(深藍(lán)色),鉬元素轉(zhuǎn)化為(NH4)2MoO4。
③[Cu(NH3)4](OH)2═[Cu(NH3)4]2++2OH-。
回答下列問(wèn)題:
(1)“焙燒”在馬弗爐中進(jìn)行。
①為了使輝鉬礦充分培燒,需要采取的措施是(寫(xiě)出一種)。
②馬弗爐中逸出的氣體可用溶液吸收。
③MoS2轉(zhuǎn)化成MoO3的化學(xué)方程式為。
(2)“氨浸”時(shí)發(fā)生多個(gè)反應(yīng),其中CuMoO4被浸取的化學(xué)方程式為。
(3)“濾渣Ⅰ”的成分有SiO2、(填化學(xué)式)。
(4)“沉銅”是在80℃時(shí)進(jìn)行的,銅沉淀完全的依據(jù)是,發(fā)生反應(yīng)的離子方程式為。組卷:22引用:3難度:0.5


