2016-2017學年河北省衡水市武邑中學高二(下)開學化學試卷
發(fā)布:2024/11/19 14:0:1
一、選擇題(本題共20小題,每小題只有一個選項符合題意,每小題2分,共20分)
-
1.有機物的種類繁多,但其命名是有規(guī)則的.下列有機物命名正確的是( )
A. 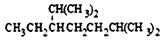
2,6-二甲基-5-乙基庚烷B. 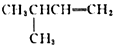
3-甲基-1-丁烯C. 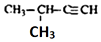
2-甲基-3-丁烯D. 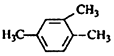
1,3,4-三甲苯組卷:28引用:3難度:0.9 -
2.下列儀器中一般不能用作反應(yīng)容器的是( )
A. 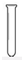
B. 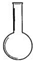
C. 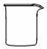
D. 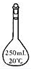 組卷:59引用:2難度:0.9
組卷:59引用:2難度:0.9 -
3.下列反應(yīng)中屬于置換反應(yīng)的是( )
A.乙醇與金屬鈉的反應(yīng) B.氫氧化鐵與稀硫酸的反應(yīng) C.氯化鐵溶液與銅片的反應(yīng) D.一氧化碳還原氧化鐵的反應(yīng) 組卷:21引用:2難度:0.9 -
4.常溫下能與水反應(yīng)的非金屬單質(zhì)是( )
A.Na B.C C.Cl2 D.NH3 組卷:17引用:2難度:0.9 -
5.下列物質(zhì)的水溶液因水解而顯酸性的是( )
A.KNO3 B.Fe2(SO4)3 C.Na2CO3 D.H2SO4 組卷:19引用:5難度:0.9 -
6.下列實驗事實不能證明醋酸是弱酸的是( )
A.常溫下,測得醋酸鈉溶液的pH>7 B.常溫下,測得0.1 mol/L醋酸溶液的pH=4 C.常溫下,將pH=1的醋酸溶液稀釋1 000倍,測得pH<4 D.常溫下,將物質(zhì)的量濃度相同的醋酸溶液與氫氧化鈉溶液等體積混合后恰好中和 組卷:48引用:20難度:0.9 -
7.在1000K時,已知反應(yīng)Ni(s)+H2O(g)?NiO(s)+H2(g)的平衡常數(shù)K=0.0059.當水蒸氣和氫氣的物質(zhì)的量濃度相等時,此反應(yīng)( )
A.已達平衡狀態(tài) B.V正>V逆 C.未達平衡狀態(tài),平衡逆向移動 D.無法確定是否達到平衡狀態(tài) 組卷:13引用:2難度:0.7 -
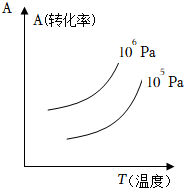 8.有一化學平衡mA(g)+nB(g)═pC(g)+qD(g),如圖表示的轉(zhuǎn)化率與壓強、溫度的關(guān)系.由此得出的正確結(jié)論是( )
8.有一化學平衡mA(g)+nB(g)═pC(g)+qD(g),如圖表示的轉(zhuǎn)化率與壓強、溫度的關(guān)系.由此得出的正確結(jié)論是( )A.正反應(yīng)是吸熱反應(yīng),(m+n)>(p+q) B.正反應(yīng)是吸熱反應(yīng),(m+n)<(p+q) C.正反應(yīng)是放熱反應(yīng),(m+n)>(p+q) D.正反應(yīng)是放熱反應(yīng),(m+n)<(p+q) 組卷:63引用:13難度:0.7
二、填空題(本題共6小題,共50分)
-
25.根據(jù)下列化合物:①NaOH,②H2SO4,③CH3COOH,④NaCl,⑤CH3COONa,⑥NH4Cl,⑦CH3COONH4,⑧NH4HSO4,⑨NH3?H2O,請回答下列問題:
(1)若濃度均為0.1mol?L-1、等體積的NaOH和NH3?H2O分別加水稀釋m倍、n倍,稀釋后兩種溶液的pH都變成9,則 mn (填“<”、“>”或“=”).
(2)已知水存在如下平衡:H2O+H2O?H3O++OH-△H>0,現(xiàn)欲使平衡向右移動,且所得溶液顯酸性,選擇的下列方法是.
A.向水中加入NaHSO4固體
B.向水中加NaHCO3固體
C.加熱至100℃[其中c(H+)=1×10-6 mol?L-1]
D.向水中加入NH4Cl固體
(3)常溫下,pH=11的CH3COONa溶液中,水電離出來的c(OH-)=;在pH=3的CH3COOH 溶液中,水電離出來的c(H+)=.
(4)NH4Cl溶液中離子濃度大小順序為.
(5)物質(zhì)的量濃度相同的⑥、⑦、⑧、⑨四種稀溶液中,NH4+濃度由大到小的順序是(填序號).
(6)已知t℃時,Kw=1×10-12,在該溫度時將pH=9的NaOH溶液a L與pH=2的H2SO4溶液b L混合(忽略混合后溶液體積的變化),若所得混合溶液的pH=3,則a:b=.組卷:24引用:4難度:0.3 -
26.工業(yè)上制備BaCl2的工藝流程圖如圖:
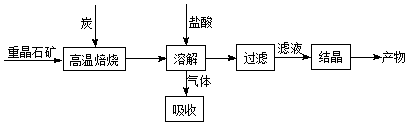
某研究小組在實驗室用重晶石(主要成分BaSO4)對工業(yè)過程進行模擬實驗.查表得
BaSO4(s)+4C(s)4CO(g)+BaS(s)△H1=+571kJ?mol-1 ①高溫
BaSO4(s)+2C(s)2CO2(g)+BaS(s)△H2=+226kJ?mol-1 ②高溫
(1)反應(yīng)C(s)+CO2(g)2CO(g)的△H=高溫kJ?mol-1.
(2)氣體用過量NaOH溶液吸收,得到Na2S,在Na2S水溶液中c(Na+)與c(S-2)的關(guān)系是.(填字母)
A.c(Na+)=2c(S2-)B.c(Na+)<2c(S2-)
C.c(Na+)>2c(S2-)D.2c(Na+)>c(S2-)
(3)向AgNO3溶液中加入BaCl2和KBr,當兩種沉淀共存時,=c(Br-)c(Cl-).
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
(4)常溫常壓下,空氣中的CO2溶于水達到平衡時,溶液的pH=5.6,溶液中 c(H2CO3)=1.5×10-5mol?L-1.若忽略水的電離及H2CO3的第二級電離,則H2CO3+H+ 的平衡常數(shù)K1=HCO-3.(保留兩位有效數(shù)字)(已知:10-5.60=2.5×10-6)組卷:5引用:2難度:0.5


