人教版(2019)選擇性必修1《2.4 化學反應的調控》2023年同步練習卷(1)(2)
發(fā)布:2024/8/16 17:0:1
一、選擇題
-
1.已知反應N2(g)+3H2(g)?2NH3(g)的ΔH<0,在恒容密閉容器中反應達到平衡時,下列說法正確的是( )
A.N2的正反應速率是H2的逆反應速率的3倍 B.通入稀有氣體使壓強增大,平衡將向正反應方向移動 C.降低溫度,混合氣體的平均相對分子質量變大 D.若平衡時N2、H2的轉化率相等,說明反應開始時N2的物質的量是H2的物質的量的3倍 組卷:2引用:2難度:0.6 -
2.下列有關以H2和N2為原料氣的工業(yè)合成氨反應的說法不正確的是( )
A.屬于放熱反應 B.△S>0 C.屬于可逆反應 D.在恒容容器中反應,壓強逐漸減小 組卷:14引用:4難度:0.5 -
3.如圖所示為工業(yè)合成氨的流程圖。下列說法錯誤的是( )
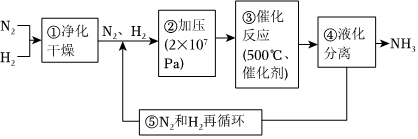
A.步驟①中“凈化”可以防止催化劑中毒 B.步驟②中“加壓”既可以提高原料的轉化率,又可以加快反應速率 C.步驟③、④、⑤均有利于提高原料平衡的轉化率 D.為保持足夠高的反應速率,應在反應達到一定轉化率時及時將氨從混合氣中分離出去 組卷:133引用:6難度:0.6 -
4.下列關于工業(yè)合成氨的敘述正確的是( )
A.合成氨工業(yè)溫度選擇為700K左右,只要是為了提高NH3產率 B.使用催化劑和施加高壓,都能提高反應速率,但對化學平衡狀態(tài)無影響 C.合成氨生產過程中將NH3液化分離,可提高N2、H2的轉化率 D.合成氨工業(yè)中為了提高氫氣的利用率,可適當增加氫氣濃度 組卷:208引用:5難度:0.7 -
 5.CH4與CO2重整生成H2和CO的過程中主要發(fā)生下列反應
5.CH4與CO2重整生成H2和CO的過程中主要發(fā)生下列反應
CH4(g)+CO2(g)═2H2(g)+2CO(g)△H=+247.1kJ?mol-1
H2(g)+CO2(g)═H2O(g)+CO(g)△H=+41.2kJ?mol-1
在恒壓、反應物起始物質的量比n(CH4):n(CO2)=1:1條件下,CH4和CO2的平衡轉化率隨溫度變化的曲線如圖所示。下列有關說法不正確的是( )A.升高溫度、減小壓強均有利于提高CH4的平衡轉化率 B.曲線B表示CH4的平衡轉化率隨溫度的變化 C.相同條件下,改用高效催化劑能使曲線A和曲線B相重疊 D.恒壓、800K、n(CH4):n(CO2)=1:1條件下,反應至CH4轉化率達到X點的值,改變除溫度外的特定條件繼續(xù)反應,CH4轉化率能達到Y點的值 組卷:53引用:8難度:0.7
四、解答題
-
16.合成氨工業(yè)的反應原理為N2+3H2
2NH3,合成氨工業(yè)對化學工業(yè)和國防工業(yè)具有重要意義。工業(yè)合成氨生產示意圖如圖甲所示。催化劑高溫、高壓
(1)X的化學式為。
(2)圖甲中條件選定的主要原因是。
A.溫度、壓強對化學平衡的影響
B.鐵觸媒在該溫度時活性大
C.工業(yè)生產受動力、材料、設備等條件的限制
(3)改變反應條件,會使平衡發(fā)生移動。如圖乙表示隨條件改變,氨的百分含量的變化趨勢。當橫坐標為壓強時,變化趨勢正確的是,當橫坐標為溫度時,變化趨勢正確的是。(填字母)組卷:6引用:2難度:0.7 -
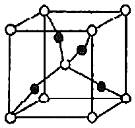 17.維持大氣中CO2的平衡對生態(tài)環(huán)境保護有著重要意義。
17.維持大氣中CO2的平衡對生態(tài)環(huán)境保護有著重要意義。
(1)CO2催化加氫合成低碳烯烴技術能有效利用大氣中的CO2。
以合成C2H4為例,該轉化分為兩步進行:
第一步:CO2(g)+H2(g)?CO(g)+H2O(g)△H1=+41.3kJ/mol
第二步:2CO(g)+4H2(g)?C2H4(g)+2H2O(g)△H2=-210.5kJ/mol
CO2加氫合成乙烯的熱化學方程式為。
(2)CO2催化加氫在一定條件下還可以合成CH4.已知反應CO2(g)+4H2(g)?CH4(g)+2H2O(g)。在體積為1L的密閉剛性容器中,充入4mol H2和1mol CO2,測得溫度對CO2的平衡轉化率和催化劑催化效率的影響如圖1所示。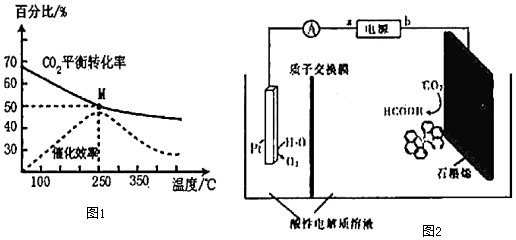
①已知M點總壓為1MPa,該反應在此溫度下的平衡常數(shù)Kp=MPa-2.(Kp是用平衡分壓代替平衡濃度表示的化學平衡常數(shù),氣體分壓=氣體總壓×物質的量分數(shù)。)
②欲增加二氧化碳的平衡轉化率,可采取的措施有(填字母)。
A.通入惰性氣體
B.提高溫度
C.增加二氧化碳濃度
D.增加氫氣濃度
(3)利用銅基配合物l,10-phenanthroline-Cu催化劑電催化CO2還原制備碳基燃料(包括CO、烷烴和酸等)是減少CO2在大氣中累積和實現(xiàn)可再生能源有效利用的關鍵手段之一,其裝置原理如圖2所示。
電池工作過程中,圖中Pt電極附近溶液的pH(填“變大”或“變小”),陰極的電極反應式為,每轉移2mol電子,陰極室溶液質量增加g。組卷:17引用:2難度:0.5


