2021年福建省廈門大學附屬科技中學創新班中考化學模擬試卷
發布:2024/6/15 8:0:9
一、選擇題(每小題只有1個正確答案,每題6分,共30分)
-
1.在明代宋應星所著的《天工開物》中,有關火法煉鋅的工藝記載:“每爐甘石十斤,裝載入一泥罐內,然后逐層用煤炭餅墊盛,其底鋪薪,發火煅紅,罐中爐甘石熔化成團。”(已知:爐甘石的主要成分是碳酸鋅)下列說法正確的是( )
A.反應前后固體的質量不變 B.在此過程中只產生一種碳的氧化物 C.“罐中爐甘石熔化成團”,團的主要成分是鋅 D.“逐層用煤炭餅墊盛”是為了燃燒提供高溫 組卷:86引用:5難度:0.7 -
2.沿海城市應當合理食用加碘食鹽。已知:①加碘鹽中的碘元素以碘酸鉀KIO3形式存在。②KIO3在酸性條件下能與KI溶液發生反應生成碘(I2)。③碘單質遇淀粉變藍色。現提供下列試劑和生活中常見的物質:①米湯;②小蘇打;③KI溶液;④蔗糖;⑤醫用酒精;⑥白醋;該同學進行檢測必須選用的試劑和物質是( )
A.①③⑥ B.①③④ C.②④⑥ D.①④⑤ 組卷:9引用:2難度:0.5 -
3.化學工藝可“變廢為寶”。工業上處理黃銅渣可得到硫酸鋅,主要流程如圖所示。已知:①黃銅渣中約含Zn7%、ZnO31%、Cu50%、CuO5%,其余為雜質;②雜質不溶于水,不參與反應。
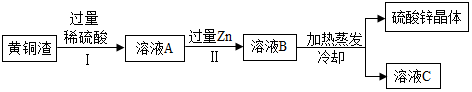
下列說法正確的是( )A.溶液A中的溶質有2種 B.溶液C中溶質的質量分數小于溶液B C.溶液A的質量大于溶液B D.Ⅰ、Ⅱ中的操作均包含過濾 組卷:12引用:3難度:0.6
二、非選擇題(4題,共70分)
-
8.鋁、鋅是生活中常見的金屬元素。它們的化學性質具有一定的相似性。化學興趣小組對鋁和鋅的某些性質進行相關探究。
【實驗回顧】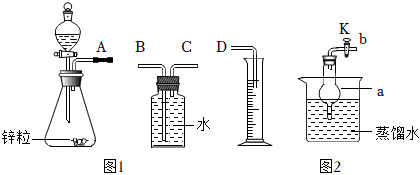
(1)鋅與稀硫酸反應
①用圖1所示裝置制取氫氣。鋅與稀硫酸反應的化學方程式為。
②裝置連接順序是:A→→→D(填字母)。
③如何檢驗氣體發生裝置的氣密性。
【實驗改進】
(2)硫酸銅對氫氣生成速率的影響。
興趣小組查閱資料得知加入少量硫酸銅可以加快氫氣的生成速率。興趣小組設計如下實驗進行探究:
在錐形瓶中分別放入足量的、等質量的、顆粒大小相同的鋅粒,再向分液漏斗中加入由31.5%的稀硫酸,不同體積水、5%的硫酸銅溶液組成的混合液,試劑用量記錄如下表所示。
①表中的V1=混合液(試管編號) ① ② ③ ④ ⑤ 31.5%的H2SO4溶液/mL 10 V1 10 10 10 5%的CuSO4溶液/mL 3.6 3.8 4.0 4.2 4.4 蒸餾水/mL 16.4 16.2 16.0 15.8 V2 收集70mL水所用時間/s 21.2 20.4 19.7 20.5 21.3 mL,V2=mL。
②表中(填寫試管編號)組反應速率最快。
【提出問題】已知鋅和水不反應,那么鋁能否與水反應生成氫氣?
【查閱資料】
(3)鋁在空氣中與氧氣反應,其表面生成一層致密的氧化鋁薄膜,起到保護膜的作用。如生活中可用鋁壺燒水。鋁與氧氣反應的化學方程式為物質 鈉與水 鋁與水 汞與水 能否發生反應 能反應 能反應 不反應 。
(4)除去鋁表面氧化鋁薄膜的方法(舉一例)。除上述方法外,還可以將鋁片浸沒在氯化汞溶液中,破壞鋁片表面致密的氧化膜且防止其重新生成。
【實驗探究】
(5)將鋁片完全浸入氯化汞(HgCl2)溶液中1min左右,取出,立即用流水沖洗干凈后放入容器a,并將a放入到蒸餾水中(如圖2),其表面生成大量氣泡、周圍出現白色沉淀,鋁與氯化汞溶液發生置換反應的化學方程式為。
(6)在導管口b處涂肥皂水,發現導管口有氣泡形成,當氣泡離開導管后,氣泡(填“下沉”或“上升”),用燃著的木條點燃氣泡,。
【實驗結論】
(7)鋁能與水反應生成氫氣,寫出鋁與水反應生成氫氧化鋁和氫氣的化學方程式。
【實驗反思】
(8)汞有毒會污染環境,興趣小組的同學用硫粉處理單質汞,用飽和硫化鈉溶液處理使用過的氯化汞廢液。組卷:6引用:2難度:0.2 -
9.疊氮化鈉(NaN3)被廣泛應用于汽車安全氣囊,工業級NaN3中常含有少量的Na2CO3,某化學研究性學習小組圍繞工業NaN3樣品的性質和純度等問題展開討論與研究:
【查閱資料】
①NaN3受撞擊會生成Na、N2。
②NaN3遇鹽酸、H2SO4溶液沒有氣體生成。
③堿石灰是CaO和NaOH的混合物。
④NaN3的制備方法是:將金屬鈉與液態氨反應制得NaNH2,再將NaNH2與N2O反應可生成NaN3、NaOH和NH3。
【問題探究】
Ⅰ.樣品性質的探究
(1)汽車經撞擊后,30毫秒內引發NaN3迅速分解,寫出該反應的化學方程式。
(2)工業級NaN3中常含有少量的Na2CO3,其原因是(用化學方程式表示)。
Ⅱ.樣品純度的測定
為測定某工業級NaN3樣品中含有Na2CO3的質量分數,小組同學設計了兩種方案。
【實驗方案】
(3)方案一:通過測定裝置(圖1)中反應前后裝置B的質量差,計算求解NaN3樣品的純度。
①測定原理(裝置A)。(用化學方程式表示)
②小組同學通過討論認為該裝置存在較多因素會導致測定數據不準確,請寫出可能的原因(寫出一種即可)。
方案二:在討論的基礎上,又設計了另一套裝置(圖2)。
裝置B中樣品在與稀硫酸反應前和停止反應后,都需要通入過量的空氣。反應前通入空氣時a、b、c三個彈簧夾的控制方法是,停止反應后,通入過量的空氣的目的是。
【實驗過程】
(4)根據方案二,小組同學設計的實驗步驟如下:
a.稱量裝置
b.稱量樣品,檢查裝置氣密性
c.打開彈簧夾,鼓入空氣
d.關閉彈簧夾,打開分液漏斗的活塞和玻璃塞,注入足量的稀硫酸,關閉活塞和玻璃塞
為保證測定結果精確,正確的操作順序為(填字母序號,可重復)。
【數據分析】
(5)若樣品的質量為mg,實驗結束測得裝置C增重m1g,裝置D增重m2g,則樣品的純度(質量分數)為(列出計算式,不需要化簡)。
【拓展延伸】
(6)若將裝置D改用裝有澄清石灰水的洗氣瓶是否可行,請說明原因:。組卷:33引用:2難度:0.5


