2020-2021學(xué)年云南省曲靖市富源一中高一(下)期中化學(xué)試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題:本題共20個小題,每小題3分,共60分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.下列關(guān)于物質(zhì)組成的說法中,正確的是( )
A.酸、堿、鹽可能都不含金屬元素 B.含氧元素的化合物一定是氧化物 C.單質(zhì)不一定只含一種元素 D.酸、堿中一定含氫,鹽一定不含氫 組卷:4引用:1難度:0.8 -
 2.固態(tài)單質(zhì)甲及其化合物之間的轉(zhuǎn)化如圖所示(某些產(chǎn)物及反應(yīng)條件略去)。下列分析錯誤的是( )
2.固態(tài)單質(zhì)甲及其化合物之間的轉(zhuǎn)化如圖所示(某些產(chǎn)物及反應(yīng)條件略去)。下列分析錯誤的是( )A.甲在空氣中燃燒產(chǎn)生淡藍(lán)色火焰 B.工業(yè)上乙→丙的條件是:高溫、高壓、催化劑 C.乙和丙的相對分子質(zhì)量比為4:5 D.戊既有還原性又有氧化性 組卷:79引用:4難度:0.4 -
3.能正確表示下列化學(xué)反應(yīng)的離子方程式的是( )
A.氫氧化鋇溶液與硫酸的反應(yīng):OH-+H+═H2O B.澄清的石灰水與醋酸反應(yīng):Ca(OH)2+2H+═Ca2++2H2O C.銅片插入硝酸銀溶液中:Cu+Ag+═Cu2++Ag D.碳酸鈣溶于稀鹽酸中:CaCO3+2H+═Ca2++H2O+CO2↑ 組卷:15引用:2難度:0.6 -
4.下列判斷不正確的是( )
A.穩(wěn)定性:HF >H2O >H2S B.還原性:K>Na >Mg C.離子半徑:Na+>Al3+>F- D.酸性強(qiáng)弱:HNO3>H2CO3>H2SiO3 組卷:2引用:1難度:0.8 -
5.SO2氣體與足量Fe2(SO4)3溶液完全反應(yīng)后,再加入K2Cr2O7溶液,發(fā)生如下化學(xué)反應(yīng):
①SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;
②Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O.
則下列有關(guān)說法不正確的是( )A.氧化性:Cr2O72->Fe3+>SO2 B.標(biāo)準(zhǔn)狀況下,若有6.72 L SO2參加反應(yīng),則最終消耗0.2 mol K2Cr2O7 C.反應(yīng)②中,每有1 mol K2Cr2O7參加反應(yīng),轉(zhuǎn)移電子的數(shù)目為6NA D.由上述反應(yīng)原理推斷:K2Cr2O7能將Na2SO3氧化成Na2SO4 組卷:78引用:13難度:0.7 -
6.只用一種試劑就能將NH4Cl、(NH4)2SO4、NaCl、Na2SO4四種溶液區(qū)分開,這種試劑是( )
A.NaOH溶液 B.AgNO3溶液 C.Ba(OH)2溶液 D.BaCl2溶液 組卷:83引用:21難度:0.7 -
7.為了除去粗鹽中的Ca2+、Mg2+、SO42-及泥沙,可將粗鹽溶于水,然后進(jìn)行下列五項操作:①過濾 ②加過量NaOH溶液 ③加適量鹽酸 ④加過量Na2CO3溶液 ⑤加過量BaCl2溶液。下列操作順序中最合適的是( )
A.①④②⑤③ B.④①②⑤③ C.②⑤④①③ D.⑤②④③① 組卷:7引用:2難度:0.5 -
8.下列說法正確的是(NA示阿伏加德羅常數(shù)的值)( )
A.32gO2所占的體積約為22.4L B.22.4LN2含NA個氮分子 C.在標(biāo)準(zhǔn)狀況下,22.4L水的物質(zhì)的量為1mol D.22g二氧化碳與標(biāo)準(zhǔn)狀況下11.2LHCl含有相同的分子數(shù) 組卷:0引用:1難度:0.6
二、填空題:本題包括4個小題,每小題10分,共40分
-
23.2SO2(g)+O2(g)?2SO3(g),是工業(yè)制硫酸的主要反應(yīng)之一。
(1)該反應(yīng)過程的能量變化如圖1所示: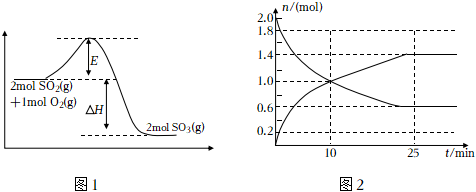
由圖中曲線變化可知,該反應(yīng)為(填“放熱”或“吸熱”)反應(yīng)。
(2)斷開氣態(tài)物質(zhì)中1mol某種共價鍵生成氣態(tài)原子需要吸收的能量稱為鍵能(kJ?mol?1)。如表所示是一些共價鍵的鍵能。
根據(jù)上表的數(shù)據(jù),在合成1mol氨共價鍵 H-H N≡N N-H 鍵能(kJ?mol-1) 436 946 391 (“放出”或“吸收”)的熱量為kJ。
(3)在2L容器中投入2molSO2和b mol O2,如圖2是部分反應(yīng)物與生成物隨時間的變化曲線。
①10min時v(正)v(逆)(填“大于”或“小于”或“等于”);0~10min內(nèi),v(SO3)=。
②反應(yīng)達(dá)到最大限度的時間是min,平衡時,SO2的轉(zhuǎn)化率為。
③下列條件能夠加快反應(yīng)速率的是。
A.升高溫度
B.保持壓強(qiáng)不變,充入He使容積增大
C.保持體積不變,充入He使壓強(qiáng)增大
D.充入一定量的氧氣
④下列情況能說明該反應(yīng)達(dá)到化學(xué)平衡的是。
A.v(SO3)=v(SO2)
B.混合氣體的密度保持不變
C.t時刻,體系的溫度不再發(fā)生改變
D.混合氣體的總物質(zhì)的量不再改變
E.SO2、O2、SO3的物質(zhì)的量之比達(dá)到2:1:2組卷:81引用:2難度:0.6 -
24.Ⅰ.以黃鐵礦(主要成分FeS2)為原料生產(chǎn)硫酸,應(yīng)將產(chǎn)出的爐渣和尾氣進(jìn)行資源化綜合利用,減輕對環(huán)境的污染。其中一種流程如圖所示。

(1)黃鐵礦中硫元素的化合價為;
(2)欲得到更純的NaHSO3,反應(yīng)①應(yīng)通入(填“過量”或“不足量”)的SO2氣體;
(3)因為Na2S2O5具有還原性,導(dǎo)致商品Na2S2O5中不可避免地存在Na2SO4,檢驗其中含有SO42-的方法是。
Ⅱ.黃鐵礦煅燒后得到的爐渣(含F(xiàn)e2O3、FeO、SiO2及Al2O3),還可以用來生產(chǎn)一種高效混凝劑聚合硫酸鐵鋁硅,工藝流程如圖。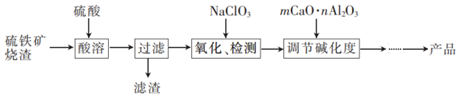
已知:mCaO?nAl2O3難溶于水。
(4)“過濾”所得濾渣為(填化學(xué)式);
(5)“氧化”時發(fā)生反應(yīng)的離子方程式為;
(6)“調(diào)節(jié)堿化度”時,mCaO?nAl2O3與溶液中H+反應(yīng)的離子方程式為。組卷:7引用:2難度:0.4


