2021-2022學年黑龍江省鶴崗一中高二(上)期末化學試卷
發(fā)布:2024/4/20 14:35:0
一、單選題(1-10題每題2分,11-20題每題3分。需在答題卡上填涂。)
-
1.下列化學用語表示正確的是( )
A.HBrO的結構式:H-Br-O B.S2-結構示意圖: 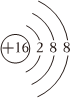
C.CCl4的電子式: 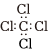
D.反-2-丁烯的結構簡式: 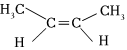 組卷:5引用:2難度:0.7
組卷:5引用:2難度:0.7 -
2.已知反應2CO(g)=2C(s)+O2(g)的△H>0,△S<0,下列說法中正確的是( )
A.低溫下能自發(fā)進行 B.高溫下能自發(fā)進行 C.任何溫度下都不能自發(fā)進行 D.任何溫度下都能自發(fā)進行 組卷:121引用:14難度:0.9 -
3.從溴水中萃取溴,下列試劑中不能用做萃取劑的是( )
A.正己烷 B.直餾汽油 C.四氯化碳 D.酒精 組卷:16引用:1難度:0.8 -
4.下列各組物質互為同分異構體的是( )
A.32S與33S B.CH3CH2CH3與CH3CH2CH(CH3)2 C.O2與O3 D.乙醇和二甲醚(CH3-O-CH3) 組卷:87引用:1難度:0.8 -
5.下列事實不能用勒夏特列原理解釋的是( )
A.開啟啤酒瓶后,馬上泛起大量泡沫 B.實驗室中常用排飽和食鹽水的方法收集氯氣 C.工業(yè)上生產(chǎn)硫酸的過程中使用過量的空氣以提高二氧化硫的利用率 D.對于2HI(g)?H2+I2,達到平衡后,縮小容器容積可使體系顏色變深 組卷:31引用:6難度:0.5 -
6.甲烷與氯氣在光照條件下反應,得到的產(chǎn)物中含有二氯甲烷、三氯甲烷和四氯化碳,分離它們的操作方法是( )
A.萃取 B.蒸餾 C.過濾 D.重結晶 組卷:386引用:6難度:0.6 -
7.有關煤、石油、天然氣的綜合利用,下列說法正確的是( )
A.石油是多種烴組成的混合物 B.水煤氣是通過煤的液化得到的氣體燃料 C.石油裂解的目的是提高輕質油的產(chǎn)量和質量 D.石油的分餾、煤的干餾是物理變化,煤的氣化和煤的液化是化學變化 組卷:59引用:4難度:0.7 -
8.使1mol乙烯與氯氣發(fā)生完全加成反應,然后使該加成反應的產(chǎn)物與氯氣在光照的條件下發(fā)生取代反應,則兩個過程中消耗氯氣的總物質的量最多是( )
A.3mol B.4mol C.5mol D.6mol 組卷:334引用:65難度:0.7
二、非選擇題
-
24.氨是重要的基礎化工原料,工業(yè)上常用于制備氨水、亞硝酸(HNO2)、連二次硝酸(H2N2O2)、尿素[CO(NH2)2]等多種含氮的化工產(chǎn)品。回答下列問題:
Ⅰ.(1)常溫下,0.01mol?L-1的氨水中=1×10-6,則該溶液的pH=c(H+)c(OH-);將pH=4的鹽酸V1L與0.01mol?L-1氨水V2L混合,若混合溶液pH=7,則V1V2(填“>”、“<”或“=”)。
(2)已知:25℃時,亞硝酸和連二次硝酸的電離常數(shù)如表所示:
0.1mol?L-1NaHN2O2溶液中離子濃度由大到小的順序為化學式 HNO2 H2N2O2 電離常數(shù) Ka=5.1×10-4 Ka1=6.17×10-8、Ka2=2.88×10-12 。
(3)向濃度均為0.1mol?L-1的CdCl2和ZnCl2混合液中滴加碳酸銨溶液,當加入碳酸銨溶液至生成兩種沉淀,則溶液中c(Zn2+):c(Cd2+)=。[已知:Ksp(CdCO3)=1.0×10-12mol2?L-2,Ksp(ZnCO3)=1.5×10-10mol2?L-2]
Ⅱ.可樂中的食品添加劑有白砂糖、二氧化碳、焦糖色、磷酸、咖啡因等。可樂的辛辣味與磷酸(化學式為H3PO4,沸點高難揮發(fā))有一定關系。
(4)羥基磷灰石[Ca5(PO4)3OH]是牙釉質的主要成分,在唾液中存在平衡:Ca5(PO4)3OH(s)?5Ca2+(aq)+3PO43-(aq)+OH-(aq)。長期過量飲用可樂會破壞牙釉質,造成齲齒。結合平衡移動原理解釋原因:。
(5)常溫下,向磷酸溶液中滴加NaOH溶液,含磷微粒的分布比例與pH的關系如圖所示。
NaH2PO4溶液顯酸性。下列有關分析正確的是。
a.溶液中c(OH-)>c(H+)
b.H2PO4-的電離程度大于其水解程度
c.c(Na+)+c(H+)=c(H2PO4-)+2c(HPO42-)+3c(PO43-)+c(OH-)
d.溶液中水的電離程度比純水大組卷:15引用:1難度:0.6 -
25.某學習小組按如下實驗流程探究海帶中碘含量的測定和碘的制取。
實驗(一)碘含量的測定
取100.00mL海帶浸取原液于錐形瓶中,用0.0100mol?L-1的AgNO3標準溶液測定其中的碘,消耗標準溶液體積的平均值為20.00mL。
(1)儀器A的名稱為。
(2)計算海帶中碘的百分含量為%。
實驗(二)碘的制取
另取海帶浸取原液,甲、乙兩種實驗方案如圖:
已知:3I2+6NaOH=5NaI+NaIO3+3H2O;酸性條件下,I2在水中的溶解度很小。
(3)“適量O2”中能代替O2的最佳物質電子式為。
(4)步驟X中,萃取后分液漏斗內觀察到的現(xiàn)象是。
(5)下列有關步驟Y的說法中正確的是(填序號)。
A.應控制NaOH溶液的濃度和體積
B.將碘轉化成離子進入水層
C.主要是除浸取原液中的有機雜質
D.NaOH溶液可由乙醇代替
(6)方案乙中,上層液體中加入H2SO4溶液,反應的離子方程式為,其中操作Z的名稱是,方案甲中采用蒸餾效果不佳,理由是。組卷:15引用:2難度:0.4


