2021-2022學年河北省唐山市高二(上)期末化學試卷
發布:2024/4/20 14:35:0
一、單項選擇題(本題包括12小題,每小題2分,共24分。)
-
1.為了實現“碳達峰”和“碳中和”,太陽能的利用逐漸得到重視。下列說法錯誤的是( )
A.煤、石油和天然氣都屬于碳素燃料 B.發展太陽能經濟有助于減緩溫室效應 C.太陽能電池可將太陽能直接轉化為電能 D.太陽能的直接利用只有“光-電轉換”和“光-生物質能轉換”兩種形式 組卷:32引用:4難度:0.6 -
2.下列變化過程中,ΔS<0的是( )
A.氨氣與氯化氫反應產生白煙 B.蔗糖溶于水 C.濃硝酸見光分解 D.鋅粒投入鹽酸中 組卷:29引用:3難度:0.7 -
3.下列物質在水溶液中,溶質存在電離平衡的是( )
A.NaHSO4 B.CH3COOH C.BaSO4 D.CH3COONa 組卷:53引用:1難度:0.9 -
4.等物質的量濃度的下列各溶液中NH4+濃度最大的( )
A.NH4Cl溶液 B.NH4HSO4溶液 C.(NH4)2CO3溶液 D.氨水 組卷:30引用:1難度:0.5 -
5.下列水解的離子方程式正確的是( )
A.NH4++2H2O?NH3?H2O+H3O+ B.I-+H2O?HI+OH- C.CO32-+2H2O?H2CO3+2OH- D.Al3++3H2O═Al(OH)3+3H+ 組卷:11引用:1難度:0.6 -
6.下列選項中出現的情況不能用勒夏特列原理解釋的是( )
A.使用含有氟化鈉的牙膏可以防止齲齒 B.硫酸亞鐵溶液在空氣中久置產生紅褐色沉淀 C.保存過久的古書籍易腐爛,因為古代的紙張中含有硫酸鋁 D.在凈水過程中,除了加入明礬外,往往再加入少量碳酸氫鈉,以增強凈水能力 組卷:11引用:1難度:0.7 -
7.下列說法錯誤的是( )
A.活化能越小,化學反應速率越大 B.有催化劑參與的化學反應至少含有兩個或多個基元反應 C.增大壓強、升高溫度均可提高反應物中活化分子百分數 D.在化學反應中,能量較高,有可能發生有效碰撞的分子稱為活化分子 組卷:130引用:3難度:0.6 -
 8.下列有關化學實驗說法正確的是( )
8.下列有關化學實驗說法正確的是( )A.鐵片上電鍍鋅時,通常把鐵片做陽極 B.驗證熱效應的氫氧化鋇晶體與氯化銨晶體反應操作中,通常小木板上要灑少量水 C.反應熱測量時,量筒中的氫氧化鈉溶液要緩慢倒入盛有鹽酸的簡易量熱計中 D.為了證明HClO是弱酸,可用廣泛pH試紙測常溫下NaClO溶液的pH值 組卷:6引用:2難度:0.5
五、計算題(本題包括2小題,共20分)
-
23.甲醇是重要的化工原料、燃料。工業上利用合成氣(主要成分為CO、CO2和H2)在催化劑的作用下合成甲醇,發生的主反應如下:
①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)ΔH=-58kJ/mol
②CO2(g)+H2(g)?CO(g)+H2O(g)ΔH=41kJ/mol
回答下列問題:
(1)CO與H2在該條件下也能化合生成甲醇蒸汽。請寫出該反應的熱化學方程式:。
(2)若300℃時,將8molCO2和20molH2充入2L體積不變的密閉容器中發生反應①,測得CH3OH的物質的量隨時間變化情況如下表所示。
①恒溫下,能判斷該反應達到化學平衡狀態依據的是時間/min 0 1 2 3 4 5 6 n(CH3OH)/mol 0 2.2 3.7 5 5.7 6 6 。
a.容器中壓強不變
b.甲醇和水蒸氣的體積比保持不變
c.v正(H2)=3v逆(CH3OH)
d.2個C=O斷裂的同時有3個H-H生成
②1~3min內H2的平均反應速率v=,平衡常數K=;
③反應達平衡時再向容器中充入2molH2、6molCH3OH,則v(正)v(逆)(填“>”“<”或“=”);
(3)若將CO2和H2按不同比例投入一密閉恒溫容器中發生反應②,反應達到平衡時,CO的體積分數隨的變化曲線如圖所示。n(CO2)n(H2)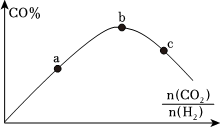
①a、b、c三點CO2的轉化率從大到小的順序為;
②a、b兩點的平衡常數大小關系為ab(填“>”“<”或“=”)。組卷:122引用:1難度:0.6 -
24.t℃時,純水中c(H+)=2.0×10-7mol?L-1,向其中加入少量Ba(OH)2溶液,保持溫度不變,測得溶液中pH=12。回答下列問題:
(1)該溶液中由水電離出來的c(OH-)=。
(2)溶液中c(OH-)-c(H+)=(用離子符號表示)。
(3)若將該溶液溫度升高,pH(填“變大”、“變小”或“不變”)。
(4)t℃時,將0.03mol?L-1的稀硫酸與該溶液等體積混合,保持溫度不變,混合后溶液的pH為。
(5)t℃時,將VAL0.04mol?L-1的醋酸和VBL的Ba(OH)2溶液混合后,得到中性澄清溶液,則其體積關系VAVB(填“>”“<”或“=”,下同)。混合溶液中必定有一種離子能發生水解,其水解反應的離子方程式為。組卷:89引用:1難度:0.6


