2019-2020學年寧夏中衛市宣和中學九年級(下)開學化學試卷
發布:2024/4/20 14:35:0
一、選擇:(選出下列各題中惟一正確的答案.1-11題每題2分,12-13題每題3分,共28分.不選、多選、錯選不得分)
-
1.下列變化不屬于化學變化的是( )
A.木材燃燒 B.露置在空氣中的鐵生銹 C.水加熱時有氣泡產生 D.澄清石灰水通入 CO2 后會變渾濁 組卷:5引用:8難度:0.9 -
2.已知標準狀況下,空氣的密度是1.29克/升,氫氣的密度是0.089克/升,氫氣難溶于水.下列方法中:①向上排空氣法,②向下排空氣法,③排水法.收集氫氣可用( )
A.① B.② C.①③ D.②③ 組卷:46引用:54難度:0.9 -
3.元素的化學性質主要取決于原子的( )
A.最外層電子數 B.核內質子數 C.核外電子總數 D.相同原子質量 組卷:6引用:5難度:0.9 -
4.加油站應貼的標志是( )
A. 
當心爆炸B. 
嚴禁煙火C. 
節能標志D. 
綠色食品組卷:39引用:18難度:0.9 -
5.下列各圖是初中化學常見的幾個實驗操作,其中錯誤的是( )
A. 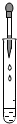
B. 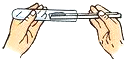
C. 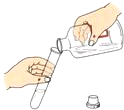
D. 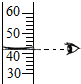 組卷:134引用:111難度:0.9
組卷:134引用:111難度:0.9 -
6.在化學反應A+2B=3C+D中,6gA與8gB恰好完全反應,生成9gD.若反應生成15gC,則參加反應的B的質量為( )
A.8g B.24g C.12g D.16g 組卷:177引用:6難度:0.7 -
7.細心的同學會注意到在面盆、痰盂等鐵制品表面有燒制搪瓷,其目的是( )
A.增大硬度防止撞壞 B.增大厚度防止磨損 C.防止鐵生銹且美觀 D.美觀和殺菌消毒作用 組卷:12引用:7難度:0.9
三、應用(21分)
-
21.某實驗小組為了測定實驗中氯酸鉀樣品的純度,取一定質量的該樣品與1g二氧化錳混合,其總質量為6g。依次加熱該混合物T1、T2、T3、T4時間后,分別冷卻稱量剩余固體質量,記錄的有關數據見如表:
反應的化學方程式為:2KClO3加熱時間 T1 T2 T3 T4 剩余固體質量 4.24g 4.16g 4.08g 4.08g 2KCl+3O2↑MnO2△
(1)完全反應后,固體剩余的物質有和。
(2)完全反應后,產生的氧氣的總質量為,你的依據是。
(3)樣品中氯酸鉀的純度是多少?(氯酸鉀樣品純度是指樣品中氯酸鉀的質量分數)組卷:18引用:2難度:0.1
四、實驗探究(共9分,方程式每個2分)
-
22.九年級化學老師從實驗桌上拿出兩瓶常用的但標簽已經模糊不清的試劑,分別是固體和液體,他取少量試劑在試管中混合,立即產生一種無色氣體。對此氣體展開了一系列探究:
(1)①此氣體是什么物質?驗證它的實驗方案如下:
②我想制取該氣體,發生裝置將選取圖1中的猜 想 驗證猜想的實驗步驟 現象及結論 我認為此氣體可能是 產生此氣體的一個化學方程式是 (填序號,以下同),收集裝置選取。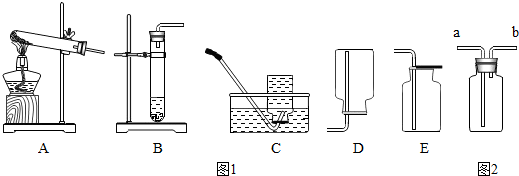
③如果用圖2所示裝置收集我猜想的氣體,我認為氣體應從端(填“a”或“b”)導入。
(2)我猜想無色氣體還可能是另外一種氣體,產生它的其中一個化學方程式是收集裝置可采用圖2中的(填序號)。組卷:52引用:8難度:0.1


