2021-2022學年遼寧省沈陽市高三(上)質檢化學試卷(一)
發布:2024/4/20 14:35:0
一、選擇題:本題共15小題,每小題3分,共45分。在每小題給出的四個選項中,只有一項符合題目要求。
-
1.化學與人類生產、生活密切相關,下列說法中錯誤的是( )
A.鍍鋅鐵破損后,鐵易被腐蝕 B.神舟十一號飛船返回艙表面材料氮化硅屬于共價晶體 C.冷敷袋俗稱冰袋,成分可以是硝酸銨和水 D.紅酒中添加適量SO2可以起到殺菌和抗氧化的作用 組卷:10引用:2難度:0.7 -
2.下列化學用語表示錯誤的是( )
A.CS2 的空間填充模型 
B.N2H4的電子式 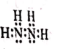
C.二氧化硅的分子式為SiO2 D..Cu的價電子排布式為3d104s1 組卷:11引用:1難度:0.7 -
3.下列說法中正確的是( )
A.明礬可用于對自來水進行殺菌消毒 B.Fe(OH)3 和FeCl2均可通過化合反應得到 C.95%乙醇溶液可以更有效的殺死新冠病毒 D.CO2通入CaCl2溶液中,溶液先變渾濁后變澄清 組卷:11引用:1難度:0.7 -
4.由下列實驗操作及現象能得出相應結論的是( )
選項 實驗操作 實驗現象 結論 A 將蘸有濃氨水的玻璃棒靠近某試劑瓶瓶口 該試劑瓶瓶口有白煙生成 該試劑瓶中盛裝的一定是濃鹽酸 B 向含有酚酞的Na2CO3溶液中加入少量BaCl2固體 溶液紅色變淺 證明Na2CO3溶液中存
在水解平衡C 向未知溶液中滴加硝酸酸化的BaCl2溶液 出現白色沉淀 證明該未知溶液中存在
SO42-或者SO32-D 向Fe(NO3)2溶液中加入稀硫酸 溶液變為棕黃色 稀硫酸具有氧化性 A.A B.B C.C D.D 組卷:11引用:2難度:0.5 -
5.下列有關不同價態含硫化合物的說法錯誤的是( )

A.工業接觸法制備硫酸涉及的轉化為FeS2→X→Y→Z B.實驗室制備乙炔中的硫化氫雜質可用M溶液除去 C.黃鐵礦的主要成分為FeS2,該化合物中陰陽離子個數比為1:1 D.硫在過量氧氣中燃燒能夠生成Y 組卷:44引用:5難度:0.8 -
6.NA是阿伏加德羅常數的值。下列敘述中正確的是( )
A.32gS8 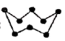 中的共價鍵數目為NA
中的共價鍵數目為NAB.25℃時,pH=1HNO3溶液中含有 的數目為0.1NANO-3C.10g49%硫酸溶液中所含的H原子數為0.1NA D.1mol氨基(-NH2)中含有的電子數為10NA 組卷:4引用:1難度:0.7
二、非選擇題:本題共4小題,共55分。
-
18.2021年9月24日,我國科學家在(Science》上發表論文《無細胞化學酶從二氧化碳合成淀粉》,代表著人類人工合成淀粉領域的重大顛覆性和原創性突破。
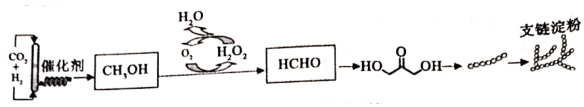
(1)第一步反應CO2和H2制CH3OH的過程中原子利用率(填“能”或“不能”)達到100%。
(2)在第二步反應中,H2O2為。
A.反應物
B.生成物
C.催化劑
D.中間產物
(3)探究CH3OH合成反應的化學平衡影響因素,有利于提高CH3OH的產率。CO2和H2在某種催化劑作用下可同時發生以下兩個反應:
Ⅰ.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)ΔH=-48.5kJ?mol-1
Ⅱ.2CO2(g)+5H2(g)?C2H2(g)+4H2O(g)ΔH=+37.1kJ?mol-1
在壓強為P,CO2、H2的起始投料為1:3的條件下,發生反應I、II,實驗測得CO2的平衡轉化率和平衡時CH3OH的選擇性隨溫度的變化如圖所示。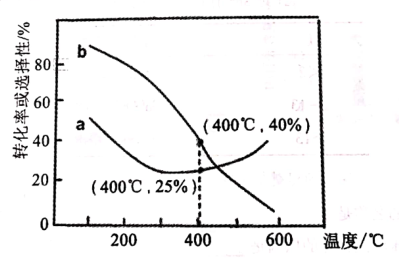
已知:CH3OH的選擇性=×100%CH3OH物質的量反應的CO2物質的量
①有利于提高CH3OH的選擇性的措施有。
A.適當降溫
B.適當升溫
C.選擇合適的催化劑
②溫度高于350℃時,體系中發生的反應以(填“Ⅰ”或“Ⅱ”)為主,并說明理由。
③其中表示平衡時CH3OH的選擇性的曲線是(填“a”或“b”)。
④400℃時,在該壓強及投料比的條件下,利用圖示所給數據計算H2的轉化率為。組卷:14引用:1難度:0.5 -
19.氮及其化合物在工農業生產和生命活動中起著重要的作用。回答下列問題:
(1)“中國制造2025”是中國政府實施制造強國戰略第一 個十年行動綱領。氮化鉻在現代工業中發揮更重要的作用,請寫出Cr3+的價電子軌道表示式;基態鉻、氮原子的未成對電子數之比為。
(2)NH3也是造成水體富營養化的重要原因之一,用NaClO溶液氧化可除去氨氣。其反應機理如圖1所示(其中H2O和NaCl略去)。NaClO 氧化NH3的總反應化學方程式為。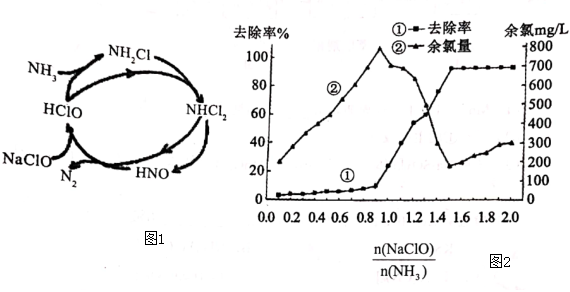
(3)改變對溶液中NaClO去除氨氣效果與余氯(溶液中+1價氯元素的含量)的影響如圖2所示,則除氨氣過程中最佳的n(NaClO)n(NH3)值約為n(NaClO)n(NH3)。
(4)室溫下,用水稀釋0.1mol?L-1氨水,溶液中隨著水量的增加而減小的是。
A.c(NH4+)?c(OH-)c(NH3?H2O)
B.c(NH3?H2O)c(OH-)
C.c(H+)
D.c(OH-)c(H+)
(5)25℃時,將amolNH4NO3溶于水,向該溶液中滴加bL氨水后溶液呈中性,滴加氨水的過程中水的電離平衡將(填“正向”、“逆向”或“不”)移動。
(6)工業上利用NH3制備聯氨(N2H4)裝置如圖,其陽極電極反應式為。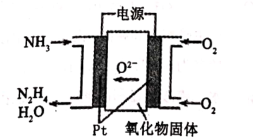 組卷:7引用:1難度:0.5
組卷:7引用:1難度:0.5


