2022-2023學年廣東省廣州六中高二(上)期中化學試卷
發布:2024/11/12 19:0:1
一、選擇題(本題包括10小題,每小題只有一個選項符合題意,每小題3分,共20分)
-
1.下列勞動項目與所述的化學知識沒有關聯的是( )
選項 勞動項目 化學知識 A 以油脂為原料制肥皂 油脂可發生皂化反應 B 面包師用小蘇打作發泡劑烘焙面包 Na2CO3可與酸反應 C 工人將模具干燥后再注入熔融鋼水 鐵與H2O高溫下會反應 D 用84消毒液對圖書館桌椅消毒 含氯消毒劑具有氧化性 A.A B.B C.C D.D 組卷:3引用:2難度:0.6 -
2.在催化劑表面CO2與H2反應的部分歷程如圖所示,吸附在催化劑表面的物種用“?”標注,Ts表示過渡態。下列說法錯誤的是反應歷程( )

A.物質吸附在催化劑表面時通常比其形成的過渡狀態穩定 B.②→③是圖中①至⑥的歷程中的決速步驟 C.③→④的過程中斷裂了非極性共價鍵 D.反應?CO2+H2(g)=?CO+H2O(g)的ΔH<0 組卷:29引用:6難度:0.6 -
3.在測定中和熱的實驗中,下列說法正確的是( )
A.在測定中和熱實驗中需要使用的儀器有:天平、量筒、燒杯、溫度計、玻璃棒 B.完成一次中和反應反應熱測定實驗,溫度計需要使用2次,分別用于測混合液的初始溫度和反應最高溫度 C.用50mL0.55mol/L的NaOH溶液與60mL0.50mol/L的鹽酸反應,測得的中和熱數值偏大 D.使用環形玻璃攪拌棒是為了使反應物充分混合減小實驗誤差 組卷:88引用:2難度:0.7 -
4.關于有效碰撞理論,下列說法正確的是( )
A.能發生有效碰撞的分子不一定是活化分子 B.活化分子之間發生的碰撞一定是有效碰撞 C.增大壓強使容器容積減小,單位體積內活化分子數目增多,化學反應速率加快 D.升高溫度和使用催化劑,均降低反應的活化能,使得活化分子百分數增大,加快化學反應速率 組卷:335引用:2難度:0.7 -
5.將一定量純凈的氨基甲酸銨置于密閉真空容器中(假設容器體積不變,固體試樣體積忽略不計),在恒定溫度下使其達到分解平衡:H2NCOONH4(s)?2NH3(g)+CO2(g)。能判斷該反應已經達到化學平衡的是( )
①v(NH3)正=2v(CO2)逆
②密閉容器中總壓強不變
③密閉容器中混合氣體的密度不變
④密閉容器中混合氣體的平均相對分子質量不變
⑤密閉容器混合氣體的總物質的量不變
⑥密閉容器中CO2的體積分數不變
⑦混合氣體總質量不變A.①②④⑤⑦ B.①②③⑤⑦ C.①④⑤⑥⑦ D.②③④⑤⑥ 組卷:49引用:3難度:0.7 -
6.如圖所示為工業合成氨的流程圖。有關說法不正確的是( )
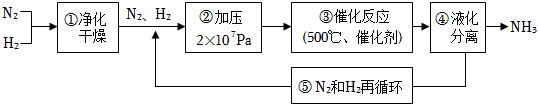
A.步驟①中“凈化”可以防止催化劑中毒 B.步驟②中“加壓”既可以提高原料的轉化率,又可以加快反應速率 C.產品液氨除可生產化肥外,還可用作制冷劑 D.步驟③、④、⑤均有利于提高原料平衡的轉化率 組卷:107引用:11難度:0.7
三、填空題(共56分)
-
19.(1)用0.2000mol/L的標準NaOH溶液滴定未知濃度的鹽酸,其操作可分為如下幾步:
①用蒸餾水洗滌堿式滴定管,注入0.2000mol/L的標準NaOH溶液至“0”刻度線以上;
②固定好滴定管并使滴定管尖嘴充滿液體;
③調節液面至“0”或“0”刻度線稍下,并記下讀數;
④量取20.00mL待測液注入潔凈的錐形瓶中,并加入1~2滴甲基橙溶液;
⑤用標準液滴定至終點,記下滴定管液面讀數。
⑥重復以上滴定操作2~3次。
①以上步驟有錯誤的是(填編號)。
②以下是實驗數據記錄表
從表中可以看出,第1次滴定記錄的NaOH溶液體積明顯多于后兩次的體積,其可能的原因是滴定次數 鹽酸體積/mL NaOH溶液體積讀數/mL 滴定前 滴定后 1 20.00 0.00 18.10 2 20.00 0.00 16.20 3 20.00 0.00 16.16 (填字母)。
A.錐形瓶裝液前,留有少量蒸餾水
B.滴定結束時,俯視計數
C.滴定前滴定管尖嘴有氣泡,滴定結束無氣泡
D.錐形瓶用待測液潤洗
E.NaOH標準液保存時間過長,有部分變質
(2)定量探究2I-+S2=I2+2O2-8的反應速率與反應物濃度的關系。SO2-4
查閱資料:該反應速率與c(S2)和c(I-)的關系為v=kcm(S2O2-8)cn(I-),k為常數。O2-8
實驗任務:測定不同濃度下的反應速率確定m、n的值。
實驗方法:按下表體積用量V將各溶液混合,(NH4)2S2O8溶液最后加入,記錄開始反應至溶液出現藍色所用的時間t。實驗過程中發生如下反應:S2+2I-=2O2-8(慢)+I2;I2+2S2SO2-4=2I-+S4O2-3(快)。實驗記錄表:O2-6
①加入KNO3、(NH4)2SO4溶液的目的是控制實驗條件,其中V1=實驗編號 A B C D E 0.2mol?L-1(NH4)2S2O8溶液/mL 10 5 2.5 10 10 0.2mol?L-1KI溶液/mL 10 10 10 5 2.5 0.05mol?L-1Na2S2O3溶液/mL 3 3 3 3 3 0.2mol?L-1KNO3溶液/mL 0 V1 V2 V3 V4 0.2mol?L-1(NH4)2SO4溶液/mL 0 V5 V6 V7 V8 0.2%淀粉溶液/mL 1 1 1 1 1 t/s t1 t2 t3 t4 t5 ,V4=,V5=。
②當溶液中(填化學式)耗盡后溶液出現藍色。根據實驗A的數據,反應速率v(S2)=O2-8mol?L-1?s-1(列出算式)。
③根據實驗數據可確定m、n的值。n=1的判斷依據是(用t的關系表示)。組卷:63引用:1難度:0.5 -
20.丙烯腈(CH2=CHCN)是一種重要的化工原料,工業上可用“丙烯氨氧化法”生產,主要副產物有丙烯醛(CH2=CHCHO)和乙腈(CH3CN)等,回答下列問題:
(1)以丙烯、氨、氧氣為原料,在催化劑存在下生成丙烯腈(C3H3N)和副產物丙烯醛(C3H4O)的熱化學方程式如下:
C3H6(g)+NH3(g)+O2(g)=C3H3N(g)+3H2O(g)ΔH=-515kJ/mol32
C3H6(g)+O2(g)=C3H4O(g)+H2O(g)ΔH=-353kJ/mol
兩個反應在熱力學上趨勢均很大,其原因是;有利于提高丙烯腈平衡產率的反應條件是;提高丙烯腈反應選擇性的關鍵因素是.
(2)圖(a)為丙烯腈產率與反應溫度的關系曲線,最高產率對應溫度為460℃.低于460℃時,丙烯腈的產率(填“是”或者“不是”)對應溫度下的平衡
產率,判斷理由是;高于460℃時,丙烯腈產率降低的可能原因是(雙選,填標號)
A.催化劑活性降低 B.平衡常數變大 C.副反應增多 D.反應活化能增大
(3)丙烯腈和丙烯醛的產率與n(氨)/n(丙烯)的關系如圖(b)所示.由圖可知,最佳n(氨)/n(丙烯)約為,理由是.進料氣氨、空氣、丙烯的理論體積比約為.組卷:85引用:6難度:0.5


