2021-2022學年江蘇省高二(上)學業水平合格性化學試卷
發布:2025/1/2 10:30:4
一、選擇題:本大題共28題,每小題3分,共計84分。在每小題的四個選項中,只有一個選項符合題目要求。
-
1.中國天宮空間站的太陽翼伸展機構的部件由碳化硅顆粒增強鋁基復合材料(其組成可表示為SiC/Al)制成,該材料不具有的性質是( )
A.耐高溫 B.密度大 C.耐腐蝕 D.抗磨損 組卷:14引用:3難度:0.6 -
2.我國力爭在2060年前實現“碳中和”。1molCO2在標準狀況下體積約為( )
A.1L B.11.2L C.22.4L D.33.6L 組卷:41引用:3難度:0.6 -
3.下列變化涉及化學變化的是( )
A.海水提取溴 B.碘的升華 C.切割大理石 D.液氨汽化 組卷:8引用:2難度:0.8 -
4.下列物質的俗名與化學式對應正確的是( )
A.膽礬——CuSO4 B.酒精——CH3CH2OH C.熟石灰——NaOH D.鐵紅——Fe3O4 組卷:28引用:2難度:0.7 -
5.螢石是一種重要礦物,其主要成分是氟化鈣(CaF2),CaF2屬于( )
A.混合物 B.酸 C.堿 D.鹽 組卷:38引用:3難度:0.8 -
6.下列物質屬于天然高分子化合物的是( )
A.蠶絲 B.聚氯乙烯 C.蔗糖 D.油脂 組卷:48引用:2難度:0.9 -
7.下列物質存在共價鍵的是( )
A.K2S B.MgCl2 C.He D.NH3 組卷:44引用:2難度:0.7 -
8.下列化學用語表示正確的是( )
A.乙烯的結構簡式:C2H4 B.氧原子的結構示意圖 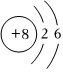
C.H2O的電子式:H:O:H D.KNO3的電離方程式:KNO3═K++N5++3O2- 組卷:28引用:2難度:0.8
二、非選擇題
-
29.硫酸是最重要的化工產品之一,常用于物質的制備、催化等領域。
(1)工業上用硫酸制備硫酸銅。
方案I:將銅與濃硫酸共熱,反應生成硫酸銅。
方案II:向銅與稀硫酸的混合物中持續通入氧氣并加熱,反應原理:2Cu+2H2SO4+O22CuSO4+2H2O。△
①方案I反應的化學方程式為。
②在實驗室中,將濃硫酸稀釋為稀硫酸的操作方法為。
③比較以上兩種制備方案,哪一種方案更好,理由是。
(2)濃硫酸常用作實驗室制取乙酸乙酯的催化劑。制取乙酸乙酯的化學方程式為CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O,乙酸中所含官能團的名稱為濃硫酸△。組卷:13引用:2難度:0.7 -
30.高鐵酸鉀(K2FeO4)為紫黑色固體,易溶于水,微溶于KOH濃溶液,是一種高效凈水劑。一種制備K2FeO4的方法為Cl2與KOH溶液反應生成KClO(在較高溫度下生成KClO、KClO、Fe(OH)3與KOH溶液反應制得K2FeO4)。實驗裝置如圖所示:
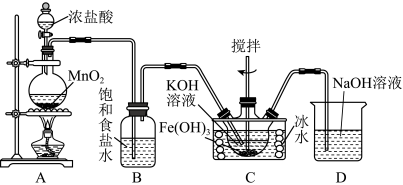
回答下列問題:
(1)裝置B的作用。
(2)裝置C中三頸燒瓶置于冰水浴中的目的是。
(3)充分反應后靜置,取裝置C中上層清液加入飽和KOH溶液,析出紫黑色晶體,過濾。使用飽和KOH溶液的作用是。
(4)實驗室可用間接碘量法測定含少量KCl雜質的K2FeO4樣品的純度:稱取0.1500gK2FeO4樣品溶于堿性KI溶液中,調節pH使混合液充分反應。用0.1000mol?L-1的Na2S2O3標準溶液進行滴定,消耗Na2SO4標準溶液25.00mL。滴定時,發生反應的離子方程式:+4I-+8H+═Fe2++2I2+4H2O;I2+2S2FeO2-4═S4O2-3+2I-。請計算K2FeO4樣品的純度:O2-6(寫出計算過程)。組卷:14引用:1難度:0.5


