2021年天津市南開區高考化學一模試卷
發布:2024/11/19 14:0:1
一.本卷共12題,每題3分,共36分。在每題給出的四個選項中,只有一項是最符合題目要求的。
-
1.下列物品所使用的主要材料不屬于無機非金屬材料的是( )
A. 
石墨烯超輕海綿B. 
宣紙C. 
瓷器D. 
碳化硅陶瓷軸承組卷:98引用:1難度:0.8 -
2.下列有關化學用語表示正確的是( )
A.丙烯的鍵線式: 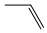
B.N2H4的電子式: 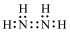
C.基態銅原子的核外電子排布式:3d104s1 D.NH3的VSEPR模型名稱:正四面體 組卷:65引用:1難度:0.6 -
3.下列敘述正確的是( )
A.在水中的溶解度:C2H5OH<CH3OCH3 B.鍵角:NH3<H2O C.電負性:S<Se D.鍵長:HF<HCl 組卷:183引用:4難度:0.5 -
4.短周期元素G、M、W、X、Y、Z的原子半徑及其最高正化合價隨原子序數遞增的變化如圖所示。下列說法正確的是( )
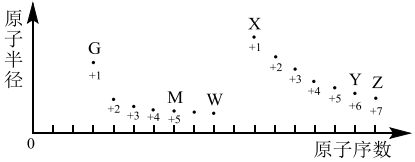
A.堿性:GOH>XOH B.還原性:HW>HZ>H2Y C.酸性:H2YO4>HZO4 D.離子半徑:M3->W->X+ 組卷:142引用:1難度:0.5 -
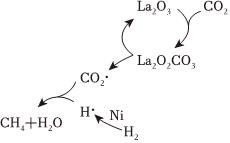 5.2021年中國科學院和中國工程院評選出2020年世界十大科技進展,排在第四位的是一種可借助光將二氧化碳轉化為甲烷的新型催化轉化方法:CO2+4H2═CH4+2H2O,這是迄今最接近人造光合作用的方法,CO2加氫制CH4的一種催化機理如圖。下列說法正確的是( )
5.2021年中國科學院和中國工程院評選出2020年世界十大科技進展,排在第四位的是一種可借助光將二氧化碳轉化為甲烷的新型催化轉化方法:CO2+4H2═CH4+2H2O,這是迄今最接近人造光合作用的方法,CO2加氫制CH4的一種催化機理如圖。下列說法正確的是( )A.反應中La2O3是中間產物 B.CO2轉化為CH4利用了CO2的氧化性 C.H2經過Ni活性中心裂解產生帶負電荷的H? D.使用催化劑可以降低反應的焓變,從而提高化學反應速率 組卷:75引用:3難度:0.5
二、本卷共4題,共64分。
-
15.硫氰化鉀(KSCN)俗稱玫瑰紅酸鉀,是一種用途廣泛的化學藥品。實驗室模擬工業制備硫氰化鉀的實驗裝置如圖所示。
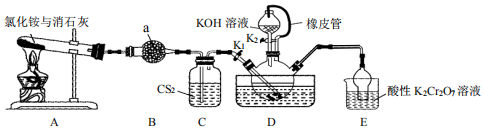
已知:①NH3不溶于CS2,CS2密度比水大且不溶于水;②三頸瓶內盛放:CS2、水和催化劑;③CS2+3NH3NH4SCN+NH4HS,該反應比較緩慢且NH4SCN在高于170℃時易分解。回答下列問題:催化劑液浴加熱
(1)儀器a的名稱為,所裝試劑為。
(2)裝置A中反應的化學方程式為。
(3)裝置D連接橡皮管的作用為。
(4)制備KSCN溶液:熄滅A處的酒精燈,關閉K1,保持三頸瓶內液溫105℃一段時間,然后打開K2,繼續保持液溫105℃,緩緩滴入適量的KOH溶液,寫出裝置D中生成KSCN的化學方程式:。
(5)裝置E的作用為吸收尾氣,防止污染環境,寫出吸收NH3時發生反應的離子方程式:。
(6)制備硫氰化鉀晶體:先濾去三頸瓶中的固體催化劑,再減壓、、過濾、洗滌、干燥,得到硫氰化鉀晶體。
(7)測定晶體中KSCN的含量:稱取12.0g樣品。配成1000mL溶液,量取20.00mL溶液于錐形瓶中,加入適量稀硝酸,再加入幾滴Fe(NO3)3作指示劑,用0.1000mol/L AgNO3標準溶液滴定,達到滴定終點時消耗AgNO3標準溶液18.00mL。
[已知:滴定時發生的反應:SCN-+Ag+═AgSCN↓(白色)。]
①達到滴定終點時的現象為;
②晶體中KSCN的質量分數為。組卷:107引用:1難度:0.5 -
16.工業排放物可能對環境和人體健康產生危害,含SO2、NOx的煙氣必須經過處理才可排放。回答下列問題:
(1)若煙氣主要成分為SO2、NO,可通過電解法除去,其原理如圖所示。陽極的電極反應式為。標準狀況下,22.4L NO完全反應轉移電子數為。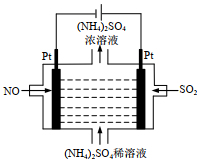
(2)若煙氣主要成分為SO2,可通入NaOH溶液將SO2完全轉化為SO32-。Na2SO3溶液中離子濃度從大到小的順序為。
(3)若煙氣主要成分為NO,O3能有效地氧化NO。
①O3分子的空間結構與水分子的相似,O3是(填“極性”或“非極性”)分子。
②已知:2NO(g)+O2(g)═2NO2(g)△H1=-114kJ?mol-1
2O3(g)═3O2(g)△H2=-284.2kJ?mol-1(活化能Ea=119.2kJ?mol-1)
NO(g)+O3(g)═NO2(g)+O2(g)△H3=kJ?mol-1(活化能Ea=3.2kJ?mol-1)
③NO可經O3處理后再用堿液吸收而實現脫除。為分析氧化時溫度對NO脫除率的影響,將NO與O3混合反應一段時間,再用堿液吸收氧化后的氣體。其他條件相同時,NO脫除率隨NO與O3混合反應時溫度變化情況為,溫度在50~150℃時,隨著溫度升高,NO脫除率無明顯變化;溫度超過150℃時,隨著溫度升高,NO脫除率下降。其可能原因是。
(4)若煙氣主要成分為NO2,用O3氧化NO2時,使用催化劑可提高氧化效率。研究發現NO2在某催化劑表面被O3氧化時反應機理如圖所示,反應過程中,氮氧化物[M]與NO2按物質的量1:1反應生成N2O5,[M]的化學式為。該催化氧化過程總反應的化學方程式為。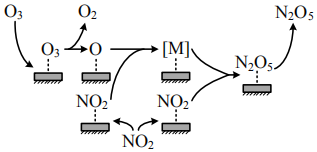 組卷:102引用:1難度:0.4
組卷:102引用:1難度:0.4


