2023-2024學(xué)年廣東省廣州市六校聯(lián)考高二(上)期中化學(xué)試卷
發(fā)布:2024/10/19 14:0:1
一.單項(xiàng)選擇題:本大題包括10小題,每小題2分,共20分.每小題給出的四個選項(xiàng)中,只有一個選項(xiàng)符合題目要求,多選、錯選均不得分.
-
1.下列圖示變化為吸熱反應(yīng)的是( )
A. 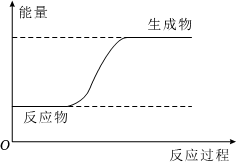
B. 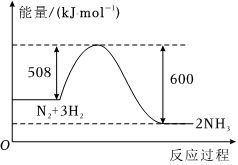
C. 
D. 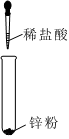 組卷:169引用:12難度:0.5
組卷:169引用:12難度:0.5 -
2.調(diào)控化學(xué)反應(yīng)速率對日常生活和工農(nóng)業(yè)生產(chǎn)都具有重要的意義。下列措施中,主要是通過濃度調(diào)控化學(xué)反應(yīng)速率的是( )
A.茶葉使用真空包裝 B.用鐵礦石煉鐵過程中將礦石粉碎 C.低溫保存疫苗 D.氨在催化劑作用下被氧化成NO 組卷:16引用:4難度:0.5 -
3.下列關(guān)于醋酸和鹽酸的說法正確的是( )
A.醋酸的電離方程式為CH3COOH═H++CH3COO- B.CH3COOH溶液中存在電離平衡,而鹽酸中不存在電離平衡 C.CH3COOH達(dá)到電離平衡時,溶液中檢測不出CH3COOH分子 D.醋酸溶液的導(dǎo)電能力不一定比鹽酸弱 組卷:29引用:1難度:0.8 -
4.在一定溫度下,可逆反應(yīng)A(g)+2B(g)?2C(g)達(dá)到平衡的標(biāo)志是( )
A.A的消耗速率與C的消耗速率相等 B.單位時間內(nèi)生成nmolA的同時生成2nmolB C.A、B的物質(zhì)的量之比為2:1 D.A、B、C的濃度都不再變化 組卷:20引用:1難度:0.7 -
5.已知COS(g)+H2(g)?H2S(g)+CO(g)ΔH=-17kJ?mol-1,則在一定條件下向密閉容器中充入1molCOS(g)和1molH2(g),充分反應(yīng),放出的熱量( )
A.大于17kJ B.等于17kJ C.小于17kJ D.上述都有可能 組卷:58引用:1難度:0.8 -
6.下列各組關(guān)于強(qiáng)電解質(zhì)、弱電解質(zhì),非電解質(zhì)的歸類,完全正確的是( )
選項(xiàng) A B C D 強(qiáng)電解質(zhì) Fe NaCl CaCO3 HNO3 弱電解質(zhì) CH3COOH NH3 H3PO4 Fe(OH)3 非電解質(zhì) 蔗糖 BaSO4 酒精 Cl2 A.A B.B C.C D.D 組卷:135引用:11難度:0.8
三、非選擇題(本題包括4個小題,共56分)
-
19.合成氨對人類的生存和發(fā)展有著重要意義,1909年哈伯在實(shí)驗(yàn)室中首次利用氮?dú)馀c氫氣反應(yīng)合成氨,實(shí)現(xiàn)了人工固氮。
(1)請結(jié)合下列數(shù)據(jù)分析,工業(yè)上選用氮?dú)馀c氫氣反應(yīng)固氮,而沒有選用氮?dú)夂脱鯕夥磻?yīng)固氮的原因是。
(2)合成氨的反應(yīng)原理為N2(g)+3H2(g)?2NH3(g);在一容積為2L的密閉容器中加入一定量的N2和0.5molH2,在一定條件下發(fā)生合成氨反應(yīng),反應(yīng)中NH3的物質(zhì)的量濃度的變化情況如圖序號 化學(xué)反應(yīng) K(298K)的數(shù)值 ① N2(g)+O2(g)?2NO(g) 5×10-31 ② N2(g)+3H2(g)?2NH3(g) 4.1×106 
①根據(jù)圖,計(jì)算從反應(yīng)開始到平衡時,平均反應(yīng)速率v(N2)=。
②平衡時測得N2的物質(zhì)的量為0.10mol,則的轉(zhuǎn)化率α(N2)=,該溫度下的平衡常數(shù)K=。
(3)對于反應(yīng)N2(g)+3H2(g)?2NH3(g),在一定條件下氨的平衡含量如下表。
①該反應(yīng)為溫度/℃ 壓強(qiáng)/MPa 氨的平衡含量 200 10 81.5% 550 10 8.25% (填“吸熱”或“放熱”)反應(yīng)。
②其他條件不變時,溫度升高,氨的平衡含量減小的原因是。
③哈伯選用的條件是550℃、10MPa,而非200℃、10MPa,可能的原因是。組卷:14引用:1難度:0.5 -
20.下表是幾種常見弱酸的電離平衡常數(shù)(25℃),回答下列各題:
(1)當(dāng)溫度升高時,Ka酸 CH3COOH H2CO3 HCN H2C2O4 電離平衡常數(shù)(Ka) 1.8×10-5 Ka1=4.2×10-7
Ka2=5.6×10-115×10-10 Ka1=5.4×10-2
Ka2=5.4×10-5(填“增大”、“減小”或“不變”)。
(2)等濃度的CH3COOH溶液和HCN溶液,導(dǎo)電性較弱的是。能使氫氰酸溶液中HCN的電離程度增大,而電離平衡常數(shù)不變的操作是(任寫其中一種)。根據(jù)上表數(shù)據(jù)判斷草酸(H2C2O4)和碳酸鈉溶液能否反應(yīng),如果不能反應(yīng)說出理由,如果能發(fā)生反應(yīng)請寫出相應(yīng)的離子方程式:。
(3)寫出草酸(H2C2O4)的一級電離方程式:。Ka1?Ka2的原因是。
(4)請?jiān)O(shè)計(jì)一個簡單的實(shí)驗(yàn)方案驗(yàn)證醋酸與碳酸的酸性強(qiáng)弱:。組卷:22引用:1難度:0.5


