2024年福建省泉州市中考化學模擬試卷(一)
發布:2025/6/29 10:0:9
一、選擇題:本題共10小題,每小題3分,共30分。四個選項中,只有一項符合題目要求。
-
1.世界充滿著各種各樣的變化,下列變化都屬于化學變化的一組是( )
A.濕衣服晾干、鐵鍋生銹 B.汽油燃燒、動植物呼吸 C.小草發芽、酒精揮發 D.冰雪融化、葡萄釀酒 組卷:30引用:2難度:0.8 -
2.下列圖示與相應的文字描述完全符合的是( )
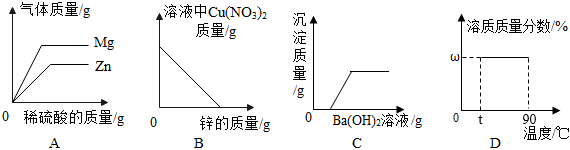
A.向等質量的鎂、鋅中,分別加入同濃度的稀硫酸 B.向裝有硝酸銅和硝酸銀混合溶液的燒杯中逐漸加入金屬鋅 C.向H2SO4和MgCl2的混合溶液中逐滴加入Ba(OH)2溶液至過量 D.t℃時取溶質質量分數為ω的KNO3飽和溶液20g,升高溫度至90℃ 組卷:213引用:3難度:0.5 -
3.某環保興趣小組的同學為證明當地硫酸工廠排出的廢水呈酸性(忽略其他因素的影響),設計了以下四種實驗方案進行檢測,其中不能達到目的的是( )
A.取樣,滴在pH試紙上 B.取樣,向其中加入氫氧化鈉溶液 C.取樣,向其中加入鋅粒 D.取樣,向其中滴加紫色石蕊溶液 組卷:243引用:6難度:0.8 -
4.2022年北京冬奧會是全球的冰雪盛會,下列舉措不符合“綠色冬奧”的是( )
A.開發新能源,減少化石燃料的使用 B.推廣使用清潔能源車輛 C.為方便運動員用餐,大量使用一次性木筷 D.使用不破壞臭氧層的二氧化碳作制冷劑制冰 組卷:13引用:3難度:0.8 -
5.甲、乙兩種物質的溶解度曲線如圖。則下列說法錯誤的是( )

A.t1℃時,甲和乙的溶解度相等 B.乙對應的a點狀態下的溶液是飽和溶液 C.在t1℃時,將100g甲物質加入到50g水中,充分溶解后恢復到原溫度,所得溶液的質量為140g D.將t1℃的甲、乙兩種物質的飽和溶液分別升溫至t3℃,兩溶液溶質的質量分數不相等 組卷:59引用:3難度:0.5 -
6.安徽綠茶享譽全國.綠茶中的茶多酚(化學式為C22H18O11)等活性物質具解毒和抗輻射作用,綠茶是一種健康飲品.有關茶多酚的描述正確的是( )
A.茶多酚是氧化物 B.茶多酚由碳、氫、氧三種元素組成 C.茶多酚中各元素的質量比為22:18:11 D.每個茶多酚分子里含有9個氫氣分子 組卷:2引用:1難度:0.9 -
7.布洛芬(中文別名異丁苯丙酸)的分子式是C13H18O2,是一種常用的解熱鎮痛類非處方藥,具有抗炎、鎮痛、解熱作用。下列說法正確的是( )
A.1個布洛芬分子中共含有33個原子 B.布洛芬從物質的分類上屬于混合物 C.布洛芬中碳、氫元素的質量比為13:18 D.布洛芬中氫元素的質量分數最大 組卷:44引用:2難度:0.8 -
8.在進行化學實驗時,必須規范實驗操作,以下的實驗操作中正確的是( )
A. 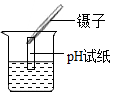
測定溶液的pHB. 
稱量固體C. 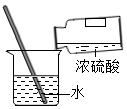
稀釋濃硫酸D. 
干燥氣體組卷:16引用:2難度:0.8 -
9.下列化學用語表示正確的是( )
A.2個氫原子:H2 B.n個鎂離子:nMg-2 C.氯化亞鐵:FeCl3 D.氧原子結構示意圖:  組卷:18引用:1難度:0.8
組卷:18引用:1難度:0.8 -
 10.KCl和 KNO3的溶解度(如表)和溶解度曲線(如圖)。下列說法正確的是( )
10.KCl和 KNO3的溶解度(如表)和溶解度曲線(如圖)。下列說法正確的是( ) 溫度/℃ 0 10 20 30 40 50 60 溶解度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 KCl 27.6 31.0 34.0 37.0 40.0 42.6 45.5 A.曲線甲代表KCl的溶解度曲線 B.40℃時KNO3飽和溶液中 KNO3的質量分數為63.9% C.t1的值在20~30之間 D.將t1℃時甲和乙的飽和溶液升溫至t2℃時,溶液中溶質的質量分數:甲>乙 組卷:344引用:5難度:0.5
二、非選擇題:本題共8小題,共70分。
-
11.分類學習是化學學習中常用的方法,通過按一定標準分類研究,往往可以收到事半功倍的效果.
(1)我們在初中階段將化合物簡單分為氧化物、酸、堿、鹽等.根據鹽的組成里所含陰、陽離子的特點,可進一步將鹽分類并稱為某鹽.例如,組成里含有碳酸根離子的鹽稱為碳酸鹽,含有鉀離子的鹽稱為鉀鹽,含有銨根離子的鹽稱為銨鹽….則CaCO3、Na2CO3、K2CO3等鹽都屬于;它們都能與稀鹽酸反應生成氣體.
(2)物質燃燒需要三個條件:可燃物、、溫度達到著火點,這三個條件缺一不可,因此,只要破壞燃燒的條件,就可以實現滅火.鐵在潮濕的空氣中易生銹,實際上是鐵與空氣中的、水蒸氣等發生化學反應的過程,同理,只要破壞鐵制品銹蝕的條件,就能防銹,請任舉一例防止鐵制品銹蝕的具體方法:.
(3)僅含碳和氫兩種元素的有機物稱為烴,如烷烴、烯烴、炔烴等.烷烴中最簡單的是甲烷(CH4),其余隨碳原子數的增加,依次為乙烷(C2H6)、丙烷(C3H8)、丁烷(C4H10)等.如果烷烴中的碳原子數為n,則烷烴的化學式可以用通式表示.它們在氧氣中完全燃燒的產物都是二氧化碳和水,試寫出甲烷在空氣中充分燃燒的化學方程式:.組卷:43引用:4難度:0.5 -
12.小明同學取下列生活中的物質,測得其pH如表所示:
由此判斷:物質 肥皂水 雨水 糖水 檸檬汁 洗潔精 pH 10.2 5.2 7.0 2.5 12.2
(1)酸性最強的物質是.
(2)能使無色酚酞試液變紅色的物質是(填一種物質即可).
(3)小明生活的環境所降的雨水(填“屬于”或“不屬于”)酸雨.
(4)橄欖油中含有多種物質,油酸(單不飽和脂肪酸):70-80%,亞油酸(多不飽和脂肪酸):6-9%,棕櫚酸(飽和脂肪酸):7-15%,另外還含有維生素A和E.油酸的化學式為C18H34O2.
①橄欖油是(選填“純凈物”、“混合物”).
②油酸完全燃燒的化學方程式是.組卷:25引用:2難度:0.9 -
13.在牙膏中常用輕質碳酸鈣粉末作摩擦劑,小強在實驗室用石灰石(雜質不反應也不溶于水)為原料制取輕質碳酸鈣和氫氧化鈉。

(1)操作②的名稱是。
(2)溶液M中的溶質是,得到輕質碳酸鈣的化學方程式為。
(3)為驗證加入Na2CO3溶液后,溶液M中的溶質是否反應完全,可取上層清液加入進行檢驗。組卷:8引用:1難度:0.5 -
14.實驗室有下列儀器和高錳酸鉀、氯酸鉀兩種藥品及升降臺、火柴兩種實驗用品。請回答下列問題:

(1)利用上述儀器和藥品可制取氧氣,需要補充的實驗用品是;制取該氣體的化學反應原理;制取該氣體所選擇的儀器是(填儀器序號);
(2)此實驗中儀器③的用途是;
(3)收集完所需氧氣,停止加熱時的實驗操作是。組卷:41引用:1難度:0.7 -
15.過氧化鈣(CaO2)為白色粉末,是一種用途廣泛的優良供氧劑。工業上可用碳酸鈣作原料制備過氧化鈣,某校活動小組同學模擬工業制備過氧化鈣樣品并測定其純度。
[實驗一]提純碳酸鈣
已知:“轉化”步驟中的反應方程式為:CaCl2+2NH3+CO2+H2O═CaCO3↓+2NH4Cl。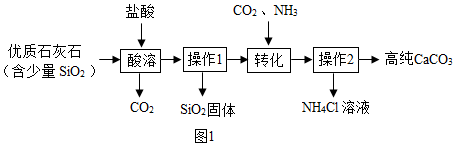
(1)酸溶過程中發生反應的化學方程式是。
(2)該流程(如圖1)中可循環利用的物質為。
[實驗二]過氧化鈣的制備:
已知:①CaCl2+H2O2+2NH3?H2O+6H2═CaO2?8H2O↓+2NH4Cl。
②CaO2?8H2O在0℃時穩定,加熱至130℃會完全脫水變為CaO2。
③CaO2在350℃開始時分解,生成氧化鈣及氧氣。完全分解的溫度為425℃。
(3)沉淀流程(如圖2)中為控制溫度為0℃左右,在實驗室宜采取的方法為。
(4)操作A在實驗室常用的步驟有、降溫結晶、過濾、洗滌、干燥,此操作中洗滌晶體時不可選用的洗滌劑為(填字母)。
A.冰水
B.40℃熱水
C.飽和NH4Cl溶液
(5)最后烘干得到過氧化鈣時,適宜的溫度范圍為。
[實驗三]過氧化鈣含量的測定
已知:①過氧化鈣在濕空氣、遇水反應緩慢地釋放出氧氣。
②過氧化鈣易和酸反應生成H2O2,CaO2+2HCl═CaCl2+H2O2(放熱)。
③過氧化鈣樣品中其他雜質不與鹽酸反應生成氣體。
該小組取樣品1.5g,設計如圖3裝置,通過測O2體積,計算樣品中CaO2的質量分數。
(6)實驗中MnO2的作用是。
(7)相同條件下,能使測定結果更準確(填“裝置A”或“裝置B”)。
實驗步驟如下:a.連接裝置并;
b.稱量樣品的質量1.5g;
c.裝藥品,調節量氣裝置兩邊液面相平,讀取量氣管刻度為10mL;
d.向廣口瓶內加入稀鹽酸,充分反應;
e.;
f.再次調節量氣裝置兩邊液面相平,讀取量氣管刻度為234mL。
(8)請將上述實驗步驟a、e補充完整;
(9)若標準狀況下,每32g氧氣的體積為22.4L。根據實驗數據計算樣品中CaO2的質量分數(寫出計算過程,結果保留到0.1%)。
反思:若其他操作均正確,僅因下列因素可使測定結果偏小的是(填字母)。
A.廣口瓶中殘留少量O2
B.烘干時溫度過高,生成了部分CaO
C.稀鹽酸的用量不足
D.步驟f中沒有調節量氣裝置兩邊液面相平,直接讀數組卷:143引用:2難度:0.5 -
 16.水是一種重要的資源,愛護水資源,人人有責。
16.水是一種重要的資源,愛護水資源,人人有責。
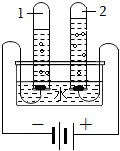
(1)如圖所示,電解水的實驗中,回答下列問題。
①通電一段時間后,試管1中收集到的氣體是(用符號表示),檢驗方法:。
②實驗結論:水是由組成的。寫出電解水的文字表達式。
③電解水時常加入氫氧化鈉,目的是。若收集到的氧氣和氫氣的體積比小于1:2,原因可能是。
(2)生活中我們常使用活性炭制作凈水器濾芯是利用它的性,生活中常用的方法降低水的硬度。
(3)消毒劑高鐵酸鈉(Na2FeO4)集氧化、吸附、凝聚、殺菌等功能于一體,目前被廣泛應用于自來水凈化。高鐵酸鈉中鐵元素的化合價為。
(4)進行過濾操作時,下列做法錯誤的是。
A.玻璃棒要靠在三層濾紙的一邊
B.漏斗下端的管口要緊靠燒杯內壁
C.濾紙的邊緣要低于漏斗口
D.液面不要低于濾紙邊緣組卷:10引用:1難度:0.6 -
17.為了弄清銅綠的組成和銅生成銅綠的條件,某化學實驗小組進行了如下探究:
1、探究銅綠的組成
【查閱資料】通過查閱資料知道:銅綠受熱易分解。
【設計與實驗】
(1)小芳從其它銅器上取下適量的干燥銅綠,按圖1所示裝置進行實驗。在實驗過程中,觀察到:試管口內有水珠出現,說明了銅綠中含有氫、氧元素;澄清石灰水變渾濁,說明了銅綠中含有元素。
(2)小芳取下少量試管內反應后的剩余物,放入另一支試管中,滴入稀硫酸,充分反應后,溶液變藍色,說明銅綠中含有元素。
【實驗結論】銅綠是由銅、氫、氧和碳元素組成的。
2、探究銅生成銅綠的條件【查閱資料】銅綠的化學式是Cu2(OH)2CO3,它受熱會分解生成三種氧化物。銅綠分解的化學方程式為。
【猜想與假設】據銅綠的組成和查閱的資料判斷,銅綠可能是銅與氧氣及共同作用而形成的。
【設計與實驗】借鑒課本“鐵釘銹蝕條件的探究”實驗,小梁設計了“銅片銹蝕條件的探究”實驗,實驗如圖2所示(所用銅片潔凈、光亮,試管內的“ ”為銅片):
”為銅片):
實驗較長時間后,發現試管中銅片最先生銹(填試管字母編號)。
【評價與改進】小區認為小梁設計的實驗還不夠完善,要得出正確的結論,還要補充一個實驗。你認為要補充的一個實驗是。組卷:11引用:1難度:0.5 -
18.1869年俄國化學家門捷列夫在編制元素周期表時曾預言31號“類鋁”元素,1875年布瓦博得證明了這種元素--鎵(Ga)的存在,并證明了它的化學性質和鋁相似,和鋁的化合價一致。
(1)寫出金屬鎵和硫酸反應的化學方程式。
(2)足量的鎵與100g溶質質量分數為9.8%的硫酸充分反應,生成H2的質量為多少。組卷:77引用:1難度:0.6


