2019-2020學年浙江省臺州市臨海市東塍中學九年級(上)月考化學試卷(三)
發布:2025/6/30 2:0:9
一、選擇題(每小題4分,共16分,每小題只有一個正確答案,多選、少選均不給分)
-
1.如圖所示四個圖像中,能正確反映對應變化關系的是( )
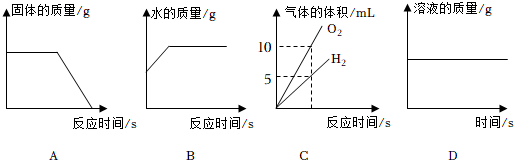
A.一定條件下氧化銅和炭粉恰好完全反應 B.向一定量稀鹽酸中加入石灰石顆粒 C.將水通電電解一段時間 D.飽和石灰水敞口放置一段時間 組卷:35引用:1難度:0.5 -
2.邏輯推理是化學學習中常用的思維方法。下列推理中正確的是( )
A.氯化銨與熟石灰混合研磨能放出氨氣,因此所有氮肥均不能與堿性化肥混合使用 B.活潑金屬和酸反應有氣體產生,則與酸反應產生氣體的物質一定是活潑金屬 C.元素的種類是由質子數決定的,則質子數相同的原子屬于同種元素 D.氧化物中含有氧元素,則含有氧元素的化合物一定是氧化物 組卷:27引用:2難度:0.6 -
3.利用圖 1 裝置進行實驗,先后將溶液快速全部推入,測得一段時間內壓強變化如圖2所示。下列說法不正確的是( )

A.先推入的是NaOH溶液 B.最終壓強比初始壓強小,可能是因為有部分二氧化碳溶于水 C.BC段,CO2與NaOH溶液反應基本停止 D.D點壓強比初始瓶內壓強大,此時瓶內二氧化碳氣體的量比初始多 組卷:547引用:7難度:0.5 -
4.在氯化銅和氯化亞鐵的混合溶液中加入一定的鎂粉,充分反應后過濾,向濾出的固體中滴加稀鹽酸,沒有氣泡產生.下列判斷正確的是( )
A.濾出的固體中一定含有銅,可能含有鐵和鎂 B.濾出的固體中一定含有銅,一定不含有鐵和鎂 C.濾液中一定含有氯化鎂和氯化亞鐵,一定沒有氯化銅 D.濾液中一定含有氯化鎂、氯化亞鐵、氯化銅 組卷:597引用:23難度:0.9
二、填空題(每空2分,共40分)
-
5.某同學配制50g5%氯化鈉溶液,整個操作過程如圖所示,回答下列問題:
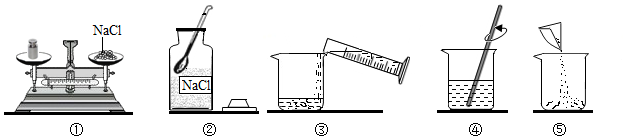
(1)配制溶液的正確操作順序為(填序號,下同),其中操作錯誤的是。
(2)圖②中盛放氯化鈉固體的儀器名稱是,需稱取氯化鈉g。
(3)量水時選用的量筒的量程最合適的是(填序號),讀數時視線要與量筒內保持水平。
A.10mL B.25mL C.50mL D.100mL
(4)經檢測,該同學配制的溶液溶質質量分數偏小,可能的原因是(填序號)。
A.氯化鈉固體不純 B.用生銹砝碼稱量 C.溶解時燒杯內壁有水珠 D.裝瓶時有少量溶液灑出。組卷:111引用:3難度:0.5 -
6.(1)溴元素在元素周期表中的信息與溴原子結構示意圖如圖1、2所示,則n=
。寫出與溴元素化學性質相似的一種元素的元素符號,溴化鈉的化學式為。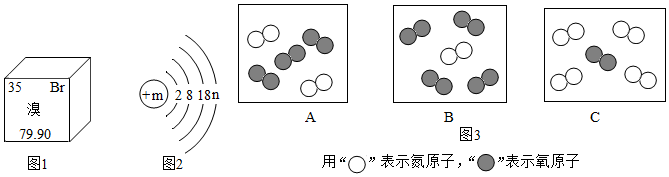
已知:同溫同壓下,氣體的體積比等于其分子個數比。若空氣中其它成分忽略不計,圖3可表示空氣微觀模型的是(填字母)。
(2)水是人類重要的資源。
①目前可供人類使用的淡水資源緊缺。因此,我們要節約用水,提高用水效率。請你寫出一條節約用水的措施。
②水曾被誤認為是一種“元素”。下列實驗能證明水是由氫、氧兩種元素組成的是。
a.水的電解 b.水的蒸發 c.氫氣在氧氣中燃燒
③硬水給生活和生產帶來很多麻煩,生活中常用的方法降低水的硬度,除去硬水中過多的Ca2+和(填離子符號)就可以得到軟水。
(3)2017年5月18日,中國在南海成功試采可燃冰,它將推動世界能源利用格局的改變。可燃冰是在高壓低溫環境條件下,水分子籠中裝有甲烷分子而成的“冰塊”,可直接點燃。已知某種可燃冰的化學式為:CH4?8H2O.請回答:
①這種可燃冰中碳、氫、氧元素質量比是C:H:O=;
②這種可燃冰的質量為g時,與44g二氧化碳所含碳元素質量相等。組卷:16引用:2難度:0.5 -
7.已知反應:
(1)3H2+Fe2O32Fe+3H2O;△
(2)3CO+Fe2O32Fe+3CO2高溫
H2和CO在這兩個反應中均將Fe2O3還原為Fe,在反應中作還原劑.
(1)請你分析上述反應,還原劑中元素化合價在化學反應前后的變化情況,歸納出化學反應中還原劑所含元素化合價變化的規律.
(2)請根據你得出的規律,判斷反應:Mg+CuCl2═MgCl2+Cu中的還原劑是.
(3)在化學反應中與還原劑中元素化合價變化規律相反的物質,被稱為氧化劑,則化學反應:Cl2+2NaBr═Br2+2NaCl中的氧化劑是.組卷:501引用:2難度:0.9 -
8.要除去FeSO4中含有的CuSO4雜質.可以在其溶液中加入
充分反應,反應的化學方程式是:.組卷:6引用:1難度:0.5
三、實驗探究題(每空3分,共45分)
-
9.如圖所示為實驗室中常見氣體制備、凈化、干燥、收集和進行實驗探究的部分儀器(組裝實驗裝置時,可重復選擇儀器),化學小組的同學利用其進行下列化學實驗。
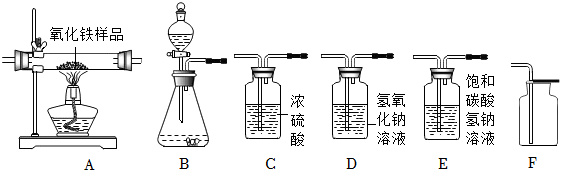
請根據題目要求,回答下列問題:
(1)以石灰石和稀鹽酸為原料,在實驗室中制備并收集一瓶干燥且不含HCl的二氧化碳氣體,按照要求設計實驗裝置,連接儀器,檢查裝置的氣密性,進行實驗。(提示:鹽酸中揮發出的少量HCl氣體可用飽和碳酸氫鈉溶液吸收)
①所選儀器的連接順序為(從左到右填寫儀器序號字母)。
②上述方法制取二氧化碳的化學方程式為。
③向一個收集滿二氧化碳氣體的集氣瓶中,同時放入一張干燥的藍色石蕊試紙和一張濕潤的藍色石蕊試紙,觀察到干燥的試紙不變色,而濕潤的試紙變紅。請敘述出現上述兩種不同現象的原因:
(2)化學小組的同學用一氧化碳氣體(含少量水蒸氣),測定某氧化鐵樣品(雜質為鐵粉)中Fe2O3的質量分數,設計了實驗方案,所選儀器按“CO(含少量水蒸氣)→C→A→D1→D2”的順序連接(D1、D2為氫氧化鈉洗氣瓶),檢查裝置的氣密性,然后進行實驗。(假設發生的化學反應都充分反應)
①該裝置中,洗氣瓶C的作用為
②進行實驗時,檢查完裝置的氣密性,在儀器A硬質玻璃管中放入12g該氧化鐵樣品后,進行以下操作,其中應該先進行的是(填選項序號之一)。
a.用酒精燈加熱
b.通入一氧化碳氣體(含少量水蒸氣)
③反應充分進行后冷卻,測得此時洗氣瓶C增重1.8g,洗氣瓶D1增重6.6g,則12g該氧化鐵樣品中Fe2O3的質量分數為(計算結果精確至0.1%),該氧化鐵樣品中鐵元素與氧元素的質量比為(填最簡整數比)。
④從環保角度考慮,該套實驗裝置還存在明顯的不足之處,你的具體改進建議是。組卷:691引用:3難度:0.4 -
10.(1)在宏觀、微觀、符號之間建立聯系,是化學學科特有的思維方式。
?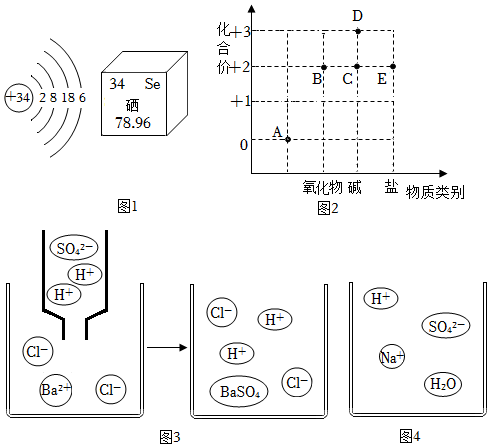
①圖1是硒元素在元素周期表中的相關信息和硒的原子結構示意圖。硒原子的相對原子質量為硒原子在化學反應中容易得到電子,形成的離子符號為。
②以化合價為縱坐標,以物質的類別為橫坐標所繪制的圖像叫價類圖。如圖2為鐵的價類圖。寫出一個由C通過中和反應轉化為E的化學方程式。
③稀鹽酸不能與氯化鋇溶液反應,而稀硫酸則能與之反應生成白色沉淀,根據圖3從微觀角度分析實際參加反應的微粒是(用符號表示)。
④通過分析組成和結構,可以預測物質的某些性質。根據圖4硫酸氫鈉溶液的微觀圖示,分析推測的性質,其中合理的是。
A.硫酸氫鈉溶液中含有氫離子,所以硫酸氫鈉屬于酸
B.硫酸氫鈉溶液能與碳酸鈉反應
C.硫酸氫鈉溶液能與銅粉反應生成氫氣
D.硫酸氫鈉溶液能與硝酸鋇溶液反應生成硫酸鋇沉淀
(2)金屬材料在生活中被廣泛應用,回答下列問題。
①合金在生活中應用非常廣泛,下列關于合金敘述中正確的是(填序號)。
A.合金中至少含有兩種金屬;
B.合金一定是混合物;
C.合金中元素以化合物形式存在;
D.合金的硬度一般比組成它的純金屬更高,抗腐蝕性也更好;
E.焊錫焊接金屬利用了熔點高的特性。
②同學們在實驗室進行“探究金屬的性質”實驗。將鋅粉和鐵粉的混合物加入到盛有一定量硝酸銀溶液的燒杯中,充分反應后過濾,得到濾渣和濾液。將所得濾渣放入稀鹽酸中,有氣泡產生,則濾渣中一定含有。
③某興趣小組探究Zn、Fe、Cu、Ag四種金屬的活動性,進行如圖中甲、乙、丙三個實驗。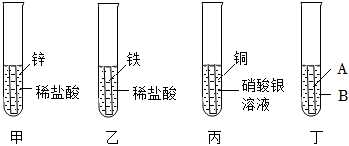 ?
?
A.甲、乙、丙三個實驗反應后溶液顏色各不相同,請寫出反應過程中溶液顏色變為淺綠色的化學反應方程式。
B.小紅同學隨后發現該實驗無法得出四種金屬的活動性順序。于是又補充圖丁實驗,最終得出四種金屬活動性順序為:Zn>Fe>Cu>Ag,若A為金屬鐵,則試劑B為溶液。組卷:67引用:1難度:0.3
四、解答題
-
11.含有蔗糖晶體的溶液A,從冰箱里取出放置一段時間后,晶體慢慢消失,形成溶液B.對于溶液A和B來說,一定處于飽和狀態的是
;兩者相比,較濃的溶液是.組卷:27引用:4難度:0.3 -
12.實驗室用鋅粒和稀硫酸反應制取氫氣。試計算實驗室制取0.4g氫氣,理論上需要消耗金屬鋅的質量?
組卷:5引用:2難度:0.6 -
13.牙膏中的摩擦劑可以增強牙膏對牙齒的摩擦作用和去污效果。已知某品牌牙膏中的摩擦劑是CaCO3和SiO2(SiO2不溶于水也不與稀鹽酸反應)。為了測定摩擦劑中 CaCO3的質量分數,通過實驗測得如圖數據:

(1)生成CO2的質量為g;
(2)求摩擦劑中CaCO3的質量分數(寫出必要的計算過程)。組卷:133引用:8難度:0.7


