2020-2021學年河北省衡水十四中高一(下)三調化學試卷
發布:2024/12/13 8:30:2
一、單選題(共15個小題,每小題2分,共30分。每小題只有一個選項符合題意)
-
1.“灌鋼法”是我國古代勞動人民對鋼鐵冶煉技術的重大貢獻,陶弘景在其《本草經集注》中提到“鋼鐵是雜煉生鍒作刀鐮者”。“灌鋼法”主要是將生鐵和熟鐵(含碳量約0.1%)混合加熱,生鐵熔化灌入熟鐵,再鍛打成鋼。下列說法錯誤的是( )
A.鋼是以鐵為主的含碳合金 B.鋼的含碳量越高,硬度和脆性越大 C.生鐵由于含碳量高,熔點比熟鐵高 D.冶煉鐵的原料之一赤鐵礦的主要成分為Fe2O3 組卷:615引用:11難度:0.9 -
2.高分子材料在生產生活中應用廣泛。下列說法錯誤的是( )
A.蘆葦可用于制造黏膠纖維,其主要成分為纖維素 B.聚氯乙烯通過加聚反應制得,可用于制作不粘鍋的耐熱涂層 C.淀粉是相對分子質量可達幾十萬的天然高分子物質 D.大豆蛋白纖維是一種可降解材料 組卷:708引用:12難度:0.7 -
3.“天問一號”著陸火星,“嫦娥五號”采回月壤。騰飛中國離不開化學,長征系列運載火箭使用的燃料有液氫和煤油等化學品。下列有關說法正確的是( )
A.煤油是可再生能源 B.H2燃燒過程中熱能轉化為化學能 C.火星隕石中的20Ne質量數為20 D.月壤中的3He與地球上的3H互為同位素 組卷:400引用:12難度:0.8 -
4.NA為阿伏加德羅常數的值。下列敘述正確的是( )
A.18g重水(D2O)中含有的質子數為10NA B.3mol的NO2與H2O完全反應時轉移的電子數為4NA C.32g環狀S8( 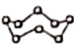 )分子中含有的S-S鍵數為NA
)分子中含有的S-S鍵數為NAD.密閉容器中1mol PCl3和1mol Cl2反應制備PCl5(g),增加2NA個P-Cl鍵 組卷:25引用:1難度:0.6 -
5.最新報道:科學家首次用X射線激光技術觀察到CO與O在催化劑表面形成化學鍵的過程。反應過程的示意圖如下:下列說法正確的是( )
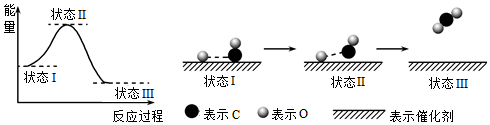
A.CO和O生成CO2是吸熱反應 B.在該過程中,CO斷鍵形成C和O C.CO和O生成了具有極性共價鍵的CO2 D.狀態Ⅰ→狀態Ⅲ表示CO與O2反應的過程 組卷:545引用:88難度:0.7 -
6.一定條件下,對于反應A2(g)+3B2(g)?2AB3(g)來說,下列所表示的化學反應速率中最大的是( )
A.v(A2)=0.8 mol/(L?s) B.v(A2)=6 mol/(L?min) C.v(AB3)=1.0 mol/(L?s) D.v(B2)=1.2 mol/(L?s) 組卷:35引用:4難度:0.5 -
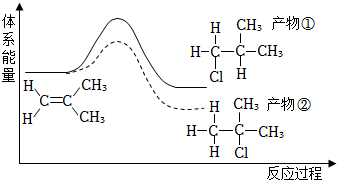 7.異丁烯與氯化氫發生加成反應過程體系能量變化如圖所示,下列敘述正確的是( )
7.異丁烯與氯化氫發生加成反應過程體系能量變化如圖所示,下列敘述正確的是( )A.產物②比產物①更穩定 B.此過程中只發生了非極性鍵的斷裂 C.異丁烯與氯化氫的加成反應為吸熱反應 D.1mol產物①或②中均含有7mol共價鍵 組卷:192引用:6難度:0.7 -
8.已知X(g)+3Y(g)?2W(g)+M(s),一定溫度下,在容積為1L密閉容器中,加入1mol X(g)與1mol Y(g),2s后Y的物質的量濃度為0.4mol/L,下列說法正確的是( )
A.X體積分數保持不變,說明反應已經達到平衡狀態 B.若減小Y的濃度,則正反應速率減小,逆反應速率增大 C.0~2s,W的平均反應速率為0.2 mol/(L?s) D.反應達到平衡狀態時,W與M的物質的量濃度比為2:1 組卷:5引用:1難度:0.5
三.非選擇題(共4個大題,共50分)
-
23.在氮及其化合物的化工生產中,對有關反應的反應原理進行研究有著重要意義。
(1)t℃時,關于N2、NH3的兩個反應的信息如表所示。
請寫出t℃時氨氣被一氧化氮氧化生成無毒氣體的熱化學方程式:化學反應 正反應活化能 逆反應活化能 t℃時平衡常數 N2(g)+O2(g)═2NO(g)△H>0 akJ/mol bkJ/mol K1 4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H<0 ckJ/mol dkJ/mol K2 ,t℃時該反應的平衡常數為。(用K1和K2表示)
(2)工業合成氨的原理為:N2(g)+3H2(g)?2NH3(g)圖甲表示在一定體積的密閉容器中反應時,H2的物質的量濃度隨時間的變化。圖乙表示在其他條件不變的情況下,起始投料H2與N2的物質的量之比(設為x)與平衡時NH3的物質的量分數的關系。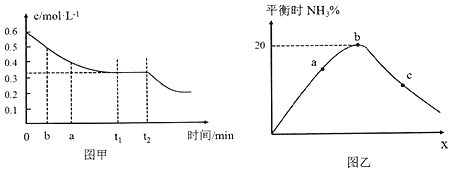
①圖甲中0~t1min內,v(N2)=mol?L-1?min-1;b點的v(H2)正a點的v(H2)逆。(填“大于”、“小于”或“等于”)
②已知某溫度下該反應達平衡時各物質均為1mol,容器體積為1L,保持溫度和壓強不變,又充入3mol N2后,平衡。(填“向右移動”、“向左移動”或“不移動”)組卷:9引用:2難度:0.7 -
 24.CH4-CO2催化重整反應為:CH4(g)+CO2(g)?2CO(g)+2H2(g)。該原理不僅可以得到合成氣(CO和H2),還對溫室氣體的減排具有重要意義。回答下列問題:
24.CH4-CO2催化重整反應為:CH4(g)+CO2(g)?2CO(g)+2H2(g)。該原理不僅可以得到合成氣(CO和H2),還對溫室氣體的減排具有重要意義。回答下列問題:
(1)已知:C(s)+2H2(g)═CH4(g)△H=-75kJ?mol-1
C(s)+O2(g)═CO2(g)△H=-394kJ?mol-1
C(s)+O2(g)═CO(g)△H=-111kJ?mol-112
①催化重整反應的△H=kJ?mol-1。
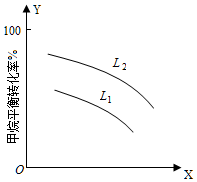
②L(L1、L2)、X可分別代表壓強或溫度。如圖表示L一定時,CH4-CO2催化重整反應中CH4(g)的平衡轉化率隨X 的變化關系。
X代表的物理量是;判斷L1、L2的大小關系L1L2 (填“>”、“<”或“=”),并簡述理由:。
(2)某溫度下,在體積為2L 的容器中加入2mol CH4、1mol CO2以及催化劑進行重整反應,經過2min 達到平衡狀態時測得CO2的轉化率是50%。
①反應達到平衡狀態的標志是(填字母)。
A.單位時間內生成n mol的CH4的同時,生成n mol 的H2
B.c(CH4):c(CO2):c(CO):c(H2)=1:1:2:2
C.反應體系中氣體的總物質的量不變
D.容器中的混合氣體密度不再發生變化
②平均化學反應速率v(CH4)mol?L-1?min-1;其平衡常數為mol2?L-2;若其它條件不變增大壓強,則合成反應的化學平衡常數(填“變大”、“變小”或“不變”)。
③達到平衡后,其它條件不變時向反應容器中充入CO2和CO 各1mol,則化學平衡移動(填“正反應方向”、“逆反應方向”或“不”)組卷:14引用:2難度:0.6


