2021-2022學年山東學情高三(上)聯考化學試卷(B卷)(10月份)
發布:2025/1/1 12:0:3
一、選擇題:本題共10小題,每小題2分,共20分。每小題只有一個選項符合題目要求。
-
1.下列物質的性質與用途均正確,且具有對應關系的是( )
A.氯氣具有漂白性,可用作自來水消毒劑 B.鈉具有很強的還原性,可用鈉與TiCl4溶液反應制取鈦 C.FeCl3溶液呈酸性,可用于刻蝕銅制電路板 D.Fe2O3呈紅棕色,可用作涂料 組卷:16引用:5難度:0.7 -
2.下列說法正確的是( )
A.CO2、SO3、N2O5、Mn2O7均為酸性氧化物 B.NH3、Na2O、SO2水溶液均能導電,它們都是電解質 C.直徑介于1~100nm的微粒稱為膠體 D.工業生產玻璃、水泥和陶瓷,均需用石灰石作原料 組卷:7引用:3難度:0.8 -
3.下列有關實驗操作說法錯誤的是( )
A.蒸餾時應先向冷凝管中通入冷水,再加熱蒸餾燒瓶 B.用二氧化錳與濃鹽酸制備氯氣時,加入濃鹽酸后再加熱 C.用分液漏斗分液時,眼睛注視分液漏斗內的液面 D.將分別盛放氯酸鉀和乙醚的試劑瓶同櫥分層存放 組卷:4引用:4難度:0.5 -
4.設NA為阿伏加德羅常數的值。下列說法正確的是( )
A.120.0gNaHSO4與MgSO4的固體混合物中含有離子總數為2NA B.1.0L1.0mol?L-1的NaHCO3水溶液中含有的氧原子數為3NA C.0.1molFe恰好溶解在100mL某濃度的硝酸溶液中,該反應轉移的電子數為0.3NA D.標準狀況下,22.4LCl2溶于水配成500mL新制氯水,氯水中Cl-數為2NA 組卷:27引用:1難度:0.5 -
5.圖中所給實驗基本操作正確的是( )
A. 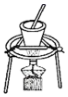
從食鹽溶液中獲得氯化鈉晶體B. 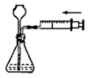
檢查氣密性C. 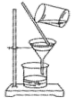
提純Fe(OH)3膠體D. 
灼燒海帶組卷:8引用:4難度:0.5 -
6.對下列事實的解釋中,錯誤的是( )
A.附著在試管內壁上的硫可用CS2洗滌,說明硫易溶于CS2 B.濃硝酸在光照下顏色變黃,說明濃硝酸不穩定 C.向某溶液中加足量稀鹽酸無現象,再加BaCl2溶液產生白色沉淀,說明該溶液中一定有SO42- D.常溫下濃硫酸可以用鐵質容器貯存,說明鐵與濃硫酸不反應 組卷:112引用:3難度:0.7
三、非選擇題(本題共5小題,共60分)
-
19.鎳是一種常用的催化劑。以紅土鎳礦(主要含有Fe2O3、FeO、NiO、SiO2等)為原料,制取納米鎳粉,同時獲得凈水劑黃鈉鐵礬[NaFe3(SO4)2(OH)6]的工藝流程如圖。
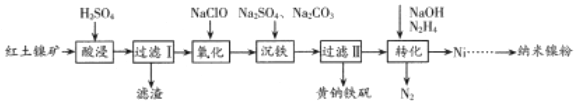
回答下列問題:
(1)濾渣的主要成分是(寫化學式)。
(2)“氧化”過程發生反應的離子方程式是。
(3)“沉鐵”過程,控制不同的條件可以得到不同的沉淀,所得沉淀與溫度、pH的關系如圖所示(圖中陰影部分表示的是黃鈉鐵礬穩定存在區域)。若反應在80℃時進行,加碳酸鈉偏多,則所得黃鈉鐵礬中混有的雜質是;檢驗沉鐵反應是否完全的方法是。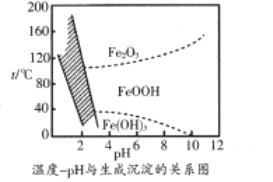
(4)“轉化”過程,向“過濾Ⅱ”所得濾液(富含Ni2+)中加入N2H4,控制溶液中NaOH的濃度,可得到不同晶態物質(NiSO4?N2H4、Ni或二者的混合物)。寫出生成Ni的離子方程式;在其他條件不變的情況下,隨NaOH濃度增大,產物中Ni的含量增加,原因是。
(5)化學鍍鎳是金屬表面鍍鎳的常用方法,以NiSO4為鍍液,次亞磷酸鈉(NaH2PO2)為還原劑,在90℃的酸性溶液中發生反應,NaH2PO2被氧化為亞磷酸(H3PO3)。寫出化學鍍鎳反應的離子方程式。組卷:39引用:5難度:0.4 -
 20.CuCl在染色和催化領域應用廣泛。實驗室利用如圖裝置(加熱和夾持裝置略去)將二氧化硫通入新制氫氧化銅懸濁液中制備CuCl。
20.CuCl在染色和催化領域應用廣泛。實驗室利用如圖裝置(加熱和夾持裝置略去)將二氧化硫通入新制氫氧化銅懸濁液中制備CuCl。
已知:Ⅰ.CuCl為白色固體,難溶于水和乙醇,能溶于濃鹽酸;
Ⅱ.Cu2O+2H+═Cu+Cu2++H2O,CuCl+HCl═HCuCl2,HCuCl2CuCl↓+HCl。稀釋
實驗步驟如下:向C中加入15mL 0.5mol?L-1的CuCl2溶液中,加入0.5mol?L-1的NaOH溶液30mL;打開A中分液漏斗的活塞產生SO2氣體,一段時間后C中產生白色固體,將C中混合物過濾、依次用水和乙醇洗滌,所得固體質量為0.597g。
(1)試劑a為,儀器b名稱為。
(2)B裝置的作用是。
(3)將二氧化硫通入C中新制氫氧化銅懸濁液,產生白色固體的離子方程式為。
(4)用乙醇洗滌CuCl的優點為,判斷CuCl洗滌干凈的實驗方案是。
(5)計算該實驗中CuCl的產率。
(6)若所得CuCl固體中混有少量Cu2O,請設計除去Cu2O的實驗方案:。組卷:22引用:3難度:0.5


