2023年山東省青島市高考化學一模試卷
發布:2024/11/24 9:30:6
一、選擇題:本題共10小題,每小題2分,共20分.每小題只有一個選項符合題意.
-
1.2022年中國十大科技新聞之一是物理化學科學家聯合突破海水無淡化原位直接電解制氫技術,向大海要水要資源又有新進展。下列說法正確的是( )
A.該過程將化學能轉化為電能 B.H2O、D2O、T2O互為同位素 C.氫能源代替化石能源可緩解海水酸化 D.實驗室電解水常加入少量稀鹽酸增強導電性 組卷:56引用:4難度:0.7 -
2.疊氮化鉛[Pb(N3)2]用作水下引爆劑,可由以下方法制得
Ⅰ:N2O+Na+NH3→NaOH+NaN3+N2;
Ⅱ:NaN3+Pb(NO3)2→NaNO3+Pb(N3)2。
下列說法正確的是( )A.NH3的鍵角大于 的鍵角NO-3B.N2O為非極性分子 C.反應Ⅰ中氧化劑和還原劑的物質的量之比可能為3:5 D.反應Ⅰ每消耗23g鈉,共轉移1mol電子 組卷:44引用:2難度:0.7 -
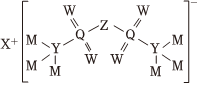 3.軟包電池的關鍵組件結構如圖所示。X、Y、Z、W、M、Q為原子序數依次增大的短周期元素,X元素最外層電子數是次外層電子數的一半,W和Q同主族。下列說法錯誤的是( )
3.軟包電池的關鍵組件結構如圖所示。X、Y、Z、W、M、Q為原子序數依次增大的短周期元素,X元素最外層電子數是次外層電子數的一半,W和Q同主族。下列說法錯誤的是( )A.簡單離子半徑Q>M>W>X B.簡單氣態氫化物的熱穩定性M>W>Q C.常溫下M單質可以置換出W單質 D.W3為V形分子,其沸點高于W2 組卷:59引用:3難度:0.5 -
 4.黑磷具有與石墨相似的層狀結構,其結構如圖所示。下列分析錯誤的是( )
4.黑磷具有與石墨相似的層狀結構,其結構如圖所示。下列分析錯誤的是( )A.黑磷中既存在非極性共價鍵又存在范德華力 B.黑磷的熔點高于白磷 C.黑磷中P原子雜化方式為sp3 D.第三周期只有Cl元素的第一電離能大于P 組卷:58引用:3難度:0.7 -
5.氧化法制備聯苯衍生物的轉化過程如圖所示。下列說法錯誤的是( )

A.②→③發生消去反應 B.②③中最多處于同一平面的碳原子數相同 C.⑤的苯環上的一氯代物有6種 D.1mol④與濃溴水反應最多可消耗3molBr2 組卷:50引用:2難度:0.7 -
6.下列實驗操作規范的是( )

A.①灼燒干海帶 B.②檢驗銅與濃硫酸反應的氧化產物 C.③用CCl4萃取碘水中的碘,振蕩、放氣 D.④配制溶液定容后搖勻 組卷:47引用:4難度:0.7
三、非選擇題:本題共5小題,共60分.
-
19.三水合草酸合鐵(Ⅲ)酸鉀{Kx[Fe(C2O4)y?3H2O],x、y均為整數}常用于化學光量計。實驗室用FeCl3(易潮解,易升華)和K2C2O4為原料制備,實驗步驟如圖:
Ⅰ.無水FeCl3的制備:
(1)儀器連接順序為A→(儀器不重復使用)。
(2)B中冷水的作用為。
Ⅱ.三水合草酸合鐵(Ⅲ)酸鉀晶體的制備:
稱取一定質量草酸鉀固體,加入蒸餾水,加熱。溶解。90~95℃時,邊攪拌邊向草酸鉀溶液中加入過量FeCl3溶液。將上述溶液置于冰水中冷卻至綠色晶體析出。用布氏漏斗過濾、乙醇洗滌、干燥得三水合草酸合鐵酸鉀晶體。整個過程需避光。
(3)用無水FeCl3配制所需FeCl3溶液,下列儀器中不需要的是(填儀器名稱)。
(4)乙醇代替水洗滌的目的是。
Ⅲ.晶體組成的測定及誤差分析
取少量晶體配成溶液,用0.0200mol?L-1標準酸性高錳酸鉀溶液進行第一次滴定,達終點時消耗18.00mL標準液,向滴定后的溶液中加入過量鋅粒將Fe3+還原為Fe2+。過濾,用該高錳酸鉀溶液進行第二次滴定,終點時消耗2.95mL標準液(雜質不反應)。
(5)第二次滴定時的離子反應方程式為。
(6)Kx[Fe(C2O4)y]?3H2O中y=。下列情況會導致y偏高的是。(填標號)。
A.樣品中含有草酸鉀雜質
B.第一次滴定前尖嘴有氣泡,滴定后氣泡消失
C.第二次滴定終點讀數時仰視
D.第二次滴定終點時顏色為深紫紅色組卷:51引用:2難度:0.6 -
20.CH4與CO2的干法重整(DRM)反應可同時轉化兩種溫室氣體,并制備CO和H2.主要反應如下:
反應Ⅰ:CH4(g)+CO2(g)?2CO(g)+2H2(g)ΔH1;
反應Ⅱ:CH4(g)+3CO2(g)?4CO(g)+2H2O(g)ΔH2;
反應Ⅲ:CO(g)+H2O(g)?CO2(g)+H2(g)ΔH3
已知:反應Ⅰ、Ⅱ的自發均需高溫條件.
(1)上述三個反應的平衡常數Kp、ΔH與溫度T關系如圖1所示.圖中a點代表的是(填“Ⅰ”、“Ⅱ”或“Ⅲ”)反應的ΔH,ΔH3=kJ?mol-1.
(2)向密閉容器中,通入3molCO2和1molCH4,若僅考慮上述反應,平衡時CO2、CH4、CO、H2的物質的量隨溫度T的變化如圖2所示.
900K時,CH4的物質的量分數為,用各物質的物質的量分數表示反應Ⅲ的平衡常數Kx=.900K后隨溫度升高,H2物質的量減少的原因為.
(3)DRM反應目前普遍存在的一個難題是積碳,該過程與兩個反應有關
①CH4C+2H2 ΔH>0;Ni
②2CO?C+CO2 ΔH<0.
目前積碳問題的解決方案主要有兩種:A.提高原料氣中CO2的占比;B.在常規的Ni催化劑中添加MgO,使其在催化劑表面與Ni形成共熔物.試解釋這兩種方法可以有效抑制積碳的原因(答出兩條即可).
(4)使用CaO/Fe3O4/Ni復合催化劑,可顯著提高二氧化碳的轉化率,實現碳氫分離,并得到富含CO的產物,催化機理如圖3所示.請用化學方程式解釋Fe3O4循環的原理. 組卷:83引用:2難度:0.3
組卷:83引用:2難度:0.3


