2021年河南省洛陽市高考化學第二次統考試卷
發布:2024/12/4 2:30:2
一、選擇題(共7小題,每小題0分,滿分0分)
-
1.化學與生活密切相關。下列說法錯誤的是( )
A.核酸檢測是確認病毒類型的有效手段,核酸是高分子化合物 B.酸雨是指pH<7的雨水,主要是由空氣中SO2含量偏高引起 C.過氧乙酸含過氧鍵而具有強氧化性 D.我國北斗導航系統所用的芯片中含高純硅 組卷:25引用:1難度:0.8 -
2.以CO2和Na2O2為原料,制取純凈干燥的O2,實驗裝置如圖。下列說法正確的是( )
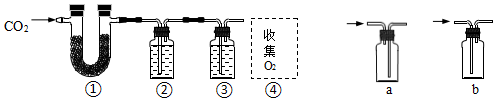
A.裝置②中試劑可以是飽和NaHCO3溶液 B.裝置③的作用是檢查CO2是否除凈 C.收集氧氣應選擇裝置a D.裝置②、③之間應增加盛澄清石灰水的洗氣瓶 組卷:26引用:3難度:0.5 -
3.2019年是“國際化學年”。元素周期表是學習化學的基本工具。已知W、X、Y、Z均為短周期元素,原子序數依次增加,其中W、X、Z組成的化合物M、N、R之間存在如圖所示的反應。下列敘述不正確的是( )

A.元素非金屬性的順序為Z>Y>X>W B.M、N、R三種分子中,M、N屬于非極性分子 C.M、N、R三種分子均含有極性鍵和非極性鍵 D.W、X、Y、Z四種元素既可形成離子化合物,又可形成共價化合物 組卷:15引用:1難度:0.5 -
4.如圖為有機物M、N、Q的轉化關系,有關說法不正確的是( )
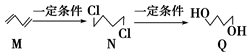
A.M生成N的反應類型是加成反應 B.可用酸性KMnO4溶液區分N與Q C.N的同分異構體有8種 D.0.3mol Q與足量金屬鈉反應生成6.72L H2 組卷:24引用:3難度:0.6
[化學一選修3:物質結構與性質]
-
 11.鋁、鋅、鐵、銅等在人類生產和生活中有重要作用,也是人體必需的微量元素。回答下列問題:
11.鋁、鋅、鐵、銅等在人類生產和生活中有重要作用,也是人體必需的微量元素。回答下列問題:
(1)Zn2+電子排布式為,Cu的基態原子能級最高的電子的電子云輪廓圖形狀為。
(2)鋅的沸點(907℃)較低,宜與銅熔合制成黃銅。已知Zn與Cu的能量變化如圖所示:
Cu(g)Cu+(g)+769kJ?mol-1①Cu2+(g)+1958kJ?mol-1②
Zn(g)Zn+(g)+906kJ?mol-1③Zn2+(g)+1733kJ?mol-1④
試解釋步驟②吸收能量大于步驟④的原因。
在Cu催化下,甲醇可被氧化為甲醛,甲醛分子中碳氫鍵之間的夾角(填“大于”、“等于”或“小于”)120°甲醛能與水形成氫鍵,請在圖中表示出來。
(3)金屬鋅采取如圖所示堆積方式:該堆積方式類型為。 Zn2+可形成[Zn(NH3)4]SO4絡合物,1 mol[Zn(NH3)4]2+配離子中含σ鍵mol,其配體中心原子的雜化方式是。
(4)FeCl3中的化學鍵具有明顯的共價性,蒸汽狀態下以雙聚分子存在的FeCl3的結構式為。
(5)Fe和N可組成一種過渡金屬氮化物,其晶胞如圖所示。六棱柱底邊邊長為xcm,高為y cm,晶胞的密度為ρg?cm-2,則阿伏加德羅常數NA的值為。(列出計算式即可)。組卷:8引用:1難度:0.5
[化學一有機化學基礎]
-
12.磷酸氯喹是一種抗瘧藥物,臨床發現它對新冠肺炎有療效,被國家衛健委推薦用于治療新冠肺炎。磷酸氯喹的有效成分為氧喹,一種合成氯喹路線如圖所示。
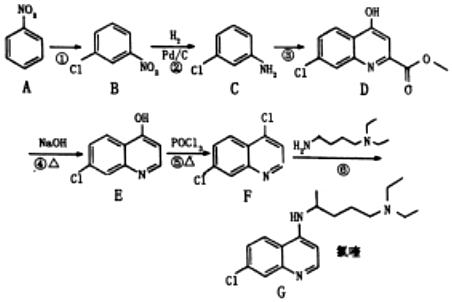
制得的氧喹與磷酸反應即可得到磷酸氧喹(與磷酸形成有機鹽增大在水中的溶解度)
已知:①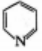 和
和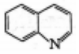 屬于芳香化合物,其性質均類似于苯;
屬于芳香化合物,其性質均類似于苯;
②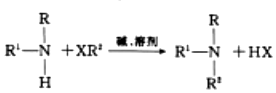 ,R3、R2為烷基,R為烷基或氫。
,R3、R2為烷基,R為烷基或氫。
回答下列問題:
(1)化合物A的化學名稱為。
(2)寫出一種含六元環(不含苯環)的C的芳香同分異構體結構簡式。
(3)化合物D中含氧官能團的名稱為。
(4)反應⑤的反應類型是。
(5)根據步驟⑥中的反應結果,分析推測化合物F中兩個氯活性的差異。
(6)反應①中,在1.0mol硝基苯中通入不同量的氯氣5.0h,產品含量如表1所示,根據反應物的性質,說明產品含量隨氯氣量的增大先增大后減小的原因。
(7)根據表1和表2,為步驟①選擇合適的反應條件并說明理由。
表1氯氣的量與產品含量的關系
表2反應時間與產品含量的關系氯氣的量/mol 0.66 0.68 0.72 0.74 0.76 產品含量/% 71.2 73.3 74.8 74.1 72.0
(8)步驟②在實驗室中通常用鈀碳催化氫氣進行還原,在實際工業生產中使用鐵粉和鹽酸還原,分析還原劑的優缺點反應時間/h 3.0 3.5 4.0 4.5 5.0 產品含量/% 70.9 73.1 74.5 74.7 74.8 。
(9)以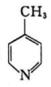 為原料合成
為原料合成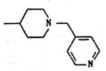 。(無機試劑任選)組卷:16引用:1難度:0.5
。(無機試劑任選)組卷:16引用:1難度:0.5


